
【题目】一种以海水晒盐后所得苦卤(溶质主要含MgCl2,还有NaCl等)为原料制取金属镁的流程如图:
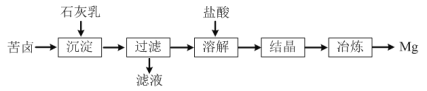
(1)“沉淀”反应的化学方程式为___。
(2)“溶解”反应的离子方程式为___。
(3)工业上冶炼镁时采用的方法是___(填字母)。
a.电解熔融MgCl2
b.用氢气还原MgCl2
c.加热分解MgCl2
【答案】MgCl2+Ca(OH)2=Mg(OH)2+CaCl2 Mg(OH)2+2H+=Mg2++2H2O a
【解析】
苦卤中除MgCl2外还含有NaCl,其与石灰乳混合后,MgCl2会转化为Mg(OH)2沉淀,而NaCl不反应;因此过滤后,需要用其滤渣来制备金属镁;滤渣在用盐酸溶解后,即可得到MgCl2溶液,进一步获得无水氯化镁,再通过电冶金的方式即可获得镁单质。
(1)通过分析可知,“沉淀”步骤发生的是MgCl2与Ca(OH)2的反应,方程式为MgCl2+Ca(OH)2=Mg(OH)2+CaCl2;
(2)通过分析可知,“溶解”步骤是将Mg(OH)2沉淀溶解,离子方程式为Mg(OH)2+2H+=Mg2++2H2O;
(3)Mg单质的活泼性较强,其冶炼方法为电冶金法,即电解熔融的MgCl2,答案选a。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.![]() 属于有机物,因此是非电解质
属于有机物,因此是非电解质
B.石油裂化和裂解的目的均是为了将长链烃转化为短链烃
C.煤的气化,液化和干馏都是化学变化
D.等质量的乙烯,丙烯分别充分燃烧,所耗氧气的物质的量一样多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑦在表中的位置,用化学用语回答下列问题:
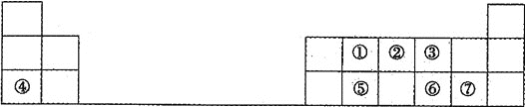
(1)①在周期表中的位置是__,②、⑤原子半径的大小关系为__(填元素符号)。
(2)①、⑤、⑦的最高价含氧酸的酸性由强到弱的顺序是__(填化学式)。
(3)③和⑥的气态氢化物稳定性强弱关系__(填化学式)。
(4)④和⑦两种单质形成的化合物含有的化学键__(填“共价键”或“离子键”),③和⑥两种单质反应的化学方程式__。
(5)②的最简单氢化物与其最高价氧化物对应水化物反应的离子方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)有机物A常用于食品行业。已知9.0 g A在足量O2中充分燃烧,混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4 g和13.2 g,经检验剩余气体为O2。
(1)A分子的质谱图如下图所示,从图中可知其相对分子质量是90,则A的分子式是_______________。
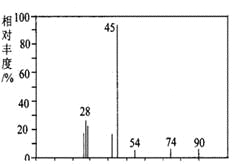
(2)A能与NaHCO3溶液发生反应,A一定含有的官能团名称是__________________。
(3)A分子的核磁共振氢谱有4个峰,峰面积之比是1:1:1:3,则A 的结构简式是_________________________________。
(4)0.1 mol A与足量Na反应,在标准状况下产生H2的体积是__________L。
(5)A在一定条件下可聚合得到一种聚酯,用于制造手术缝合线,其反应的化学方程式是________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸亚铁晶体{[CH3CH(OH)COO]2Fe·3H2O,相对分子质量为288}易溶于水,是一种很好的补铁剂,可由乳酸[CH3 CH(OH)COOH]与FeCO3反应制得。
I.碳酸亚铁的制备(装置如下图所示)

(1)仪器B的名称是__________________;实验操作如下:打开kl、k2,加入适量稀硫酸,关闭kl,使反应进行一段时间,其目的是__________________。
(2)接下来要使仪器C中的制备反应发生,需要进行的操作是____________,该反应产生一种常见气体,写出反应的离子方程式_________________________。
(3)仪器C中混合物经过滤、洗涤得到FeCO3沉淀,检验其是否洗净的方法是__________。
Ⅱ.乳酸亚铁的制备及铁元素含量测定
(4)向纯净FeCO3固体中加入足量乳酸溶液,在75℃下搅拌使之充分反应,经过滤,在____________的条件下,经低温蒸发等操作后,获得乳酸亚铁晶体。
(5)两位同学分别用不同的方案进行铁元素含量测定:
①甲同学通过KMnO4滴定法测定样品中Fe2+的含量计算样品纯度。在操作均正确的前提下,所得纯度总是大于l00%,其原因可能是_________________________。
②乙同学经查阅资料后改用碘量法测定铁元素的含量计算样品纯度。称取3.000 g样品,灼烧完全灰化,加足量盐酸溶解,取所有可溶物配成l00mL溶液。吸取25.00 rnL该溶液加入过量KI溶液充分反应,然后加入几滴淀粉溶液,用0. 100 mol·L-1硫代硫酸钠溶液滴定(已知:I2+2S2O32-=S4O62-+2I-),当溶液_____________________,即为滴定终点;平行滴定3次,硫代硫酸钠溶液的平均用量为24.80 mL,则样品纯度为_________%(保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置完成相关实验,不合理的是( )
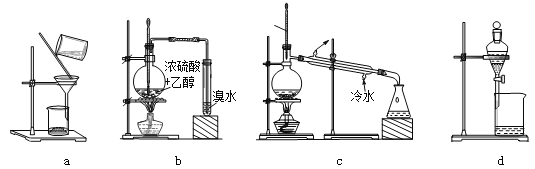
A. 用a趁热过滤提纯苯甲酸B. 用b制备并检验乙烯
C. 用c除去溴苯中的苯D. 用d分离硝基苯与水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( )
A.S![]() SO3
SO3![]() H2SO4B.Al2O3
H2SO4B.Al2O3![]() NaAlO2(aq)
NaAlO2(aq) ![]() Al(OH)3
Al(OH)3
C.SiO2 ![]() SiCl4
SiCl4![]() SiD.Fe2O3
SiD.Fe2O3![]() FeCl3(aq)
FeCl3(aq) ![]() 无水FeCl3
无水FeCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是一种有机光电材料中间体。实验室由芳香化合物A制备H的一种合成路线如下:

已知:①![]()
![]()
![]()
②
回答下列问题:
(1)A物质所含官能团的名称和结构简式为_____________。
(2)E的结构简式为_____________。
(3)G为甲苯的同分异构体,由F生成H的化学方程式为_____________。
(4)芳香化合物X是F的同分异构体,X能与饱和碳酸氢钠溶液反应放出CO2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6:2:1:1,写出一种符合要求的X的结构简式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数,下列说法不正确的是( )
A.1.5 mol NO2与足量的H2O反应,转移的电子数为NA
B.常温常压下,18g D2O含有的原子数为3NA
C.氧气和臭氧的混合物32 g中含有2NA个氧原子
D.在标准状况下,0.5NA个氯气分子所占体积约是11.2 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com