
| A、强电解质和弱电解质的本质区别在于电离程度的不同 |
| B、中性溶液中既没有H+也没有OH- |
| C、pH=4的溶液稀释10000倍,会成为碱性溶液 |
| D、向缓冲溶液中加入少量的酸或碱时,溶液的pH基本不发生变化 |


科目:高中化学 来源: 题型:
| A、由水电离出的c(H+)=l×10-12mol/L、的溶液中:K+、Ba2+、OH-、NO3- |
| B、澄清透明的溶液中:I-、Cl-、ClO-、Na+ |
| C、使pH试纸呈红色的溶液中:K+、Fe2+、NO3-、MnO4- |
| D、含有S2O32-的溶液中:K+、Na+、H+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定有甲烷 |
| B、一定有乙烷 |
| C、一定含有甲烷,不一定含有乙烷 |
| D、可能是甲烷和丙烷的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 与醇形成的酯类化合物,主要用作有机合成、食品、化妆品、医药的杀菌防腐剂,也用作于饲料防腐剂.下列说法中正确的是( )
与醇形成的酯类化合物,主要用作有机合成、食品、化妆品、医药的杀菌防腐剂,也用作于饲料防腐剂.下列说法中正确的是( )| A、尼泊金乙酯与NaOH溶液反应时,可消耗1mol NaOH |
| B、尼泊金乙酯分子结构中,至少有6个碳原子在一个平面内 |
| C、尼泊金丁酯最多可与4mol H2发生加成反应 |
D、尼泊金丁酯是由对羟基苯甲酸与1-丁醇形成的酯,结构简式如图: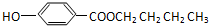 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、反应I2(aq)+I-(aq)?I3-(aq)的△H<0 |
| B、若温度为T1、T2,反应物的转化率分别为a1、a2,则a1>a2 |
| C、若反应进行到状态D时,一定有v正<v逆 |
| D、状态A与状态B相比,状态B的c(I2)大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蔗糖和麦芽糖的水解产物完全相同 |
| B、蔗糖与麦芽糖互为同分异构体 |
| C、蔗糖与麦芽糖的分子式都是C12H22O11 |
| D、麦芽糖能发生银镜反应,蔗糖不能发生银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、强电解质溶液导电能力一定比弱电解质溶液导电能力强 |
| B、水的电离过程是吸热过程,升高温度,KW和pH都增大 |
| C、AlCl3和FeCl3既可作净水剂也可作消毒剂 |
| D、将碳酸钠溶液蒸干并灼烧,所得固体的成分仍为碳酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
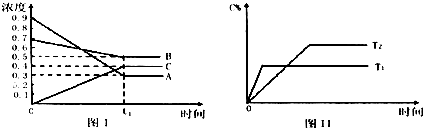
| A、在时间为t1时,保持其他条件不变,增大压强,平衡向逆反应方向移动 |
| B、在时间为t1时,保持温度和压强不变,通入稀有气体,平衡向正反应方向移动 |
| C、其它条件不变,T℃时由0.6 mol/LA、0.6mol/LB、0.2mol/LC开始反应,达到平衡后C的浓度仍为0.4mol/L |
| D、其它条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com