
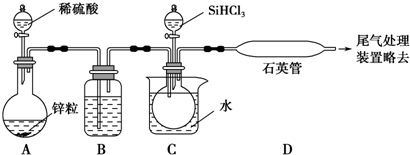
分析 根据题目给出的信息,高温下,碳做还原剂时,碳和二氧化硅生成CO和硅;利用沸点的不同提纯SiHCl3属于蒸馏;浓硫酸是常用的干燥剂,装置C需水浴加热,目的是加快反应的速率;装置D不能采用普通玻璃管的原因是温度太高,普通玻璃管易熔化;保证实验成功的关键是:装置要严密;控制好温度等.
(1)高温下,碳和二氧化硅反应生成硅和一氧化碳;
(2)根据题中数据,采用分馏方法提纯SiHCl3;
(3)浓硫酸是常用的干燥剂,装置C需水浴加热,目的是使SiHCl3气化,与氢气反应;SiHCl3与过量的H2在1000℃~1100℃反应制得纯硅,温度太高,普通玻璃管易熔化;保证实验成功的关键是:装置要严密;控制好温度等;书写化学方程式时,要注意配平.
解答 解:(1)高温下,碳做还原剂时,生成CO,即2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
故答案为:2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑
(2)利用沸点的不同提纯SiHCl3属于蒸馏,
故答案为:蒸馏(或分馏)
(3)①生成的氢气含有水蒸气,用浓H2SO4干燥;加热促使SiHCl3气化,
故答案为:浓硫酸;使SiHCl3气化,与氢气反应;
②SiHCl3和氢气反应有硅单质生成,根据硅的颜色判断D装置中的颜色变化;反应温度较高,普通玻璃会软化;SiHCl3和H2反应生成硅和氯化氢,
故答案为:有固体物质生成,温度太高,普通玻璃管易熔化;SiHCl3+H2$\frac{\underline{\;1100℃-1200℃\;}}{\;}$Si+3HCl;
③氢气是可燃性气体,易产生爆炸,为防止安全事故的发生,所以先通一段时间H2,将装置中的空气排尽.
故答案为:排尽装置中的空气.
点评 本考点属于物质的转化和制备题,还考查了化学方程式的书写.本题利用文字描述设计出相应的实验步骤,分步骤进行鉴别,解决本考点需要根据实验现象,综合分析,从而得出正确的结论,要注意知识的整体性.此考点主要出现在实验题中.


科目:高中化学 来源: 题型:解答题
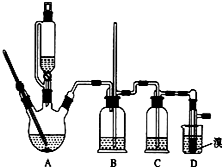 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
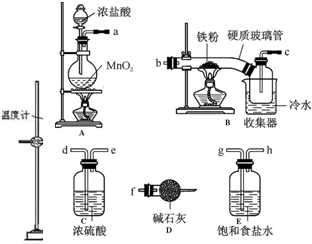

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
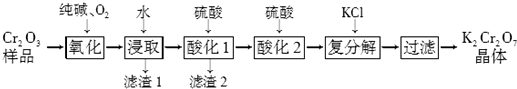
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
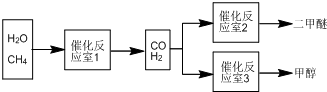
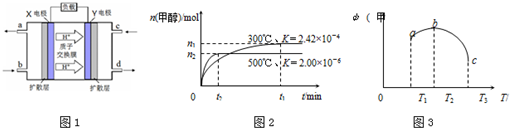
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
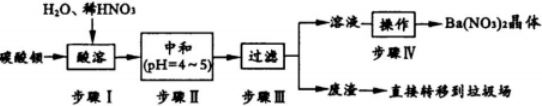
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
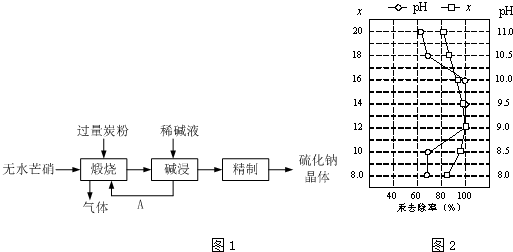
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com