
【题目】下列离子方程式,正确的是
A. 澄清石灰水中通入过量二氧化碳:Ca2+ +2OH +CO2 =CaCO3↓+H2O
B. 碳酸钠溶液中加入二氧化硅:CO32 +SiO2=SiO32 +CO2↑
C. 二氧化硅与烧碱溶液反应:SiO2 +2OH =SiO32+H2↑
D. 硅酸与烧碱溶液中和:H2SiO3 +2OH = SiO32+2H2O
科目:高中化学 来源: 题型:
【题目】如图是Zn和Cu形成的原电池,回答下列问题:
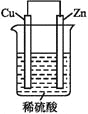
(1)正极发生____反应(选填“氧化”或“还原”),负极电极反应式为:____。
(2)电子流动方向,从____电极(选填“Cu”或“Zn”),经外电路,流向另一电极。阳离子向____电极定向移动(选填“Cu”或“Zn”)。
(3)有0.1 mol电子流过导线,则产生H2在标准状况下的体积为____,若是断开Zn和Cu之间的导线,产生气泡的速度____(选填“加快”、“不变”或“减慢”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E五种物质,且A、B、C、D的焰色反应呈黄色,它们的关系如下图所示,已知E为气体单质,能使带火星的木条复燃。

(1)写出下列物质的化学式:A ,B C ,
D ,E 。
(2)写出A受热分解的化学方程式: 。
(3)写出Y与C反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)利用太阳光分解水制氢是未来解决能源危机的理想方法之一。某研究小组设计了如下图所示的循环系统实现光分解水制氢。反应过程中所需的电能由太阳能光电池提供,反应体系中I2和Fe2+等可循环使用。
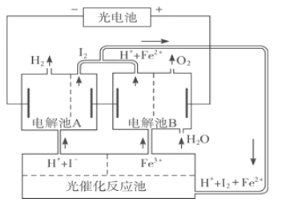
(1)写出电解池A、电解池B和光催化反应池中反应的离子方程式。
(2)若电解池A中生成3.36 L H2(标准状况),电解池B中生成Fe2+的物质的量为 。
(3)若循环系统处于稳定工作状态时,电解池A中流入和流出的HI浓度分别为a mol·L-1和b mol·L-1,光催化反应生成Fe3+的速率为c mol·L-1,循环系统中溶液的流量为Q(流量为单位时间内流过的溶液体积)。试用含所给字母的代数式表示溶液的流量Q。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 按系统命名,有机物CH3CH(C2H5)CH(CH3)2的名称是 ( )
A.1,3-二甲基戊烷 B.2-甲基-3-乙基丁烷
C.3,4-二甲基戊烷 D.2,3-二甲基戊烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】24Cr原子处于基态时,价电子排布可用电子排布图表示成![]() ,而不是
,而不是![]() 。下列说法中,正确的是()
。下列说法中,正确的是()
A. 这两种排布方式都符合能量最低原理
B. 这两种排布方式都符合泡利原理
C. 这两种排布方式都符合洪特规则
D. 这个实例说明洪特规则有时候和能量最低原理是矛盾的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是
A. 加热
B. 不用稀硫酸,改用98%的硫酸
C. 滴加少量CuSO4溶液
D. 不用铁片,改用铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可用食盐和石灰石为主要原料,经不同的方法生产纯碱。请回答下列问题:
(1)卢布兰芳是以食盐、石灰石、浓硫酸、焦炭为原料,在高温下进行煅烧,再浸取,结晶而制得纯碱。
①食盐和浓硫酸反应的化学方程式为 _;
②硫酸钠和焦炭、石灰石反应的化学方程式为_ (已知产物之一为CaS);
(2)氨碱法的工艺如下图所示,得到的碳酸氢钠经煅烧生成纯碱。
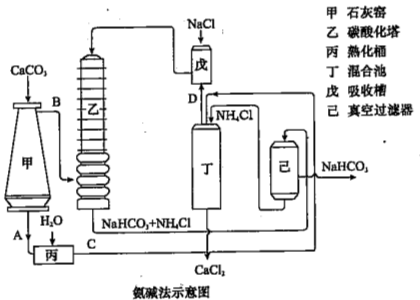
①图中的中间产物C是_______,D_______。(写化学式);
②装置乙中发生反应的化学方程式为 ;
(3)联合制碱法对氨碱法的改进,其优点是 ;
(4)有人认为碳酸氢钾与碳酸氢钠的化学性质相似,故也可用氨碱法以氯化钾和石灰石为原料制碳酸钾。请结合下图的溶解度(S)随温度变化曲线,分析说明是否可行?
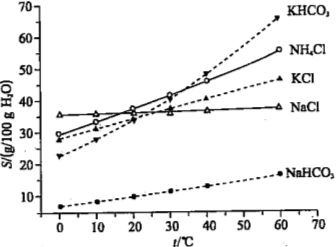
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用下图所示的装置制取乙酸乙酯。回答下列问题:
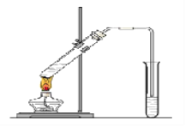
(1)写出制取乙酸乙酯的化学反应方程式: 。
(2)饱和碳酸钠溶液的主要作用是: 。
(3)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是: 。
(4)应结束后,振荡试管b,静置。观察到的现象是 。
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是(填名称): 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com