
【题目】等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间(t)产生氢气体积(V)的数据,根据数据绘制如图,则曲线a、b、c、d所对应的实验组别可能是( )

组别 | c(HCl)/(molL-1) | 温度/℃ | 状态 |
1 | 2.0 | 25 | 块状 |
2 | 2.5 | 30 | 块状 |
3 | 2.5 | 50 | 粉末状 |
4 | 2.5 | 30 | 粉末状 |
A.④—③—②—①B.①—②—③—④
C.③—④—②—①D.①—②—④—③
科目:高中化学 来源: 题型:
【题目】微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,总反应为Ag2O+Zn=ZnO+2Ag,其中一个电极反应为Ag2O+H2O+2e-=2Ag+2OH-。

(1)正极材料为___________。
(2)写出另一电极的电极反应式__________。
(3)在电池使用的过程中,电解质溶液中KOH的物质的量怎样变化?________(增大、减小、不变)。
(4)当电池工作时通过电路对外提供了1mol电子,计算消耗的负极的质量_______。
(5)利用下列反应:Fe+2Fe3+=3Fe2+设计一个原电池,请选择适当的材料和试剂。
①电解质溶液为_____________。
②负极反应式:____________________。
③溶液中Fe3+向__________极移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应mA(g)+nB(s)![]() pC(g)+qD(g),在反应过程中,当其他条件不变时,D的百分含量与温度(T)和压强(P)的关系如图所示,判断下列叙述中不正确的是:
pC(g)+qD(g),在反应过程中,当其他条件不变时,D的百分含量与温度(T)和压强(P)的关系如图所示,判断下列叙述中不正确的是:
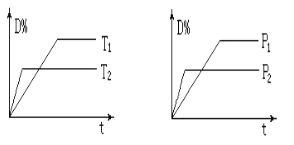
A. 达到平衡后,升高温度,平衡向逆反应方向移动
B. 达到平衡后,若使用催化剂,D的物质的量分数不变
C. 化学方程式中一定有m<p+q
D. 平衡后增大B的量,有利于平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时草酸(H2C2O4)的电离常数为K1=5.0×10-2,K2=5.4×10-5,草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9。不同温度下水的离子积常数见下表:
t/℃ | 0 | 10 | 20 | 25 | 40 | 50 | 90 | 100 |
Kw/10-14 | 0.134 | 0.292 | 0.681 | 1.00 | 2.92 | 5.57 | 38.0 | 55.0 |
(1)常温下将0.2 mol/L的KOH溶液20 mL与0.2 mol/L的草酸溶液20 mL混合后溶液显酸性,则混合后溶液中各离子浓度的大小顺序为__________________________________;
(2)已知草酸能使酸性高锰酸钾溶液(稀硫酸酸化)褪色,若在锥形瓶中放入20.00mL未知浓度的草酸,用0.1mol/L高锰酸钾溶液滴定,当到达滴定终点时,若共消耗VmL高锰酸钾溶液,则草酸的物质的量浓度为__________mol/L。
(3)90℃时,将0.005 mol/L的氢氧化钙溶液20 mL与0.0012 mol/L的草酸溶液20 mL混合,混合后溶液的pH=___________;
(4)25℃时若向20 mL草酸钙的饱和溶液中逐滴加入8.0×10-4 mol/L的碳酸钾溶液10 mL,能否产生沉淀,___________(填“能”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 某温度下,一元弱酸HA的Ka越小,则NaA的Kh(水解平衡常数)越小
B. 铁管镀锌层局部破损后,铁管仍不易生锈
C. 铜既可以发生析氢腐蚀又可以发生吸氧腐蚀
D. 不能用红外光谱区分C2H5OH和CH3OCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒压下,向密闭容器中充入4 mol SO2和2 mol O2,发生如下反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0,2min后,反应达到平衡,生成SO3为1.4 mol,同时放出热量Q kJ。则下列分析正确的是( )
2SO3(g) ΔH<0,2min后,反应达到平衡,生成SO3为1.4 mol,同时放出热量Q kJ。则下列分析正确的是( )
A. 在该条件下,反应前后的压强之比为6∶5.3
B. 若反应开始时容器体积为2 L,则v(SO3)=0.35 mol/(L·min)
C. 若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)<1.4 mol
D. 若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量大于Q kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为______(写离子符号);若所得溶液c(HCO3)∶c(CO32)=2∶1,溶液pH=___________。(室温下,H2CO3的K1=4×107;K2=5×1011)
(2)CO2与CH4经催化重整,制得合成气:
CH4(g)+ CO2(g) ![]() 2CO (g)+ 2H2(g)
2CO (g)+ 2H2(g)
①已知上述反应中相关的化学键键能数据如下:
化学键 | C—H | C=O | H—H | C |
键能/kJ·mol1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=_________。分别在VL恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1 mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是_______(填“A” 或“B ”)。
②按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图3所示。此反应优选温度为900℃的原因是________。

(3)O2辅助的Al~CO2电池工作原理如图4所示。该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料。
电池的负极反应式:________。
电池的正极反应式:6O2+6e![]() 6O2
6O2
6CO2+6O2![]() 3C2O42
3C2O42
反应过程中O2的作用是________。
该电池的总反应式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员研制出一种室温Na-CO2电池。该电池吸收CO2的工作原理如图所示。吸收的全部CO2中,有![]() 转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面。下列说法不正确的是
转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面。下列说法不正确的是
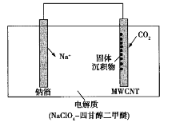
A. 钠箔为负极,发生氧化反应
B. 每吸收22.4 LCO2,转移电子数为![]() mol
mol
C. 正极反应式:4Na++3CO2+4e-=2Na2CO3+C
D. Na+通过电解质移向MWCNT极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图;研究发现在以Fe2O3为主的催化剂上可能发生的反应过程如下图,下列说法正确的是( )

A. 脱硝的总反应为:4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g)
4N2(g)+6H2O(g)
B. NH3催化还原NO为吸热反应
C. 过程1中NH3断裂非极性键
D. 过程中NO为氧化剂,Fe2+为还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com