
| A. | v甲>v乙>v丙 | B. | v乙>v甲>v丙 | C. | v甲>v丙>v乙 | D. | v甲=v乙=v丙 |
分析 不同物质表示的速率之比等于其化学计量数之比,故不同物质的表示的速率与其化学计量数的比值越大,表示的反应速率越快.
解答 解:反应方程式为:N2+3H2=2NH3,不同物质表示的速率之比等于其化学计量数之比,故不同物质的表示的速率与其化学计量数的比值越大,表示的反应速率越快,则:
$\frac{{v}_{甲}({H}_{2})}{3}$=1mol•L-1•min-1;
$\frac{{v}_{乙}({N}_{2})}{1}$=2mol•L-1•min-1;
$\frac{{v}_{丙}(N{H}_{3})}{2}$=0.5mol•L-1•min-1,
故反应速率v乙>v甲>v丙,
故选:B.
点评 本题考查化学反应速率快慢比较,难度不大,利用比值法可以迅速判断,也可以转化同一物质表示的速率进行比较.


科目:高中化学 来源: 题型:填空题
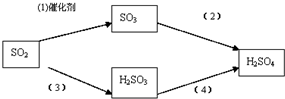 (1)黑火药爆炸时,发生的反应之一为:S+2KNO3+3C$\stackrel{引燃}{→}$K2S+3CO2↑+N2↑,该反应中氧化剂为S、KNO3,1molS能氧化C0.5mol
(1)黑火药爆炸时,发生的反应之一为:S+2KNO3+3C$\stackrel{引燃}{→}$K2S+3CO2↑+N2↑,该反应中氧化剂为S、KNO3,1molS能氧化C0.5mol查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{c(N{H}_{3}•{H}_{2}O)}{c(O{H}^{-})}$ | B. | $\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$ | C. | c(H+)和c(OH-)的乘积 | D. | OH-的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成物能量一定低于反应物总能量 | |
| B. | 放热反应不必加热就一定能发生 | |
| C. | 应用盖斯定律,可计算某些难以直接测量的反应的焓变 | |
| D. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件的△H不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
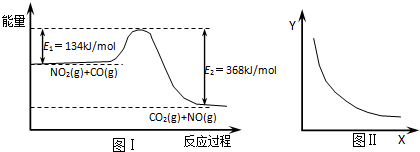
| A. | 该反应的焓变△H=234kJ/mol | |
| B. | 若X表示CO的起始浓度,则Y表示的可能是NO2的转化率 | |
| C. | 若X表示反应时间,则Y表示的可能是混合气体的密度 | |
| D. | 若X表示温度,则Y表示的可能是CO2的物质的量浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①或② | B. | 只有②或④ | C. | 只有①或②或③ | D. | ①②③④中任意一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素 | |
| B. | 在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素 | |
| C. | 在非金属元素区域可以寻找制备新型农药材料的元素 | |
| D. | 最外层电子数为8的粒子是稀有气体元素的原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| 开始沉淀的pH | 7.5 | 2.8 | 4.2 | 9.6 |
| 沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com