
分析 根据反应速率之比等于化学计量数之比判断m,利用三段式法计算相关物理量,
v(D)=$\frac{\frac{0.2mol}{0.4L}}{5min}$=0.1mol•L-1•min-1,又知5min内用E表示的平均反应速率为0.1mol•L-1•min-1,
则v(D):c(E)=0.1mol•L-1•min-1:0.1mol•L-1•min-1=1:1,
反应速率之比等于化学计量数之比,则m=1,则
2A(g)+B(g)?D(g)+E(g)
起始:0.6mol 0.5mol 0 0
转化:0.4mol 0.4mol 0.2mol 0.2mol
平衡:0.2mol 0.1mol 0.2mol 0.2mol
解答 解:v(D)=$\frac{\frac{0.2mol}{0.4L}}{5min}$=0.1mol•L-1•min-1,又知5min内用E表示的平均反应速率为0.1mol•L-1•min-1,
则v(D):c(E)=0.1mol•L-1•min-1:0.1mol•L-1•min-1=1:1,
反应速率之比等于化学计量数之比,则m=1,则
2A(g)+B(g)?D(g)+E(g)
起始:0.6mol 0.5mol 0 0
转化:0.4mol 0.4mol 0.2mol 0.2mol
平衡:0.2mol 0.1mol 0.2mol 0.2mol
(1)由以上计算可知,D、E的反应速率相同,则m=1,
答:m的值为1;
(2)c(A)=$\frac{0.2mol}{0.4L}$=0.5mol•L-1,
答:平衡时A的物质的总浓度0.5mol•L-1;
(3)平衡时混合物总物质的量为0.2mol+0.1mol+0.2mol+0.2mol=0.7mol,
答:平衡时气体的总物质的量0.7mol.
点评 本题考查了化学平衡的计算应用,主要是反应速率,浓度概念的计算分析,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
| MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5 min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30min |
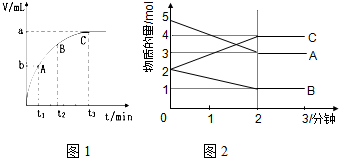
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | X、Y、Z元素分别为N、P、O | |
| B. | 白格中都是主族元素,灰格中都是副族元素 | |
| C. | 原子半径:Z>X>Y | |
| D. | X、Y、Z的气态氢化物中最稳定的是:X的氢化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +2nH2O.
+2nH2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
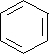 .
. .
.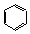 ;CH2=CH2和
;CH2=CH2和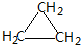 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com