
a.PCl3在热水中水解,产物有H3PO3,结构式为: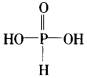
b.H3PO3与NaOH反应,只生成Na2HPO3和NaH2PO3两种盐
c.H3PO3能使碘水褪色,再加入过量AgNO3溶液,生成黄色沉淀M,过滤后再加入CaCO3粉末,又生成黄色沉淀N
d.向H3PO3溶液中加AgNO3溶液,有黑色Ag和棕色气体生成
(1)H2PO3是________元________酸(填“强”或“弱”),具有________性(氧化或还原),与以上判断对应信息分别是a~d中的________、________.
(2)信息c中M是(填化学式)________,N是________,确证M与N是否是同一物质的理论依据是________.
(3)H3PO3与AgNO3溶液反应的化学方程式为_________________,被还原元素为________.
科目:高中化学 来源: 题型:


 (酮也可发生类似的反应)
(酮也可发生类似的反应)

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 键能 | 键能 | 键能 | |||
| H-H | 436 | Cl-Cl | 243 | C-F | 427 |
| H-N | 393 | H-O | ? | H-F | 565 |
| C-Cl | 330 | H-S | 339 | H-Cl | 431 |
| C-O | 347 | C-I | 218 | H-Br | 366 |
查看答案和解析>>
科目:高中化学 来源: 题型:
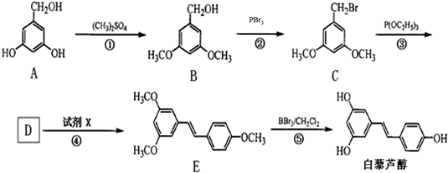
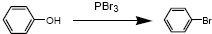
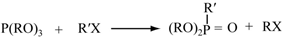
 (酮也可发生类似的反应)
(酮也可发生类似的反应)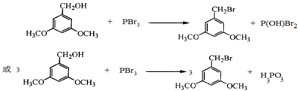



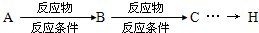
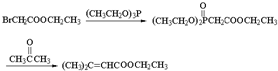

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com