
【题目】下列电子排布图(每一个小方框表示一个原子轨道)所表示元素的原子中,其能量处于最低状态的是( )
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
【答案】A
【解析】
试题A.能级能量由低到高的顺序为:1s、2s、2p;每个轨道最多只能容纳两个电子,且自旋相反,简并轨道(能级相同的轨道)中电子优先单独占据1个轨道,且自旋方向相同,能量最低,故A正确;B.2p能级的3个简并轨道(能级相同的轨道)只有被电子逐一自旋平行地占据后,才能容纳第二个电子,不符合能量最低原理,原子处于能量较高的激发态,故B错误;C.2s能级的能量比3p能量低,电子尽可能占据能量最低的轨道,不符合能量最低原理,原子处于能量较高的激发态,故C错误;D.2s能级的能量比2p能量低,电子尽可能占据能量最低的轨道,不符合能量最低原理,原子处于能量较高的激发态,故D错误;故选A。


科目:高中化学 来源: 题型:
【题目】进一步认识氧化还原反应。氯化铵可除去铜器表面的氧化铜:![]()
(1)氧化还原反应的实质是__________(填写编号)。
A.得氧和失氧 B.化合价的升降 C.有无新物质生成 D.电子的得失和偏移
(2)用单线桥标出上述反应中电子转移的方向和数目________。
(3)上述反应中,氯化铵中N的化合价_______(“升高”或“降低”),_____(“得”或“失”)电子,作____(“氧化剂”或“还原剂”),表现_____(“氧化”或“还原”)性,发生____(“氧化”或“还原”)反应。
(4)氧化剂和还原剂物质的量之比是___。
(5)当生成![]() 11.2 L(标准状况)时,转移___个电子,被还原的CuO__mol。
11.2 L(标准状况)时,转移___个电子,被还原的CuO__mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达到平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )
2SO3(g) ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达到平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )

A. 由图甲知,A点SO2的平衡浓度为0.4 mol·L-1
B. 由图甲知,B点SO2、O2、SO3的平衡浓度之比为2∶1∶2
C. 达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示
D. 压强为0.50 MPa时,不同温度下SO2转化率与温度关系如丙图,则T2>T1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组的学生在实验室用二氧化锰和浓盐酸反应来制取氯气,装置如图:

(1)写出实验室制取氯气的化学反应方程式___。
(2)为了除去氯气中的少量氯化氢气体,可以在收集氯气之前,让氯气经过___(填试剂序号)。为吸收残余氯气,可在烧杯中加入___(填试剂序号)。其化学方程式是___。
A.水 B.浓硫酸 C.饱和食盐水 D.烧碱溶液
(3)兴趣小组成员甲同学认为,此反应装置还可以用来制取___(填编号)。
A.氧气 B.氢气 C.二氧化碳 D.氯化氢
但是,成员乙同学认为,要用整套装置来制取甲同学提出的气体,必须改进其中的___(填编号),理由是___。
A.气体的发生装置 B.气体的收集装置 C.尾气吸收装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将70mLKBr和KI的混合溶液分为两等份。向其中一份通入足量的Cl2,完全反应后蒸发溶液至干,灼烧后得到11.92g固体残留物。测得另一份混合液中I-的物质的量为0.03mol,计算
(1)固体残留物中含有什么物质?____
(2)原溶液中含有KBr的质量是多少?____
(3)与原70mL溶液中的KBr和KI完全反应时,需消耗氯气的体积(标准状况)是多少?____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】决定物质性质的重要因素是物质结构.请回答下列问题.
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:

则,A的化合价__B的化合价(填“>”、“<”或“=”).
(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:

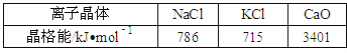
则该 4种离子晶体(不包括NaCl)熔点从高到低的顺序是:__.
(3)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是___________________________.
(4)某配合物的分子结构如图所示,则N原子的杂化方式为__;基态Ni原子的电子排布式__.
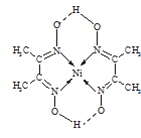
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数依次增大的四种主族元素A,B,C,D分别处于第一至第四周期,其中A元素原子核是一个质子;B元素原子核外电子有6种不同的运动状态,B与C可形成正四面体形分子,D原子外围电子排布为3d104s1。请回答下列问题:
(1)这四种元素中电负性最大的是________(填元素符号),第一电离能最小的是________(填元素符号)。
(2)C所在的主族元素气态氢化物中,沸点最低的是________(填化学式)。
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体结构如图所示,其原子的杂化类型为________杂化。

(4)D的水合醋酸盐晶体局部结构如图所示,该晶体中含有的化学键是________(填选项序号)。

①极性键 ②非极性键 ③配位键 ④金属键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ |
(1)在这些元素中,化学性质最不活泼的是:_____(填元素符号),原子结构示意图为_____ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是_______,碱性最强的化合物的电子式是:_____________。
(3)用电子式表示元素④与⑥的化合物的形成过程:________,该化合物属于_____(填 “共价”或“离子”)化合物。
(4)表示①与H的化合物的化学式_________________,该化合物是由____________(填“极性”“非极性”)键形成的。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化工厂用石墨电解Na2CrO4溶液制备Na2Cr2O7的模拟装置如下图所示,下列有关说法错误的

A. 溶液中OH-由阴极区流向阳极区
B. 阳极的电极反应式为2H2O-4e-=O2↑+4H+
C. 阳极区产生的气体与阴极区产生的气体在相同状况下体积之比为1∶2
D. Na2CrO4转化为Na2Cr2O7的离子方程式为2CrO42-+2H+=Cr2O72-+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com