
| A. | 热化学方程式中的化学计量数表示物质的量,可以是分数 | |
| B. | 应用盖斯定律可计算某些难以直接测量的反应焓变 | |
| C. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| D. | 已知2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol,则氢气的燃烧热为285.8kJ/mol |
分析 A、热化学方程式的化学计量数表示物质的量,不表示分子个数;
B、CO燃烧的反应难以实现,可以通过C燃烧生成二氧化碳的焓变和CO燃烧生成二氧化碳的焓变利用盖斯定律求CO燃烧的焓变;
C、能量越低越稳定;
D、燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量,根据燃烧热的定义判断热化学方程式是否正确.
解答 解:A、热化学方程式的化学计量数表示物质的量,可以是整数也可以是分数,故A正确;
B、CO燃烧的反应难以实现,可以通过C燃烧生成二氧化碳的焓变和CO燃烧生成二氧化碳的焓变利用盖斯定律求CO燃烧的焓变,故B正确;
C、C(石墨,s)═C(金刚石,s)△H>0,则金刚石能量高,则石墨稳定,故C错误;
D、由2H2(g)+O2(g)=2H2O(l)△H=-571.6 kJ/mol,可知1mol氢气完全燃烧生成稳定的氧化物放出的热量为285.8KJ,所以氢气的燃烧热△H=-285.8 kJ/mol,故D正确;
故选:C.
点评 本题虽难度不大,但考查范围广,考查知识基础、全面,是一道好题.


科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.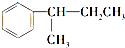 $\stackrel{酸性KMnO_{4}溶液}{→}$
$\stackrel{酸性KMnO_{4}溶液}{→}$ .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 粗铜板作阳极,电解硫酸铜溶液 | 粗铜溶解,纯铜在阴极上析出 | Cu 放电是氧化剂 |
| B | 向银氨溶液中滴加几滴乙醛后 水浴加热 | 银附着在试管壁上 | 乙醛发生还原反 应 |
| C | 向含 I-的无色溶液中滴加少量 新制氯水,再滴加淀粉溶液 | 加入淀粉后溶液变成蓝色 | 氧化性:Cl2>I2 |
| D | 向 FeSO4溶液中先滴入 KSCN 溶液再滴加 H2O2 溶液 | 加入 H2O2后溶液变成血红色 | Fe2+既有氧化性又 有还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某物质经测定,只含有一种组成元素,则该物质一定是单质 | |
| B. | 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 | |
| C. | 碱性氧化物均是金属氧化物,酸性氧化物均是非金属氧化物 | |
| D. | 纯净的硫酸是纯净物,而纯净的盐酸是混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
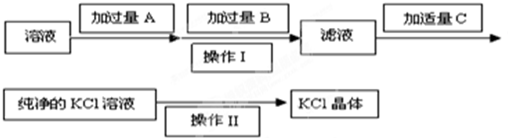
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com