
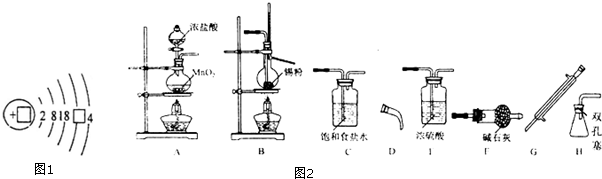
·ÖĪö £Ø1£©Óɽį¹¹Ź¾ŅāĶ¼æÉÖŖ£¬ĪżŹĒµŚĖÄÖÜĘŚµŚIVA×彚ŹōŌŖĖŲ£¬ÓÉÄÜĮæ×īµĶŌĄķ£¬æÉÖŖŌ×ÓŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ1s22s22p63s23p63d104s24p2£»
£Ø2£©Fe2£ØSO4£©3½«Sn2+Č«²æŃõ»ÆĪŖSn4+£¬Ķ¬Ź±Éś³ÉFe2+£¬øł¾ŻŌŖĖŲŹŲŗć¼°µē×ӵƏ§ŹŲŗć£¬æÉµĆ¹ŲĻµŹ½£ŗ3Sn”«3Sn2+”«6Fe3+”«6Fe2+”«K2Cr2O7£¬øł¾ŻK2Cr2O7µÄĪļÖŹµÄĮææɼĘĖć³öĪżµÄĪļÖŹµÄĮ棬ŌŁĒóµĆĪżµÄÖŹĮ棬½ų¶ų¼ĘĖćĪżµÄÖŹĮæ·ÖŹż£»
£Ø3£©Sn2+Ņ×Ė®½ā”¢Ņ×±»Ńõ»Æ£¬ĖłŅŌŹµŃéŹŅÅäÖĘSnCl2ČÜŅŗŹ±ŅŖ·ĄÖ¹ĘäĖ®½ā¼°·¢ÉśŃõ»Æ·“Ó¦£»
£Ø4£©ĻņĖįŠŌSnCl2ČÜŅŗÖŠ¼ÓČėĢ¼ĖįĒāļ§ČÜŅŗµ÷ PH=7£¬æÉŅŌÉś³ÉSnO£¬Ķ¬Ź±»¹ÓŠ¶žŃõ»ÆĢ¼ŗĶĀČ»Æļ§Éś³É£¬øł¾ŻµēŗÉŹŲŗćŗĶŌŖĖŲŹŲŗćŹéŠ“Ąė×Ó·½³ĢŹ½£»
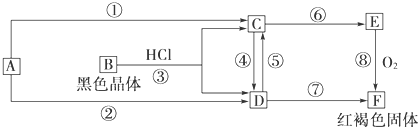
£Ø5£©SnCl4¼«Ņ×Ė®½ā£¬·“Ó¦Ó¦ŌŚĪŽĖ®»·¾³ĻĀ½ųŠŠ½ųŠŠ£¬AÖŠ·¢Éś·“Ó¦£ŗMnO2+4HCl£ØÅØ£© $\frac{\underline{\;\;”÷\;\;}}{\;}$MnCl2+Cl2”ü+2H2O£¬ÓÉÓŚŃĪĖįŅ×»Ó·¢£¬ÖʱøµÄĀČĘųÖŠŗ¬ÓŠHCl¼°Ė®ÕōĘų£¬ĖłŅŌŅŖÓƱ„ŗĶŹ³ŃĪĖ®³żČ„HCl£¬æÉŅŌ½µµĶĀČĘųµÄČܽā£¬ÅØĮņĖįĪüŹÕĖ®ÕōĘų£¬øÉŌļĀČĘų£¬ĀČĘųÓėSnŌŚBÖŠ·“Ӧɜ³ÉSnCl4£¬¾ĄäÄżŗóÓĆH×°ÖĆ½ųŠŠŹÕ¼ÆSnCl4£¬Ī“·“Ó¦µÄĀČĘų£¬ÓĆøÉŌļ¹ÜÖŠ¼īŹÆ»ŅĪüŹÕ£¬Ķ¬Ź±ÓÖæÉŅŌ·ĄÖ¹æÕĘųÖŠµÄĖ®·Ö½ųČėHÖŠŹ¹²śĪļĖ®½ā£®
½ā“š ½ā£ŗ£Ø1£©Óɽį¹¹Ź¾ŅāĶ¼æÉÖŖ£¬ĪżŹĒµŚĖÄÖÜĘŚµŚIVA×彚ŹōŌŖĖŲ£¬ÓÉÄÜĮæ×īµĶŌĄķ£¬æÉÖŖŌ×ÓŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ1s22s22p63s23p63d104s24p2£¬²¹³äĶźÕūµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ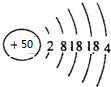 £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø2£©Fe2£ØSO4£©3½«Sn2+Č«²æŃõ»ÆĪŖSn4+£¬Ķ¬Ź±Éś³ÉFe2+£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ2Fe3++Sn2+=2Fe2++Sn4+£¬øł¾ŻŌŖĖŲŹŲŗć¼°µē×ӵƏ§ŹŲŗć£¬æÉµĆ¹ŲĻµŹ½£ŗ3Sn”«3Sn2+”«6Fe3+”«6Fe2+”«K2Cr2O7£¬K2Cr2O7µÄĪļÖŹµÄĮæĪŖ0.2000mol•L-1”Į0.025L=0.005mol£¬ÓɹŲĻµŹ½æÉÖŖ£¬ĪżµÄĪļÖŹµÄĮæĪŖ0.005mol”Į3=0.015mol£¬ŌņĪżµÄÖŹĮæ·ÖŹżĪŖ$\frac{0.015mol”Į119g/mol}{2.38g}$”Į100%=75%£¬
¹Ź“š°øĪŖ£ŗ2Fe3++Sn2+=2Fe2++Sn4+£»75%£»
£Ø3£©Sn2+Ņ×Ė®½ā”¢Ņ×±»Ńõ»Æ£¬ĖłŅŌŹµŃéŹŅÅäÖĘSnCl2ČÜŅŗŹ±ŅŖ·ĄÖ¹ĘäĖ®½ā¼°·¢ÉśŃõ»Æ·“Ó¦£¬ŅŖĻČ½«SnCl2¹ĢĢåČÜÓŚÉŁĮæÅØŃĪĖįÖŠ£¬²¢ŌŚŠĀÅäÖʵÄSnCl2ČÜŅŗÖŠ¼ÓČėÉŁĮæĪż·Ū£¬
¹Ź“š°øĪŖ£ŗČÜÓŚ½ĻÅØŃĪĖį£»Īż·Ū£»·ĄÖ¹ĘäĖ®½ā¼°·¢ÉśŃõ»Æ·“Ó¦£»
£Ø4£©ĻņĖįŠŌSnCl2ČÜŅŗÖŠ¼ÓČėĢ¼ĖįĒāļ§ČÜŅŗµ÷ PH=7£¬æÉŅŌÉś³ÉSnO£¬Ķ¬Ź±»¹ÓŠ¶žŃõ»ÆĢ¼ŗĶĀČ»Æļ§Éś³É£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖSn2++2HCO3-=SnO”ż+2CO2”ü+H2O£¬
¹Ź“š°øĪŖ£ŗSn2++2HCO3-=SnO”ż+2CO2”ü+H2O£»
£Ø5£©SnCl4¼«Ņ×Ė®½ā£¬·“Ó¦Ó¦ŌŚĪŽĖ®»·¾³ĻĀ½ųŠŠ½ųŠŠ£¬AÖŠ·¢Éś·“Ó¦£ŗMnO2+4HCl£ØÅØ£© $\frac{\underline{\;\;”÷\;\;}}{\;}$MnCl2+Cl2”ü+2H2O£¬ÓÉÓŚŃĪĖįŅ×»Ó·¢£¬ÖʱøµÄĀČĘųÖŠŗ¬ÓŠHCl¼°Ė®ÕōĘų£¬ĖłŅŌŅŖÓƱ„ŗĶŹ³ŃĪĖ®³żČ„HCl£¬æÉŅŌ½µµĶĀČĘųµÄČܽā£¬ÅØĮņĖįĪüŹÕĖ®ÕōĘų£¬øÉŌļĀČĘų£¬ĀČĘųÓėSnŌŚBÖŠ·“Ӧɜ³ÉSnCl4£¬¾ĄäÄżŗóÓĆH×°ÖĆ½ųŠŠŹÕ¼ÆSnCl4£¬Ī“·“Ó¦µÄĀČĘų£¬ÓĆøÉŌļ¹ÜÖŠ¼īŹÆ»ŅĪüŹÕ£¬Ķ¬Ź±ÓÖæÉŅŌ·ĄÖ¹æÕĘųÖŠµÄĖ®·Ö½ųČėHÖŠŹ¹²śĪļĖ®½ā£¬
¢Łøł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬ŅĒĘ÷×°ÖĆ¼°ŗĻĄķµÄĻČŗóÅÅĮŠĖ³ŠņŹĒA”śC”śE”śB”śG”śD”śH”śF£¬
¹Ź“š°øĪŖ£ŗC”śE”śB”śG”śD”śH”śF£»
¢ŚÓÉÓŚĪżÓėĀČĘųµÄ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬ĖłŅŌµ±æŖŹ¼Éś³ÉSnCl4Ź±¼“æÉĻØĆšB“¦¾Ę¾«µĘ£¬·“Ó¦ČŌæɳ֊ų½ųŠŠ£¬
¹Ź“š°øĪŖ£ŗĪżÓėĀČĘųµÄ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬·Å³öµÄČČĮæĪ¬³Ö·“Ó¦¼ĢŠų½ųŠŠ£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹÖʱø·½°ø”¢»Æѧ¹¤ŅÕĮ÷³Ģ”¢ĪļÖŹŗ¬Įæ²ā¶Ø”¢Ō×Ó½į¹¹µČÖŖŹ¶£¬ŹĒ¶Ōѧɜ×ŪŗĻÄÜĮ¦µÄ漲飬ŠčŅŖѧɜ¾ß±øŌśŹµµÄ»ł“”£¬ÄѶČÖŠµČ£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 5£ŗ3£ŗ2 | B£® | 3£ŗ2£ŗ2 | C£® | 5£ŗ4£ŗ1 | D£® | 3£ŗ2£ŗ1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
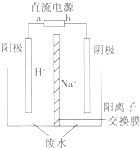 ĪŖ“¦ĄķĀČ¼×ĶéÉś²śĘóŅµµÄø±²śĪļCCl4£¬ŅŌ¼õÉŁĘä¶Ō³ōŃõ²ćµÄĘĘ»µ£®»Æѧ¼ŅŃŠ¾æŌŚ“ß»ÆĢõ¼žĻĀ£¬Ķعż·“Ó¦CCl4+H2?CHCl3+HCl”÷H£¼O£¬Ź¹CCl4×Ŗ»ÆĪŖÖŲŅŖµÄ»Æ¹¤ŌĮĻĀČ·Ā£ØCHCl3£©£®ŅŃÖŖCCl4µÄ·ŠµćĪŖ77”ę£¬CHCl3µÄ·ŠµćĪŖ61.2”ę£®ŌŚĆܱÕČŻĘ÷ÖŠ£¬øĆ·“Ó¦“ļµ½Ę½ŗāŗ󣬲āµĆČēĻĀŹż¾Ż£®
ĪŖ“¦ĄķĀČ¼×ĶéÉś²śĘóŅµµÄø±²śĪļCCl4£¬ŅŌ¼õÉŁĘä¶Ō³ōŃõ²ćµÄĘĘ»µ£®»Æѧ¼ŅŃŠ¾æŌŚ“ß»ÆĢõ¼žĻĀ£¬Ķعż·“Ó¦CCl4+H2?CHCl3+HCl”÷H£¼O£¬Ź¹CCl4×Ŗ»ÆĪŖÖŲŅŖµÄ»Æ¹¤ŌĮĻĀČ·Ā£ØCHCl3£©£®ŅŃÖŖCCl4µÄ·ŠµćĪŖ77”ę£¬CHCl3µÄ·ŠµćĪŖ61.2”ę£®ŌŚĆܱÕČŻĘ÷ÖŠ£¬øĆ·“Ó¦“ļµ½Ę½ŗāŗ󣬲āµĆČēĻĀŹż¾Ż£®| ŹµŃéŠņŗÅ | ĪĀ¶Č”ę | ³õŹ¼CCl4ÅØ¶Č£Ømol•L-1£© | ³õŹ¼H2ÅØ¶Č£Ømol•L-1£© | CCl4µÄ×Ŗ»ÆĀŹ |
| 1 | 110 | 1 | 1 | 50% |
| 2 | 100 | 1 | 1 | x |
| 3 | 110 | 0.8 | y | 60% |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū¢Ü | B£® | ¢Ū¢Ü | C£® | ¢Ś¢Ū¢Ü | D£® | ¢Ś¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1mol Cl2Óė×ćĮæµÄNaOHČÜŅŗ·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ2NA | |
| B£® | 0.1molZnÓėŗ¬0.1molHClµÄŃĪĖį³ä·Ö·“Ó¦£¬×ŖŅʵĵē×ÓŹżÄæĪŖ0.2NA | |
| C£® | 1molNaÓė×ćĮæO2·“Ó¦£¬Éś³ÉNa2OŗĶNa2O2µÄ»ģŗĻĪļ£¬×ŖŅʵĵē×ÓŹżĪŖNA | |
| D£® | ĻņFeI2ČÜŅŗÖŠĶØČėŹŹĮæCl2£¬µ±ÓŠ1molFe2+±»Ńõ»ÆŹ±£¬¹²×ŖŅʵĵē×ӵďżÄæĪŖNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
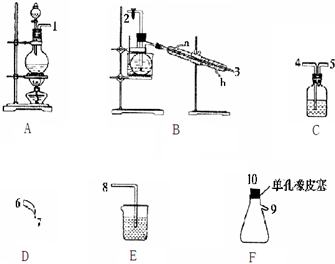
| ĪļĄķŠŌÖŹ | ÖʱøŌĄķ | »ÆѧŠŌÖŹ |
| »ĘÉ«ÓĶדŅŗĢå ČŪµćĪŖ-40”ę£¬·ŠµćĪŖ71”ę ²»ČÜÓŚĄäĖ®£¬Ņ×ČÜÓŚÓŠ»śČܼĮ ĆܶČĪŖ1.65g/mL | Cl2ÓėNH4ClĖ®ČÜŅŗŌŚµĶĪĀĻĀ·“Ó¦ | 95”걬ÕØ£¬ČČĖ®ÖŠ·¢ÉśĖ®½ā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČĘųČÜÓŚĖ®£ŗCl2+H2OØT2H++Cl-+ClO- | |
| B£® | ĻņNa2SiO3ČÜŅŗÖŠĶØČėÉŁĮæCO2£ŗSiO32-+CO2+H2OØTH2SiO3”ż+CO32- | |
| C£® | ĀĮ·ŪĶ¶ČėNaOHČÜŅŗÖŠ£ŗ2Al+2OH-ØT2AlO2-+H2”ü | |
| D£® | AlCl3ČÜŅŗÖŠ¼ÓČė×ćĮæ°±Ė®£ŗAl3++3OH-ØTAl£ØOH£©3”ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČ»ÆÄĘČܽā¶Č¼õŠ” | B£® | ČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹż±äŠ” | ||
| C£® | ČܼĮµÄÖŹĮæ¼õŠ” | D£® | ČÜŅŗ±ä³É²»±„ŗĶČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com