
同温同压下,气体的密度之比等于相对分子质量之比,已知空气的平均相对分子质量为29,同温同压下,下列气体的密度比空气密度小的是
A.二氧化氮 B.二氧化碳 C.二氧化硫 D.一氧化碳
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源:2014-2015广东省高二上学期期中联考化学(理)试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.实验室用大理石与醋酸反应制取二氧化碳:CaCO3+2H+=Ca2++CO2↑+H2O
B.氯乙酸与氢氧化钠溶液共热:CH2ClCOOH+OH- →CH2ClCOO-+H2O
C.苯与浓硫酸、浓硝酸的混合液共热制硝基苯:
D.用银氨溶液检验乙醛中的醛基:CH3CHO +2[Ag(NH3)2]++2OH- CH3COO-+NH4+ +3NH3+2Ag↓+ H2O
CH3COO-+NH4+ +3NH3+2Ag↓+ H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省江南十校高三上学期期末联考理综化学试卷(解析版) 题型:填空题
(14分)X、Y、及W是短周期中的四种元素,其原子序数依次增大。相关信息如下表
元素 | 相关信息 |
X | 具有多种同素异形体,形成的化合物种类繁多 |
Y | 短周期主族元素中原子半径最大 |
Z | 位于元素周期表金属与非金属元素的分界线上,最高化合价为十4 |
W | 富集在海水中的元素,它的某些化合物常用作消毒刹 |
(1)Z元素基态原子的核外电子排布式为 ,其未成对的电子数目为 。
(2)Y位于元素周期表中第 周期,第 族,四种元素的电负性由大到水的顺序是 (写元素符号)。
(3)氢化物中X-H和W-H的化学键极性较强的是 ,耐磨材料(XY)和单质y 熔点较高的
是 (均用元素符号表示)。
(4)已知400 ℃时,HW 可被氧气催化氧化生成W 的单质,从而实现化更生产上W的循环利用。若断开1mo1H一W化学键,该反应放热28.9KJ,试写出相应的热化学方程式: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高三上学期期末考试化学试卷(解析版) 题型:选择题
向物质M的溶液中逐滴加入NaOH溶液,先产生白色沉淀,然后沉淀逐渐溶解,则物质M可能是
A.MgSO4 B.NaAlO2 C.AlCl3 D.FeCl3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高三上学期期末考试化学试卷(解析版) 题型:选择题
俗话说“雷雨发庄稼”这是因为雷雨天空气中的某些物质之间发生了一系列化学反应,最终产生了氮肥。下列不属于其中的反应的是
A.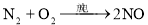
B.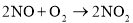
C.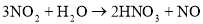
D.
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高三上学期期末考试化学试卷(解析版) 题型:选择题
加碘食盐中的”碘”应理解为
A.碘单质 B.碘原子 C.碘离子 D.碘元素
查看答案和解析>>
科目:高中化学 来源:2015年湖北省荆门市高三元月调考理综化学试卷(解析版) 题型:选择题
工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g) Si(s)+4HCl(g) △H= Q kJ/mol (Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是
Si(s)+4HCl(g) △H= Q kJ/mol (Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol, 则达平衡时,吸收热量为Q kJ
C.反应至4 min时,若HCl浓度为0.12 mol/L,则H2的反应速率为0.03 mol/(L·min)
D.当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol/L的NaOH溶液恰好反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市七校高三上学期期末联考理综化学试卷 (解析版) 题型:选择题
有关实验的叙述,正确的是
A.将浓硫酸加入容量瓶中溶解并稀释至刻度,配制成一定物质的量浓度的硫酸溶液
B.用玻璃棒蘸取溶液,点在湿润的pH试纸上测定溶液的pH值
C.用 溶液洗涤并灼烧铂丝后,再进行焰色反应
溶液洗涤并灼烧铂丝后,再进行焰色反应
D.读取量筒内液体的体积,俯视读数导致读数偏大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省杭州地区7校高三上学期期末模拟联考化学试卷(解析版) 题型:填空题
(7分)NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,
用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:
(1)相同条件下,相等物质的量浓度的NH4Al(SO4)2中c(NH4+) (填“=”、“>”“<”)NH4HSO4中c(NH4+)。
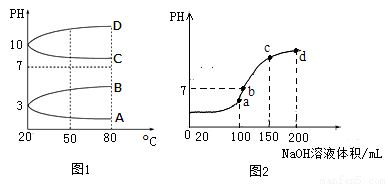
(2)如图1是0.1mol?L﹣1电解质溶液的pH随温度变化的图象。
①其中符合0.1mol?L﹣1 NH4Al(SO4)2的pH随温度变化的曲线是 (填写字母);
②室温时,0.1mol?L﹣1 NH4Al(SO4)2中2c(SO42﹣)﹣c(NH4+)﹣3c(Al3+)= mol?L﹣1(填数值)
(3)室温时,向100mL 0.1mol?L﹣1 NH4HSO4溶液中滴加0.1mol?L﹣1 NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是 ;在b点,溶液中各离子浓度由大到小的排列顺序是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com