
(12·Ц)ОӘСйЦӨСх»ҜРФЈәCl2>Fe3+>SO2Ј¬ДіРЎЧйУГПВНјЛщКҫЧ°ЦГҪшРРКөСй(јРіЦТЗЖчәНAЦРөДјУИИЧ°ЦГТСВФЈ¬ЖшГЬРФТСҫӯјмСйНкұП)КөСй№эіМИзПВЈә
ўсЈ®ҙтҝӘөҜ»ЙјРK1Ў«K4Ј¬НЁИлТ»¶ОКұјдN2Ј¬ФЩҪ«TРНөј№ЬІеИлBЦРЈ¬јМРшНЁИлN2Ј¬И»әу№ШұХK1ЎўK3ЎўK4Ј®
ўтЈ®ҙтҝӘ»оИыaЈ¬өОјУТ»¶ЁБҝөДЕЁСОЛбЈ¬ёшAјУИИЈ®
ўуЈ®өұBЦРөДИЬТәұд»ЖКұЈ¬НЈЦ№јУИИЈ¬јРҪфөҜ»ЙјРK2Ј®
ўфЈ®ҙтҝӘ»оИыbЈ¬К№Фј2mlөДИЬТәБчИлDКФ№ЬЦРЈ¬јмСйЖдЦРөДАлЧУЈ®
VЈ®ҙтҝӘөҜ»ЙјРK3Ўў»оИыcЈ¬јУИл70ЈҘөДБтЛбЈ¬Т»¶ОКұјдәујРҪфөҜ»ЙјРK3Ј®
ўцЈ®ёьРВКФ№ЬDЈ¬ЦШёҙ№эіМўфЈ¬јмСйBИЬТәЦРөДАлЧУЈ®
ЈЁ1Ј©№эіМўсөДДҝөДКЗ______________________ЎЈ
ЈЁ2Ј©ГЮ»ЁЦРҪюИуөДИЬТәОӘ__________________ЎЈ
ЈЁ3Ј©AЦР·ўЙъ·ҙУҰөД»ҜС§·ҪіМКҪОӘ__________________________________ЎЈ
ЈЁ4Ј©УГ70ЈҘөДБтЛбЦЖИЎSO2Ј¬·ҙУҰЛЩВКұИУГ98ЈҘөДБтЛбҝмЈ¬ФӯТтКЗ______________
ЈЁ5Ј©№эіМўцЦРјмСйBИЬТәЦРКЗ·сә¬УРБтЛбёщөДІЩЧчКЗ________________________________
ЈЁ6Ј©јЧЎўТТЎўұыИэО»Н¬С§·ЦұрНкіЙБЛЙПКцКөСйЈ¬ЛыГЗөДјмІвҪб№ыТ»¶ЁДЬ№»ЦӨГчСх»ҜРФCl2>Fe3+>SO2өДКЗ
| | №эіМIV BИЬТәЦРә¬УРөДАлЧУ | №эіМVI BИЬТәЦРә¬УРөДАлЧУ |
| јЧ | УРFe3+ОЮFe2+ | УРSO42©Ғ |
| ТТ | јИУРFe3+УЦУРFe2+ | УРSO42©Ғ |
| ұы | УРFe3+ОЮFe2+ | УРFe2+ |
 ГҝИХ10·ЦЦУҝЪЛгРДЛгЛЩЛгМмМмБ·ПөБРҙр°ё
ГҝИХ10·ЦЦУҝЪЛгРДЛгЛЩЛгМмМмБ·ПөБРҙр°ё
| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәМоҝХМв
ИзПВНјКЗіЈјыТЗЖчөДІҝ·ЦҪб№№ЎЈ
(1)РҙіцТЗЖчГыіЖAЎЎЎЎЎЎЎЎ,BЎЎЎЎЎЎЎЎ,CЎЎЎЎЎЎ,DЎЎЎЎЎЎЎЎЎЈ
(2)К№УГЗ°РијмІйКЗ·сВ©Л®өДТЗЖчУРЎЎЎЎЎЎЎЎЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәМоҝХМв
АыУГБтЛбФьЈЁЦчТӘә¬Fe2O3ЎўSiO2ЎўAl2O3ЎўMgOөИФУЦКЈ©ЦЖұёСх»ҜМъөД№ӨТХБчіМИзПВЈә
ЈЁ1Ј©Ў°ЛбҪюЎұЦРБтЛбТӘККөұ№эБҝЈ¬ДҝөДКЗўЩМбёЯМъөДҪюіцВКЈ¬ўЪ ЎЈ
ЈЁ2Ј©Ў°»№ФӯЎұКЗҪ«Fe3Ј«ЧӘ»ҜОӘFe2Ј«Ј¬Н¬КұFeS2ұ»Сх»ҜОӘSO42ЈӯЈ¬ёГ·ҙУҰөДАлЧУ·ҪіМКҪОӘ ЎЈ
ЈЁ3Ј©ОӘІв¶ЁЎ°ЛбҪюЎұІҪЦиәуИЬТәЦРFe3Ј«өДБҝТФҝШЦЖјУИлFeS2өДБҝЎЈКөСйІҪЦиОӘЈәЧјИ·БҝИЎТ»¶ЁМе»эөДЛбҪюәуөДИЬТәУЪЧ¶РОЖҝЦРЈ¬јУИлHClЎўЙФ№эБҝSnCl2Ј¬ФЩјУHgCl2іэИҘ№эБҝөДSnCl2Ј¬ТФ¶юұҪ°·»ЗЛбДЖОӘЦёКҫјБЈ¬УГK2Cr2O7ұкЧјИЬТәөО¶ЁЈ¬УР№Ш·ҙУҰ·ҪіМКҪИзПВЈә
2Fe3Ј«Ј«Sn2Ј«Ј«6ClЈӯЈҪ2Fe2Ј«Ј«SnCl62ЈӯЈ¬
Sn2Ј«Ј«4ClЈӯЈ«2HgCl2ЈҪSnCl62ЈӯЈ«Hg2Cl2ЎэЈ¬
6Fe2Ј«Ј«Cr2O72ЈӯЈ«14HЈ«ЈҪ6Fe3Ј«Ј«2Cr3Ј«Ј«7H2OЎЈ
ўЩИфSnCl2І»ЧгБҝЈ¬ФтІв¶ЁөДFe3Ј«Бҝ ЈЁМоЎ°Ж«ёЯЎұЎўЎ°Ж«өНЎұЎўЎ°І»ұдЎұЈ¬ПВН¬Ј©Ј¬
ўЪИфІ»јУHgCl2Ј¬ФтІв¶ЁөДFe3Ј«Бҝ ЎЈ
ЈЁ4Ј©ўЩҝЙСЎУГ ЈЁМоКФјБЈ©јмСйВЛТәЦРә¬УРFe3+ЎЈІъЙъFe3+өДФӯТтКЗ ЈЁУГАлЧУ·ҙУҰ·ҪіМКҪұнКҫЈ©ЎЈ
ўЪТСЦӘІҝ·ЦСфАлЧУТФЗвСх»ҜОпРОКҪіБөнКұИЬТәөДpHјыПВұнЈә
| іБөнОп | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | Mn(OH)2 |
| ҝӘКјіБөн | 2.7 | 3.8 | 7.5 | 9.4 | 8.3 |
| НкИ«іБөн | 3.2 | 5.2 | 9.7 | 12.4 | 9.8 |
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәКөСйМв
БтҙъБтЛбДЖөДҙҝ¶ИҝЙУГөО¶Ё·ЁҪшРРІв¶ЁЈ¬ФӯАнКЗЈә2S2O32Јӯ+ I2 Ўъ S4O62Јӯ+ 2I-
38.ЕдЦЖ100 mL0.0500 mol/L I2ИЬТәЈ¬І»РиТӘөДТЗЖчКЗ ЈЁСЎМоұаәЕЈ©ЎЈ
aЈ®100 mLИЭБҝЖҝ bЈ®БҝНІ cЈ®ЙХұӯ dЈ®ІЈБ§°ф
өО¶Ё№ЬұкУРК№УГОВ¶ИЈә20oC; өО¶Ё№ЬөДЧоРЎҝМ¶ИОӘ mLЎЈ
39.ИЎ2 .500gә¬ФУЦКөДNa2S2O3ЎӨ5H2Oҫ§МеЕдіЙ50mLИЬТәЈ¬ГҝҙОИЎ10.00mL·ЕИлЧ¶РОЖҝАпЈ¬јУ2өОөн·ЫОӘЦёКҫјБЈ¬ФЩУГ0.0500 mol/L I2ИЬТәөО¶ЁЈ¬КөСйКэҫЭИзПВ(өЪ3ҙОіх¶БКэОӘ 0.00Ј¬ЦХөг¶БКэИзНј; ФУЦКІ»ІОјУ·ҙУҰ)Јә
| ұаәЕ | 1 | 2 | 3 |
| ПыәДI2ИЬТәөДМе»э/mL | 19.98 | 20.02 | |
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәКөСйМв
ПВБРКөСйІЩЧч¶јДЬҙпөҪФӨЖЪДҝөДөДКЗ( )
ўЩХфёЙAlCl3ИЬТәҝЙөГҙҝҫ»өДОЮЛ®ВИ»ҜВБЈ»ўЪЦҪІгОц·Ё·ЦАлМъАлЧУәННӯАлЧУКөСйЦРЈ¬өгСщәуөДВЛЦҪРиБАёЙәуЈ¬ІЕДЬҪ«ВЛЦҪПВ¶ЛҪюИлХ№ҝӘјБЦРҪшРРКөСйЈ»ўЫУГ№г·әpHКФЦҪІвөГДіИЬТәpHОӘ3.5Ј»ўЬөОИл·УМӘИЬТәИ·¶ЁҙҝјоЦРУРОЮЙХјоЈ»ўЭУГГЧМАЦұҪУјмСйКіУГСОЦРКЗ·сә¬УРөвФӘЛШЈ»ўЮУГЛбКҪөО¶Ё№ЬБҝИЎ20.00 mLёЯГМЛбјШЛбРФИЬТәЈ»ўЯУГдеөДЛДВИ»ҜМјИЬТәіэИҘ»мФЪјЧНйЦРөДТТП©ЖшМе
| AЈ®ўЮўЯ | BЈ®ўЪўЮ | CЈ®ўЭўЮўЯ | DЈ®Ц»УРўЮ |
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәКөСйМв
FeCl3ФЪПЦҙъ№ӨТөЙъІъЦРУҰУГ№г·әЎЈДі»ҜС§СРҫҝРФС§П°РЎЧйДЈДв№ӨТөБчіМЦЖұёОЮЛ®FeCl3Ј¬ФЩУГёұІъЖ·FeCl3ИЬТәОьКХУР¶ҫөДH2SЎЈ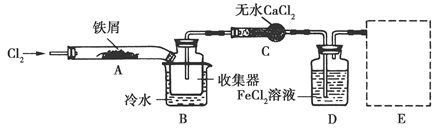
ўс.ҫӯІйФДЧКБПөГЦӘЈәОЮЛ®FeCl3ФЪҝХЖшЦРТЧіұҪвЈ¬јУИИТЧЙэ»ӘЎЈЛыГЗЙијЖБЛЦЖұёОЮЛ®FeCl3өДКөСй·Ҫ°ёЈ¬Ч°ЦГКҫТвНј(јУИИј°јРіЦЧ°ЦГВФИҘ)ј°ІЩЧчІҪЦиИзПВЈә
ўЩјмСйЧ°ЦГөДЖшГЬРФЈ»
ўЪНЁИлёЙФпөДCl2Ј¬ёПҫЎЧ°ЦГЦРөДҝХЖшЈ»
ўЫУГҫЖҫ«өЖФЪМъРјПВ·ҪјУИИЦБ·ҙУҰНкіЙЈ»
ўЬЎӯЎӯ
ўЭМеПөАдИҙәуЈ¬НЈЦ№НЁИлCl2Ј¬ІўУГёЙФпөДN2ёПҫЎCl2Ј¬Ҫ«КХјҜЖчГЬ·вЎЈ
Зл»ШҙрПВБРОКМвЈә
(1)Ч°ЦГAЦР·ҙУҰөД»ҜС§·ҪіМКҪОӘ______________ЎЈ
(2)өЪўЫІҪјУИИәуЈ¬ЙъіЙөДСМЧҙFeCl3ҙуІҝ·ЦҪшИлКХјҜЖчЈ¬ЙЩБҝіБ»эФЪ·ҙУҰ№ЬAУТ¶ЛЎЈТӘК№іБ»эөДFeCl3ҪшИлКХјҜЖчЈ¬өЪўЬІҪІЩЧчКЗ________ЎЈ
(3)ІЩЧчІҪЦиЦРЈ¬ОӘ·АЦ№FeCl3іұҪвЛщІЙИЎөДҙлК©УР(МоІҪЦиРтәЕ)________ЎЈ
(4)Ч°ЦГBЦРАдЛ®ФЎөДЧчУГОӘ________Ј»Ч°ЦГCөДГыіЖОӘ________Ј»Ч°ЦГDЦРFeCl2И«Іҝ·ҙУҰәуЈ¬ТтК§ИҘОьКХCl2өДЧчУГ¶шК§Р§Ј¬РҙіцјмСйFeCl2КЗ·сК§Р§өДКФјБЈә________ЎЈ
(5)ФЪРйПЯҝтЦР»ӯіцОІЖшОьКХЧ°ЦГEІўЧўГчКФјБЎЈ
ўт.ёГЧйН¬С§УГЧ°ЦГDЦРөДёұІъЖ·FeCl3ИЬТәОьКХH2SЈ¬өГөҪөҘЦКБтЈ»№эВЛәуЈ¬ФЩТФКҜД«ОӘөзј«Ј¬ФЪТ»¶ЁМхјюПВөзҪвВЛТәЎЈ
(6)FeCl3УлH2S·ҙУҰөДАлЧУ·ҪіМКҪОӘ________________ЎЈ
(7)өзҪвіШЦРHЈ«ФЪТхј«·ЕөзІъЙъH2Ј¬Сфј«өДөзј«·ҙУҰКҪОӘ____________________ЎЈ
(8)ЧЫәП·ЦОцКөСйўтөДБҪёц·ҙУҰЈ¬ҝЙЦӘёГКөСйУРБҪёцПФЦшУЕөгЈә
ўЩH2SөДФӯЧУАыУГВКОӘ100%Ј»ўЪ________________ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәКөСйМв
БтЛбНӯҫ§МеФЪІ»Н¬ОВ¶ИПВҝЙК§ИҘІҝ·Ц»тИ«ІҝҪбҫ§Л®ЙхЦБ·ЦҪвіЙСх»ҜОпЎЈДіС§ЙъФЪІ»Н¬ОВ¶ИПВёш8.000 gБтЛбНӯҫ§МејУИИЈЁОВ¶ИЦрҪҘЙэёЯЈ©Ј¬КөСйҪб№ыјЗВјИзПВЈә
| КөСйҙОРт | ОВ¶ИЈЁЎжЈ© | АдИҙәуКЈУа№ММеөДЦКБҝЈЁgЈ© |
| 1 | 102 | 6.848 |
| 2 | 113 | 5.696 |
| 3 | 258 | 5.120 |
| 4 | 570 | 2.560 |
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәКөСйМв
ВИ»ҜёЖіЈУГУЪөАВ·ИЪұщјБәНёЙФпјБЈ¬ҫЯУРТЧИЬУЪЛ®Ј¬ТЧОьіұөИРФЦКЎЈКөСйКТУГ№ӨТөҙуАнКҜЈЁә¬УРЙЩБҝAl2O3ЎўFe2O3өИФУЦКЈ©ЦЖұёВИ»ҜёЖөДЦчТӘБчіМИзПВЈә НкіЙПВБРМоҝХЈә
НкіЙПВБРМоҝХЈә
ЈЁ1Ј©ЙПКцК№УГөДСОЛбөДОпЦКөДБҝЕЁ¶ИФјОӘ6.0mol/LЈ¬ИфУГ36.5%өДСОЛбЈЁГЬ¶ИОӘ1.2g/mLЈ©ЕдЦГ6.0mol/LөДСОЛб100mLЈ¬ЛщРиөДІЈБ§ТЗЖчУРІЈБ§°фЎўБҝНІЎўҪәН·өО№ЬЎў Ј»РиТӘБҝИЎ36.5%өДСОЛб mLЈ»ЕдЦЖ№эіМЦРЈ¬ИфЖдЛыІЩЧч¶јХэИ·Ј¬ПВБРІЩЧч»бТэЖрЕЁ¶ИЖ«РЎөДКЗ ЎЈ
| AЈ®¶ЁИЭТЎФИәу·ўПЦТәГжөНУЪҝМ¶ИПЯ |
| BЈ®¶ЁИЭКұё©КУИЭБҝЖҝөДҝМ¶ИПЯ |
| CЈ®Ҫ«ИЬТәЧӘИлИЭБҝЖҝәуЈ¬Г»УРПҙөУЙХұӯәНІЈБ§°фЈ¬ҫНЧӘИл¶ЁИЭІЩЧч |
| DЈ®Из№ыјУЛ®і¬№эБЛҝМ¶ИПЯЈ¬ИЎіцЙЩБҝЛ®К№ТәГжЗЎәГөҪҝМ¶ИПЯ |
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәКөСйМв
БтЛбСЗМъҝЙУлөИОпЦКөДБҝөДБтЛбп§ЙъіЙБтЛбСЗМъп§ЈәЈЁNH4Ј©2SO4ЎӨFeSO4ЎӨ6H2OЈ¬ЙМЖ·ГыіЖОӘДӘ¶ыСОЈ¬КЗТ»ЦЦёҙСОЎЈТ»°гСЗМъСОФЪҝХЖшЦРТЧұ»СхЖшСх»ҜЈ¬РОіЙёҙСОәуҫНұИҪПОИ¶ЁЎЈУлЖдЛыёҙСОТ»СщЈ¬БтЛбСЗМъп§ФЪЛ®ЦРөДИЬҪв¶ИұИЧйіЙЛьөДГҝТ»ЦЦСОөДИЬҪв¶И¶јРЎЈ¬ЗТјёәхІ»ИЬУЪТТҙјЈ¬АыУГХвТ»РФЦКҝЙТФЦЖИЎБтЛбСЗМъп§ҫ§МеЎЈИэЦЦСОөДИЬҪв¶ИЈЁөҘО»ОӘg/l00gH2OЈ©јыПВұнЈә
КөСйУГЖ·Јә FeРјЈЁә¬ЙЩБҝМјЈ©Ўў3mol/LH2SO4ЎўЈЁ NH4Ј©2SO4ЎўХфБуЛ®ЎўОЮЛ®ТТҙјЎЈ
КөСйІҪЦиБчіМНјЈә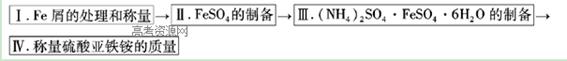
ЗлНкіЙТФПВКөСйјЗВјЈә
ЈЁ1Ј©ІҪЦиIЦРУГ10% Na2CO3өДИИИЬТәҙҰАнМъРјөДДҝөДКЗ Ј¬ҫӯҙҰАнәуөДёЙФпМъРјЦКБҝјЗОӘm1Ј»
ЈЁ2Ј©Ҫ«іЖБҝәГөДFeРј·ЕИлЧ¶РОЖҝЦРЈ¬јУИлККБҝ3mol/LH2SO4ИЬТәЈ¬·ЕФЪЛ®ФЎЦРјУИИЦБЖшЕЭБҝІъЙъҪПЙЩКұОӘЦ№ЈЁУРЗвЖшЙъіЙЈ¬УГГч»рјУИИЧўТв°ІИ«Ј©ЎЈіГИИ№эВЛЈ¬ІўУГЙЩБҝИИЛ®ПҙөУЧ¶РОЖҝј°ВЛЦҪЈ¬Ҫ«ВЛТәәНПҙөУТәТ»ЖрЧӘТЖЦБХф·ўГуЦРЎЈҪ«ВЛЦҪЙПөД№ММеіЈОВёЙФпәуіЖЦШЈ¬јЗОӘm2Ј»
ЈЁ3Ј©іЖИЎТ»¶ЁЦКБҝөДЈЁNH4Ј©2SO4Ј¬јУИл______ gЈЁУГә¬m1әНm2өДҙъКэКҪұнКҫЈ¬ТӘЗу»ҜјтЈ¬ПВН¬ЎЈЈ©Л®ЕдЦЖіЙКТОВПВЈЁ20ЎжЈ©өДұҘәНИЬТәЈ¬ІўҪ«ЖдјУИлөҪЙПГжКөСйөДХф·ўГуЦРЈ¬»ә»әјУИИЈ¬ЕЁЛхЦБұнГжіцПЦҪбҫ§ұЎДӨОӘЦ№ЎЈ·ЕЦГАдИҙЈ¬өГөҪБтЛбСЗМъп§өДҫ§МеЈ¬№эВЛәуУГ____________ПҙөУҫ§МеЎЈ
ЈЁ4Ј©ІъЖ·ҙҝ¶ИөДІв¶Ё
ПИіЖИЎІъЖ·1.600gЈ¬јУЛ®ИЬҪвЈ¬ЕдіЙ100mlИЬТәЈ¬ТЖИЎ25.00mLҙэІвИЬТәУлЧ¶РОЖҝЦРЈ¬ФЩУГБтЛбЛб»ҜөД0.0100mol/LKMnO4ұкЧјИЬТәҪшРРөО¶ЁЖдЦРөДFe2+Ј¬ҙпөҪөО¶ЁЦХөгКұПыәДұкЧјТәөДЖҪҫщЦөОӘ20.00mLЈ¬ФтСщЖ·ЦРөДЈЁNH4Ј©2SO4ЎӨFeSO4ЎӨ6H2OөДЦКБҝ·ЦКэЈҝЈЁБРКҪјЖЛгЈ©
Ійҝҙҙр°ёәНҪвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com