
| A. | ①②③ | B. | ①②③⑤ | C. | ③⑤ | D. | 除⑥外 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | 酸碱盐都是电解质 | |
| B. | 弱碱分解均生成对应的氧化物和水 | |
| C. | 酸酐不 一定是氧化物 | |
| D. | 电解原理精炼铜的过程中两电极质量变化相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
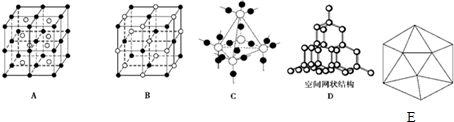
| 金刚石 | 晶体硅 | 晶体硼 | |
| 熔点/K | >3 823 | 1 683 | 2 573 |
| 沸点/K | 5 100 | 2 628 | 2 823 |
| 硬度/Moh | 10 | 7.0 | 9.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
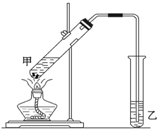 在实验室里用乙醇、冰醋酸和浓硫酸来制备一种有香味的物质,实验装置如图所示,请根据要求作答.
在实验室里用乙醇、冰醋酸和浓硫酸来制备一种有香味的物质,实验装置如图所示,请根据要求作答.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| B. | Fe3O4 与稀硝酸反应:Fe3O4+8H+=2Fe3++Fe2++4H2O | |
| C. | 碳酸氢铵溶液与足量烧碱溶液共热:NH${\;}_{4}^{+}$+OH$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 将过量氨水中加入氯化铁溶液中:Fe3++3NH3•H2O═Fe(OH)3↓+3NH${\;}_{4}^{+}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com