
【题目】下列说法不正确的是( )
A.常温下,在0.1molL﹣1的HNO3溶液中,由水电离出的c(H+)< ![]()
B.浓度为0.1molL﹣1的NaHCO3溶液:c(H2CO3)>c(CO32﹣)
C.25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同
D.冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小
【答案】D
【解析】解:A.酸、碱或强酸酸式盐抑制水电离,硝酸是强酸,抑制水电离,所以水电离出的c(H+)< ![]() ,故A正确;B.碳酸氢钠溶液呈碱性,因为碳酸氢根离子水解程度大于电离程度,所以c(H2CO3)>c(CO32﹣),故B正确;
,故A正确;B.碳酸氢钠溶液呈碱性,因为碳酸氢根离子水解程度大于电离程度,所以c(H2CO3)>c(CO32﹣),故B正确;
C.溶度积常数只与温度有关,温度不变,溶度积常数不变,与溶液浓度无关,故C正确;
D.冰醋酸中逐滴加入水,促进醋酸电离,醋酸电离程度增大,随着水的加入,溶液中氢离子浓度先增大后减小,所以溶液导电能力先增大后减小,溶液的pH先减小后增大,故D错误;
故选D.
A.酸、碱或强酸酸式盐抑制水电离;
B.碳酸氢钠溶液呈碱性,因为碳酸氢根离子水解程度大于电离程度;
C.溶度积常数只与温度有关,温度不变,溶度积常数不变;
D.冰醋酸中逐滴加入水,促进醋酸电离,醋酸电离程度增大,溶液导电性与离子浓度成正比,溶液中氢离子浓度越大pH越小.


科目:高中化学 来源: 题型:
【题目】X、Y、Z是周期表中相邻的三种短周期元素,X和Y同周期,Y和Z同主族,三种元素原子的最外层电子数之和为17,核内质子数之和为31,则X、Y、Z是 ( )
A. Mg Al Si B. Li Be Mg C. N O S D. P S O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制取自来水的装置示意图,根据图示回答下列问题。

(1)图中的两处明显的错误是____________________、_____________________。
(2)A仪器的名称是______________,B仪器的名称是_______________。
(3)实验时A中除加入少量自来水外,还需加入少量___________,其作用是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲池的总反应式为:N2H4+O2═N2+2H2O下列关于该电池工作时说法正确的是( ) 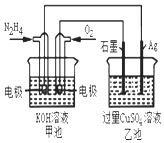
A.甲池中负极反应为:N2H4﹣4e﹣═N2+4H+
B.甲池溶液pH不变,乙池溶液pH减小
C.反应一段时间后,向乙池中加一定量CuO固体,能使CuSO4溶液恢复到原浓度
D.甲池中消耗2.24L O2 , 此时乙池中理论上最多产生12.8g固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100mL的混合液中,硝酸和硫酸的物质的量浓度分别是0.3molL﹣1、0.15molL﹣1 , 向该混合液中加入2.56g铜粉,加热,待充分反应后,所得溶液中铜离子的物质的量浓度是( )
A.0.15 molL﹣1
B.0.225 molL﹣1
C.0.30 molL﹣1
D.0.45 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷与氧可发生如下反应:P4+5O2═P4O10 . 已知断裂下列化学键需要吸收的能量分别为:P﹣P:a kJmol﹣1、P﹣O:b kJmol﹣1、P=O:c kJmol﹣1、O=O:d kJmol﹣1 . 根据图示的分子结构和有关数据估算该反应的△H,其中正确的是( ) 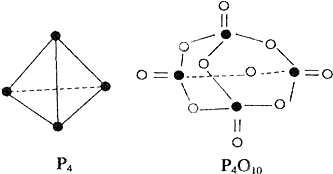
A.(6a+5d﹣4c﹣12b)kJmol﹣1
B.(4c+12b﹣6a﹣5d)kJmol﹣1
C.(4c+12b﹣4a﹣5d)kJmol﹣1
D.(4a+5d﹣4c﹣12b)kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X,Y,Z,W均为短周期元素,它们在元素周期表中的位置如下图所示.若Y原子的最外层电子数是次外层电子数的2倍,下列说法中正确的是( ) ![]()
A.氢化物稳定性:X>Y
B.最高价氧化物对应的水化物的酸性:W>Y
C.4种元素的单质中,W单质的熔、沸点最高
D.干燥的W单质具有漂白性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com