
【题目】在2 L密闭容器内,加入0.100 molCO气体和0.080 molCuO固体,800℃时发生如下反应:2CuO(s)+CO(g)![]() Cu2O(s)+CO2(g),n(CuO)随时间的变化如表:
Cu2O(s)+CO2(g),n(CuO)随时间的变化如表:
时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
n(CuO)(mol) | 0.080 | 0.060 | 0.040 | 0.020 | 0.020 | 0.020 |
(1)用CO表示前2min内的化学反应速率=________。
(2)计算此反应在800C时的化学平衡常数k=______________。若向平衡后的体系中加入CO和CO2各0.05mol,则此时v(正)_______v (逆) 。
(3)用来还原CuO的CO可以用C和水蒸气反应制得。
已知:C(s)+O2(g)![]() CO2(g) H =-393.5 kJ/mol,2CO(g)+ O2(g)
CO2(g) H =-393.5 kJ/mol,2CO(g)+ O2(g)![]() 2CO2(g) H=-566 kJ/mol,2H2(g)+ O2(g)
2CO2(g) H=-566 kJ/mol,2H2(g)+ O2(g)![]() 2H2O(g) H =-571.6 kJ/mol,则C(s)+H2O(g)
2H2O(g) H =-571.6 kJ/mol,则C(s)+H2O(g)![]() CO(g)+H2(g) H = __________。此反应的化学平衡表达式为:_______________________。
CO(g)+H2(g) H = __________。此反应的化学平衡表达式为:_______________________。
【答案】0.005mol/(Lmin)0.429小于+175.3kJ/molK=c(H2)c(CO)/c(H2O)
【解析】
本题考查了化学反应速率和化学平衡的计算、盖斯定律的相关知识。(1)根据前2min内,氧化铜的变化量求出一氧化碳的变化量,再根据公式V= ![]() 进行一氧化碳反应速率的计算。
进行一氧化碳反应速率的计算。
(2)①根据平衡时,氧化铜的变化量,求出各量的变化量,然后根据化学平衡常数K=c(CO2)/c(CO)进行计算;②温度不变,根据QC与K关系,判定反应进行的方向,从而判定v(正)与v (逆)的关系。
(3)根据盖斯定律进行计算。
(1)前2min内,反应的氧化铜为0.04mol,则反应的一氧化碳为0.02 mol, v(CO)=0.02/(2×2)=0.005mol/(Lmin);正确答案:0.005mol/(Lmin)。
(2)①平衡时,反应的氧化铜为0.06mol,则反应的一氧化碳为0.03 mol,在800C时的化学平衡常数K=c(CO2)/c(CO)=[0.03/2]/[(0.10-0.03)/2]=0.429;②若向平衡后的体系中加入CO和CO2各0.05mol,QC=[0.08/2]/[(0.1-0.03+0.05)/2]=0.667>K,平衡逆向移动,则此时v(正)小于v (逆) ;正确答案:0.429;小于。
(3)①C(s)+O2(g)![]() CO2(g) H =-393.5 kJ/mol,②2CO(g)+ O2(g)
CO2(g) H =-393.5 kJ/mol,②2CO(g)+ O2(g)![]() 2CO2(g) H=-566 kJ/mol,③2H2(g)+ O2(g)
2CO2(g) H=-566 kJ/mol,③2H2(g)+ O2(g)![]() 2H2O(g) H =-571.6 kJ/mol;根据盖斯定律可知:将①- (②+③),得C(s)+H2O(g)
2H2O(g) H =-571.6 kJ/mol;根据盖斯定律可知:将①- (②+③),得C(s)+H2O(g)![]() CO(g)+H2(g) H = (-393.5kJ/mol)-1/2[(-566kJ/mol)+( -571.6kJ/mol)]=+175.3kJ/mol;此反应的化学平衡表达式为:K=c(H2)×c(CO)/c(H2O);正确答案:+175.3kJ/mol;K=c(H2)×c(CO)/c(H2O)。
CO(g)+H2(g) H = (-393.5kJ/mol)-1/2[(-566kJ/mol)+( -571.6kJ/mol)]=+175.3kJ/mol;此反应的化学平衡表达式为:K=c(H2)×c(CO)/c(H2O);正确答案:+175.3kJ/mol;K=c(H2)×c(CO)/c(H2O)。


科目:高中化学 来源: 题型:
【题目】【化学—选修:物质结构与性质】
金属钛(22Ti)号称航空材料。回答下列问题:
(1)钛元素基态原子未成对电子数为________个,能量最高的电子占据的能级符号为___________,该能级所在能层具有的原子轨道数为_____________。
(2)[Ti(OH)2(H2O)4]2+中的化学键有_____________。
a.σ键 b.π键 c.离子键 d.配位键
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图所示。

化合物甲的分子中采取sp2杂化方式的碳原子个数为__________,化合物乙中采取sp3杂化的原子的第一电离能由小到大的顺序为____________。
(4)工业上制金属钛采用金属还原四氯化钛。先将TiO2(或天然的金红石)和足量炭粉混合加热至1000~1100K,进行氯化处理,生成TiCl4.写出生成TiCl4的化学反应方程式:_______________。
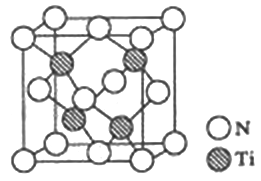
(5)有一种氮化钛晶体的晶胞如图所示,该晶体的化学式为____________,该晶体中Ti原子周围与距离最近且相等的 N原子的个数为___________。已知晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,则晶胞边长为________cm(用含ρ、NA的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】你认为减少酸雨产生可采用的措施是( )
①少用煤作燃料 ②把工厂烟囱加高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A.①②③B.②③④⑤
C.①③⑤D.①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硬脂酸甘油酯在碱性条件下水解的装置如图所示。进行皂化反应时的步骤如下:
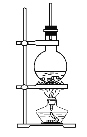
(1)在圆底烧瓶中装入7~8 g硬脂酸甘油酯,然后加入2~3 g的氢氧化钠、5 mL水、10 mL酒精。加入酒精的作用为______________________;
加入NaOH溶液的作用是___________________________。
(2)隔着石棉网给反应混合物加热约10 min,皂化反应基本完成。证明皂化反应进行完全的方法是_______________________。
(3)皂化反应完成后,加入饱和NaCl溶液的作用是____________________。
(4)图中长玻璃导管的作用为________________________。
(5)写出该反应的化学方程式:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三聚氰胺含氮量较高,但对人体有害。一些不法乳制品企业为了提高乳制品中蛋白质含量,向乳制品中添加三聚氰胺,使儿童患肾结石。下图所示的实验装置可用来测定三聚氰胺的分子式。
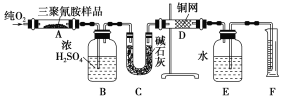
已知三聚氰胺的相对分子质量为126。取1.26 g三聚氰胺样品,放在纯氧中充分燃烧,生成CO2、H2O、N2,实验测得装置B增重0.54 g,C增重1.32 g,排入F中水的体积为672 mL(可按标准状况计算)。
(1)E装置的作用是________________________。
(2)需要加热的装置是____________(填字母)。
(3)装置D的作用是_________________________。
(4)F处读数时应该注意:_________________、__________________。
(5)三聚氰胺的分子式为___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某中学化学兴趣小组对乙醇的分子结构进行探究,其过程如下:
猜想一:乙醇的结构简式是CH3CH2OH
猜想二:乙醇的结构简式是CH3OCH3
制定方案并实施:按下图所示实验装置进行实验,
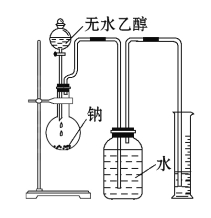
测定乙醇与钠反应(放热)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子的数目。
试回答下列问题:
(1)指出实验装置中的错误 。
(2)如果实验装置和操作正确,且结论符合猜想一,则参加反应的乙醇的物质的量与产生氢气的物质的量之比可能为 。
(3)如果实验装置和操作正确,且结论符合猜想二,则参加反应的乙醇的物质的量与产生氢气的物质的量之比可能为 。
(4)如果实验装置正确,实验结果为2.3 g乙醇与足量金属钠反应时产生了标准状况下的氢气约0.56 L,则乙醇的结构简式应为 ,理由是 。
(5)该实验获得成功的关键,除了需要纠正图中的装置错误以外,还需注意下列问题中的 (用序号填写)。
①装置的气密性良好;
②实验开始前准确测定乙醇的量;
③钠足量;
④广口瓶中水的体积大于560 mL;
⑤氢气的体积测算准确。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可利用硫酸厂废渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4·7H2O),聚铁的化学式可表示为[Fe2(OH)n(SO4)3-0.5n]m,主要工艺流程下:

下列说法不正确的是
A. 炉渣中FeS与稀硫酸和氧气反应的离子方程式为:4FeS+3O2+12H+===4Fe3++4S↓+6H2O
B. 气体M的成分是SO2,通入H2O2溶液得到硫酸,可循环使用
C. 向溶液X中加入过量铁粉,充分反应后过滤得到溶液Y,再经蒸干即得绿矾
D. 溶液Z的pH影响聚铁中铁的质量分数,若其pH偏小,将导致聚铁中铁的质量分数偏小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去空气中的二氧化硫和氨氧化物气体对环境保护有重要意义。
(1)二氧化硫易溶于水,溶于水后所得溶液中H2SO3、HSO3-和SO32- 占三种粒子总数的比例随pH的变化如下图所示。由图可知H2SO3 的电离平衡常数Ka1=____________。
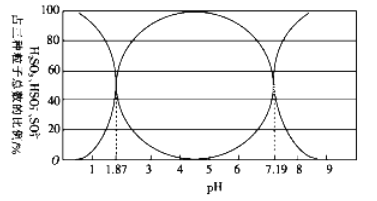
(2)利用尿素[CO(NH2)2]水解的溶液可以吸收含SO2 的空气。已知尿素水解放热,常温下水解反应较慢,水解的反应方程式如下:CO(NH2)2+H2O=H2NCOONH4(氨基甲酸铵)。
①氨基甲酸铵会与空气中的SO2 和O2 反应生成(NH4)2SO4,该反应的化学方程式为__________。
②一定条件下,用尿素溶液吸收含SO2 的空气,测得SO2 的吸收率随溶液的温度变化如图甲所示。温度高于60 ℃时,SO2 的吸收率逐渐升高的原因是_____________。

③尿素溶液吸收SO2 的吸收率随溶液的pH变化如图乙所示。尿素溶液吸收含SO2的空气后溶液的pH会降低,为提高SO2 的吸收率和充分回收产物,最好向溶液中加入_____(填溶液的名称)并控制pH 为_______。
(3)一种电化学脱硝法的原理如图所示。

①电解池阴极所发生的电极反应为_____________。
②相同条件下通入的污染气和生成的X 的体积比为40 :3,污染气中NO 和NO2 占总体积的10%,若NaClO完全反应,污染气中NO和NO2 被完全吸收且其余气体不参与反应,则NO和NO2 的体积比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积为V L的密闭容器中进行反应:aN(g)bM(g),M、N的物质的量随时间的变化曲线如下图所示:

(1)此反应的化学方程式中=___________。
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为________________________。
(3)下列叙述能说明上述反应达到平衡状态的是_________(填字母序号)。
A.反应中M与N的物质的量之比为1∶1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内每消耗a mol N,同时生成b mol M
E.混合气体的压强不随时间的变化而变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com