
分析 (1)①根据放热反应中生成物能量总和与反应物能量总和的关系;
②根据热化学方程式2H2(g)+O2(g)═2H2O(l)△H=-572kJ/mol进行计算以及液态水变成水蒸气需要吸热来判断;
③根据反应产物和反应热分析;
(2)利用盖斯定律,将热化学方程式进行运算,计算反应的焓变;
(3)根据盖斯定律,利用方程式的加减得出C3H5(ONO2)3分解成CO2、N2、H2O、O2的化学方程式,其反应热也要相应的加减,从而得出其热化学反应方程式.
解答 解:(1)①因放热反应中生成物能量总<与反应物能量总和,而2H2(g)+O2(g)═2H2O(l)△H=-572kJ/mol是放热反应,
故答案为:小于;
②据热化学方程式2H2(g)+O2(g)═2H2O(l)△H=-572kJ/mol,2mol氢气完全燃烧生成液态水放出热量572kJ,因液态水变成水蒸气需要吸热,所以2mol氢气完全燃烧生成水蒸气放出热量小于572kJ,
故答案为:<;
③与化石燃料相比,利用氢能源有很多优点,燃烧产物为水无污染,燃烧热值高;
故答案为:热值高,无污染;
(2)2SO2(g)+O2(g)=2SO3(g)△H1=一197kJ/mol ①
2H2O (g)=2H2O(1)△H2=-44kJ/mol ②
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)△H3=一545kJ/mol③
利用盖斯定律:(③-①-②)×$\frac{1}{2}$得SO3 (g)+H2O(l)=H2SO4(l)△H=-152kJ/mol,
SO3(g)+H2O(g)=H2SO4(l)△H3=-152kJ/mol,
故答案为:SO3(g)+H2O(g)=H2SO4(l)△H3=-152kJ/mol;
(3)已知:
①6C(s)+5H2(g)+3N2(g)+9O2(g)═2C3H5(ONO2)3(l)△H1
②2H2(g)+O2(g)═2H2O(g)△H2
③C(s)+O2(g)═CO2(g)△H3
由盖斯定律:5×②+12×③-2×①得:4C3H5(ONO2)3(l)═12CO2(g)+10H2O(g)+O2(g)+6N2(g)△H=12△H3+5△H2-2△H1;
故答案为:12△H3+5△H2-2△H1.
点评 本题考查了化学反应的吸放热与反应物产物能量之间的关系、热化学方程式和盖斯定律的计算等知识,准确把握盖斯定律的概念是关键,注意知识的整理和应用,难度中等.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.9 mol H2O | B. | 0.3 mol H2SO4 | C. | 0.2 mol NH3 | D. | 0.4 mol CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的碳酸钠和碳酸氢钠分别与足量盐酸反应,碳酸氢钠产生的二氧化碳多 | |
| B. | 等物质的量的盐酸分别与足量的碳酸钠和碳酸氢钠反应,碳酸氢钠产生的二氧化碳多 | |
| C. | 相同温度在水中的溶解度:碳酸钠大于碳酸氢钠 | |
| D. | 用氢氧化钙溶液鉴别碳酸钠和碳酸氢钠两种溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 营养平衡、科学使用食品添加剂有助于健康和提高免疫力.
营养平衡、科学使用食品添加剂有助于健康和提高免疫力.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
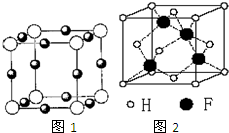 已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F.其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F.其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氧化铝坩埚可用于熔融NaOH实验 | |
| B. | 氧化铝的熔点很高,是一种较好的耐火材料 | |
| C. | 明矾可用于自来水的消毒 | |
| D. | 氢氧化铝能中和胃酸,适合于胃溃疡患者服用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com