
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如图:

回答下列问题:
(1)NaClO2中Cl的化合价为___;电解产生的Cl2是___色,实验室制备氯气的化学方程式为:____。
(2)写出“反应”步骤中生成ClO2的化学方程式:___。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为___、___。
【答案】+3价 黄绿色 MnO2+4HCl(浓)![]() MnCl2+Cl2+2H2O↑ 2NaClO3+SO2+H2SO4=2NaHSO4+2ClO2 NaOH溶液 Na2CO3溶液
MnCl2+Cl2+2H2O↑ 2NaClO3+SO2+H2SO4=2NaHSO4+2ClO2 NaOH溶液 Na2CO3溶液
【解析】
二氧化硫和氯酸钠在酸性条件下发生反应产生二氧化氯和硫酸氢钠,二氧化氯和食盐水通入电解装置中电解,得到亚氯酸钠和氯气,尾气中的二氧化氯被氢氧化钠和过氧化氢的混合溶液吸收转变成亚氯酸钠,成品液经过结晶、干燥得到亚氯酸钠固体,据此分析解答。
(1) NaClO2中Na为+1价,O为-2价,根据化合价代数和为0,则Cl的化合价为+3价;氯气为黄绿色气体,实验室通过二氧化锰与浓盐酸加热制备氯气,反应方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2+2H2O↑,
MnCl2+Cl2+2H2O↑,
故答案为:+3;黄绿色;MnO2+4HCl(浓)![]() MnCl2+Cl2+2H2O↑;
MnCl2+Cl2+2H2O↑;
(2) 二氧化硫和氯酸钠在酸性条件下发生反应产生二氧化氯和硫酸氢钠,反应方程式为:2NaClO3+SO2+H2SO4=2NaHSO4+2ClO2,
故答案为:2NaClO3+SO2+H2SO4=2NaHSO4+2ClO2;
(3) “电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,需将镁离子转变成氢氧化镁,钙离子转变成碳酸钙,为不引入杂质离子,所选试剂分别为:NaOH溶液和Na2CO3溶液,
故答案为:NaOH溶液;Na2CO3溶液;


科目:高中化学 来源: 题型:
【题目】在相同的密闭容器中,用高纯度纳米级Cu2O分别进行催化分解水的实验:2 H2O(g)![]() 2 H2(g) + O2(g) H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
2 H2(g) + O2(g) H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
序号 | 时间/min | 0 | 10 | 20 | 30 | 40 | 60 |
① | 温度T1 / 1号Cu2O | 0.0500 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
② | 温度T1 / 2号Cu2O | 0.0500 | 0.0490 | 0.0483 | 0.0480 | 0.0480 | 0.0480 |
③ | 温度T2 / 2号Cu2O | 0.0500 | 0.0480 | 0.0470 | 0.0470 | 0.0470 | 0.0470 |
下列说法不正确的是( )
A. 实验时的温度T2高于T1
B. 2号Cu2O的催化效率比1号Cu2O的催化效率高
C. 实验①前20 min的平均反应速率v(O2) = 7×10ˉ5 mol·Lˉ1·minˉ1
D. 等质量纳米级Cu2O比微米级Cu2O催化效率高,这与Cu2O的粒径大小有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家发明了一种“可固氮”的锂-氮二次电池,将可传递![]() 的醚类作电解质,电池的总反应为6Li +N2
的醚类作电解质,电池的总反应为6Li +N2![]() 2Ll3N,下列说法不正确的是( )
2Ll3N,下列说法不正确的是( )

A.固氮时,阳极区发生反应![]()
B.脱氮时,钌复合电极的电极反应:![]()
C.醚类电解质可换成![]() 溶液
溶液
D.脱氮时,![]() 向锂电极迁移
向锂电极迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分:
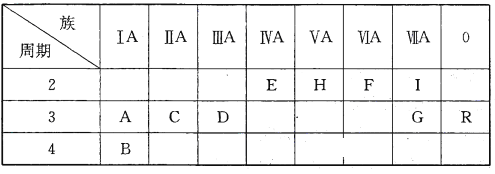
根据要求回答下列问题:
(1)十种元素中化学性质最不活泼的元素是__________________(填元素符号,下同),形成化合物种类最多的元素是_____________________。
(2)A、C、D三种元素的最高价氧化物对应的水化物,其中碱性最强的是______________(填化学式,下同),E、H、G三种元素的最高价氧化物对应的水化物中酸性最强的是______________。
(3)I元素跟A元素形成化合物的电子式是______________。高温灼烧该化合物时,火焰呈______________色。
(4)分别写出B、G两种单质和水反应的离子方程式_____________、________________。
(5)元素A和F能形成两种化合物,写出其中较稳定的化合物与CO2反应生成氧气的化学方程式:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对CH4与Cl2的反应(如图所示)叙述不正确的是( )
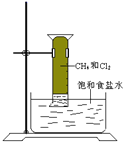
A.该反应属于取代反应
B.该反应的条件是光照
C.该反应的生成物有四种
D.该反应的现象是量筒内气体颜色变浅,器壁上有油状液滴,量筒内液面上升并产生白雾,水槽中有晶体析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的仪器选择和部分实验操作均正确的是( )
选项 | 实验 | 所选主要仪器铁架台等忽略 | 部分操作 |
A | 用浓硫酸配制480mL0.1mol/L硫酸溶液 | 500mL容量瓶、烧杯、玻璃棒、量筒、胶头滴管 | 将刚稀释所得的硫酸溶液立刻转移至500mL容量瓶,并加水至刻度线即可 |
B | 从食盐水中得到NaCl晶体 | 坩埚、酒精灯、玻璃棒、泥三角、三脚架 | 当加热至大量晶体出现时,停止加热,利用余热继续蒸干 |
C | 从碘的四氯化碳溶液中得到碘 | 蒸馏烧瓶、酒精灯、温度计、冷凝管、锥形瓶、牛角管 | 温度计水银球插入液液面以下 |
D | 用汽油提取溴水中的Br2 | 分液漏斗、烧杯 | 分离时下层液体从分液漏斗下口放出,上层液体从上口倒出 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象与实验操作不相匹配的是( )
实验操作 | 实验现象 | |
A | 将镁条点燃后迅速伸入集满CO2的集气瓶 | 集气瓶中产生浓烟并有黑色颗粒产生 |
B | 向盛有高锰酸钾酸性溶液的试管中通入足 量的乙烯后静置 | 溶液的紫色逐渐褪去,静置后溶液分层 |
C | 向盛有饱和硫代硫酸钠溶液的试管中滴加稀盐酸 | 有刺激性气味气体产生,溶液变浑浊 |
D | 向盛有FeCl3溶液的试管中加过量铁粉,充分振荡后加1滴KSCN溶液 | 黄色逐渐消失,加KSCN后溶液颜色不变 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组探究![]() 和
和![]() 的反应规律。实验操作及现象如下:
的反应规律。实验操作及现象如下:
实验及试剂 | 编号 | 无色 | 试管中溶液颜色 | 淀粉KI试剂颜色 |
| 1 | 0.5mL | 浅黄色 | 无色 |
2 | 0.20mL | 深黄色 | 无色 | |
3 | 0.25mL | 浅黄色 | 蓝色 | |
4 | 0.30mL | 无色 | 蓝色 |
(1)取实验2后的溶液,进行如下实验:

经康康同学检验,上述白色沉淀是![]() 。写出加入0.20mL
。写出加入0.20mL ![]() 后,溶液中
后,溶液中![]() 和
和![]() 发生反应的离子方程式:____________。
发生反应的离子方程式:____________。
(2)查阅资料:一定条件下,![]() 和
和![]() 都可以被氧化成
都可以被氧化成![]() 。
。
作出假设:![]() 溶液用量增加导致溶液褪色的原因是过量的
溶液用量增加导致溶液褪色的原因是过量的![]() 溶液与(1)中的反应产物继续反应,同时生成
溶液与(1)中的反应产物继续反应,同时生成![]() 。进行实验:
。进行实验:
①取少量实验4中的无色溶液进行以下实验,进一步佐证其中含有![]() 。
。

其中试剂X可以是_________(填字母序号)。
a 碘水 b ![]() 溶液 c
溶液 c ![]() 溶液 d
溶液 d ![]() 溶液
溶液
②李政同学提出,仅通过润湿淀粉![]() 试纸变蓝的现象不能说明生成
试纸变蓝的现象不能说明生成![]() ,理由是_______,便补充了如下实验:将实验4中的湿润淀粉
,理由是_______,便补充了如下实验:将实验4中的湿润淀粉![]() 试纸替换为________,在滴加
试纸替换为________,在滴加![]() 溶液后,发现________,进一步佐证实验4中生成了
溶液后,发现________,进一步佐证实验4中生成了![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上采用硫铁矿焙烧去硫后的烧渣(主要成分为Fe2O3、FeO、SiO2、Al2O3,不考虑其他杂质) 制取七水合硫酸亚铁(FeSO4·7H2O) ,流程如下:
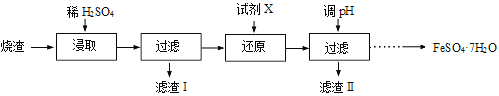
(1)浸取时,溶液中的Fe2+易被空气中的O2氧化,其离子方程式为 。能提高烧渣浸取速率的措施有 (填字母)。
A.将烧渣粉碎 B.降低硫酸的浓度 C.适当升高温度
(2)还原时,试剂X的用量与溶液pH的变化如图所示,则试剂X可能是 (填字母)。
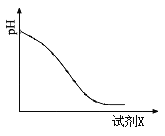
A.Fe粉 B.SO2 C.NaI
还原结束时,溶液中的主要阴离子有 。
(3)滤渣Ⅱ主要成分的化学式为 ;由分离出滤渣Ⅱ后的溶液得到产品,进行的操作是 、 过滤、洗涤、干燥。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com