
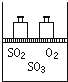
 如图,将4mol SO2和2mol O2混合置于体积可变的等压密闭容器中,在一定温度下发生如下反应2SO2(g)+O2(g)?2SO3(g);△H<0.该反应达到平衡状态时,测得气体的总物质的量为4.2mol.试回答:
如图,将4mol SO2和2mol O2混合置于体积可变的等压密闭容器中,在一定温度下发生如下反应2SO2(g)+O2(g)?2SO3(g);△H<0.该反应达到平衡状态时,测得气体的总物质的量为4.2mol.试回答:分析 (1)依据化学平衡三段式列式计算,设生成三氧化硫物质的量为2x,根据平衡时混合气体总物质的量为2.4mol列式计算得到三氧化硫物质的量;
(2)等压容器中,若起始时a=1.2mol,b=0.6mol,a:b=2:1,等于起始时加入的2mol SO2和1mol O2的量的比值,二者建立的平衡一定为等效平衡;
(3)起始时,若SO2和O2的量均为0,则c值最大,利用一边倒,完全转化为SO2和O2的量分别为2mol和1mol,C为2mol;根据(1)计算平衡时SO3的量为1.2mol,则c值应该大于1.2.
解答 解:(1)设反应达到平衡时生成三氧化硫物质的量为2x,
2SO2(g)+O2(g) $\frac{\underline{催化剂}}{△}$2SO3(g),△H<0
起始(mol) 4 2 0
变化(mol) 2x x 2x
平衡(mol) 4-2x 2-x 2x
(4-2x)+(2-x)+2x=4.2
x=1.8mol 则n(SO3)=3.6 mol,
故答案为:1.2mol;
(2)等压容器中,若起始时1.2mol SO2、0.6mol O2和x mol SO3,二氧化硫和氧气的物质的量之比是2:1,等于起始时加入的:4mol SO2和2mol O2的量的比值,反应2SO2(g)+O2(g)?2SO3(g)△H<0产物只有三氧化硫,无论三氧化硫的量为多少,利用一边倒的方法,转化为二氧化硫和氧气的量之比均为2:1,二者建立的平衡一定为等效平衡,故达到平衡后各气体的体积分数与平衡状态A相同,
故答案为:≥0的任意值;
(3)若要使反应开始时向逆反应方向进行,且达到平衡后各气体的物质的量与平衡状态A相同,三氧化硫最小值为(1)中平衡时三氧化硫的物质的量,即大于3.6mol,c值最大时,SO2和O2的量均为0,利用一边倒,完全转化为SO2和O2的量分别为4mol和2mol,C应为4mol,故3.6<c≤4,故答案为:3.6<c≤4.
点评 本题考查了等效平衡的判断与利用,题目难度较大,试题培养了学生的分析、理解能力及灵活应用所学知识解决实际问题的能力.


 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L1mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| B. | 88g乙酸乙酯中存在的共价键总数为14NA | |
| C. | 加热时,含2molH2SO4的浓硫酸与足量铜反应,转移的电子数为2NA | |
| D. | 1mol羟基所含的电子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2 mol | B. | 0.25 mol | C. | 0.3 mol | D. | 0.35 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| Zn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀pH | 5.4 | 7.0 | 2.3 | 4.7 |
| 完全沉淀pH | 8.0 | 9.0 | 4.1 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:5 | B. | 1:1 | C. | 2:1 | D. | 5:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com