
【题目】判断下列反应的熵值的变化,在每小题后面的横线上填上“增加”、“减小”或“无明显变化”。
(1)2H2(g)+O2(g) ![]() 2H2O(l)________。
2H2O(l)________。
(2)H2(g)+Cl2(g) ![]() 2HCl(g)________。
2HCl(g)________。
(3)(NH4)2CO3(s)=NH4HCO3(s)+NH3(g)_______________________________________。
(4)Cu(s)+Cl2(g) ![]() CuCl2(s)________。
CuCl2(s)________。
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
【题目】目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:
CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
已知H2的体积分数随温度升高而增加。
若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化。(选填“增大”、“减小”或“不变”)
v正 | v逆 | 平衡常数K | 转化率α |
相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
[CO2]/mol·L1 | [H2]/mol·L1 | [CH4]/mol·L1 | [H2O]/mol·L1 | |
平衡Ⅰ | a | b | c | d |
平衡Ⅱ | m | n | x | y |
a、b、c、d与m、n、x、y之间的关系式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾是一种常见的强氧化剂。实验室以精选铬铁矿(主要成分可表示为FeO.Cr2O3,还含有SiO2、Al2O3等杂质)为原料制备重铬酸钾晶体(K2Cr2O7,式量294)的流程如下:

请回答下列问题:
(1)操作1中发生的反应有:
4FeO·Cr2O3 + 8Na2CO3 + 7O2 = 8Na2CrO4 + 2Fe2O3 + 8CO2↑
Na2CO3 + Al2O3 = 2NaAlO2 + CO2↑ Na2CO3 + SiO2 = Na2SiO3 + CO2↑
该步骤在常温下的反应速率较慢,为使反应速率增大,可采取的措施是_____________________,__________________________。(写出两条)
(2)固体Y中主要含有 ______________。(填写化学式)
(3)酸化步骤使含铬物质发生了转化为_________,请写出离子反应方程式____________。
(4)操作4中的化学反应在溶液中能发生的可能理由是_________________,获得晶体的操作依次是:加入KCl固体,在水浴上加热浓缩至____________________,冷却结晶,抽滤、洗涤、干燥。
(5)通过下列实验可测定产品中重铬酸钾的质量分数:
称取重铬酸钾试样1.470g,用100mL容量瓶配制成溶液。移取25.00mL溶液于碘量瓶中,加入适量稀硫酸和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min。然后加入一定量的水,加入淀粉指示剂,用0.1500mol/L Na2S2O3标准溶液滴定,共消耗标准液36.00mL。滴定时发生的反应的离子方程式为:I2 + 2S2O32- = 2I- + S4O62-则所测定产品中重铬酸钾的纯度为___________。
(6)有关上述实验过程中涉及的部分实验操作的描述,正确的是____________。
A.粗产品若要进一步提纯,可以采用重结晶的方法
B.配制溶液时,用托盘天平称取试样后,一般经溶解、转移(含洗涤)、定容等步骤,配制成100mL溶液
C.滴定时,当最后一滴标准溶液滴入时,溶液变为蓝色,且半分钟内不变色,可判断滴定终点
D.滴定终点时俯视读数,测定结果偏低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图与对应的反应情况符合的是( )
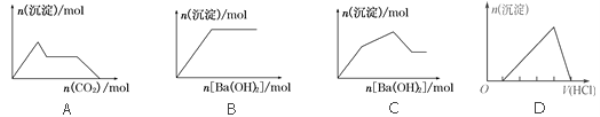
A. 向含0.01 mol KOH和0.01 mol Ca(OH)2的混合溶液中缓慢通入CO2至过量
B. 向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量
C. 向KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液至过量
D. 向含有少量氢氧化钠的NaAlO2溶液中逐滴加入盐酸至过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】V mL Al2(SO4)3溶液中含Al3+a g,取 ![]() mL溶液稀释到4V mL,则稀释后溶液中SO42﹣的物质的量浓度是( )
mL溶液稀释到4V mL,则稀释后溶液中SO42﹣的物质的量浓度是( )
A.![]() ?mol?L﹣1
?mol?L﹣1
B.![]() ?mol?L﹣1
?mol?L﹣1
C.![]() ?mol?L﹣1
?mol?L﹣1
D.![]() ?mol?L﹣1
?mol?L﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com