
【题目】实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数ω(Na2CO3),称取此混合物mg,溶于水中,配成溶液。
I.方案一:沉淀法。利用化学反应把HCO3-、CO32-完全转化为沉淀,称量干燥沉淀的质量,由此计算混合物中ω(Na2CO3)。
(1)量取配置好的溶液于烧杯中,滴加足量沉淀剂,把溶液中HCO3-、CO32-完全转化为沉淀,应选用的试剂是 。
(2)若选用(1)的沉淀剂沉淀后,过滤,洗涤沉淀,判断沉淀是否洗净的方法是 。
II.方案二:量气法。如图所示,量取配制好的溶液与足量稀硫酸溶液反应,测定生成气体的体积,由此计算混合物中ω(Na2CO3)。
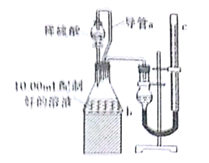
(1)装置中导管a的作用是 。
(2)正确读取气体体积的操作 。
(3)某同学根据方案二的思路提出方案三:把生成的气体通入足量的生石灰,测定增重的质量,由此计算混合物中ω(Na2CO3),若按此方案,则测得的ω(Na2CO3) (填“偏大”“偏小”或“无影响”)。为减小误差,请完善他的方案 。
【答案】I.(1)Ba(OH)2溶液[或Ca(OH)2溶液,合理即可]
(2)取少量最后一次洗涤液,滴加Na2SO4溶液,如无沉淀,则沉淀已洗净,反之则为未完成
II.(1)平衡气压,使液体顺利滴下
(2)读数前上下移动c,使b、c的液面相平,读数时,视线要和c的凹液面相切
(3)偏小 应先把气体通入浓硫酸后再通入生石灰
【解析】
试题分析:I.(1)把溶液中HCO3-、CO32-完全转化为沉淀,需要加入碱,且要生成碳酸盐的沉淀,所以应选用的试剂是Ba(OH)2溶液。
(2)加入沉淀剂Ba(OH)2溶液沉淀后,过滤,洗涤沉淀,是洗去沉淀上粘附的Ba2+,所以判断沉淀是否洗净的方法是取少量最后一次洗涤液,滴加Na2SO4溶液,如无沉淀,则沉淀已洗净,反之则为未完成。
II.(1)由于碳酸盐与酸反应产生二氧化碳气体,瓶内压强增大,所以装置中导管a的作用是平衡压强、使液体顺利滴下。
(2)读数时必须与外界大气压相同,因此注意事项是①待冷却至室温才开始读数,②读数前上下移动c,使b、c的液面相平, 读数时,视线要和c的凹液面相切。
(3)生成的气体中含有水蒸气,通入足量的生石灰,测定增重的质量是CO2和水蒸气的质量,碳酸氢钠的质量增加,由此计算混合物中ω(Na2CO3)将偏小;为减小误差,需先除去水蒸气,所以方案为应先把气体通入浓硫酸后再通入生石灰。


科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 食盐和醋可作调味剂,也可用作食品防腐剂 B. 植物秸秆不可用来制造酒精
C. 镁合金可用于制造火箭、导弹和飞机的部件 D. 二氧化硅可用于制光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X2、Y2、Z2、W2的氧化能力为:W2>Z2>X2>Y2 ,下列反应能够发生的是
A. 2W-+Z2=2Z-+W2 B. 2X-+Z2=2Z-+X2
C. 2W-+Y2 = 2Y-+W2 D. 2Z-+X2=2X-+Z2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学实验操作中“先”与“后”的说法错误的是( )
A.用排水法收集气体后,先移出导管后撤酒精灯
B.给试管加热时,先均匀加热,后局部加热
C.碱液流到桌子上,先用稀醋酸溶液中和,后用水洗
D.浓硫酸不慎溅到到皮肤上,先涂上质量分数为3%~5%的NaHCO3溶液,后用水冲洗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定某氯酸钾与二氧化锰混合物中氯酸钾的质量分数,课外小组的同学设计了如下实验:取3.0g 混合样品放入如图所示的大试管中,充分加热,直到反应完全,并用如图所示装置测量出生成氧气的体积。试回答下列问题:
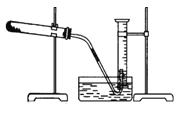
(1)如何检查装置的气密性?
(1)现有如下可供选择的操作:①将导气管放入盛满水的量筒内;②给药品加热;③有连续气泡产生时开始收集气体;④取出导气管;⑤反应完全后停止加热(如图,此时导管出口略高于液面);⑥冷却至室温;⑦调整量筒内外液面高度使之相同后读出量筒内气体体积数。
为了较准确地测量出生成的氧气在常温、常压下的体积,正确的操作顺序是(填序号)______________。
(3)为了较准确地测量到气体的体积,需要调整量筒内外液面高度,其原理是:____________________。
(4)在常温常压下共收集到气体680mL(此时氧气密度为1.41g·L-1),其质量为_______g,原混合物中氯酸钾的质量分数约是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.将一小块铜片放入盛有浓硫酸的试管中加热反应后的溶液呈蓝色
B.将一小块钠放入盛有水的烧杯中,钠在水面上游动,同时看到烧杯内的溶液变为红色
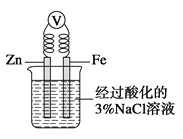
C.如图,一段时间后给烧杯内的溶液中加入黄色的K3[Fe(CN)6]溶液,可看到Fe电极附近有蓝色沉淀生成
D.向盛有少量Mg(OH)2沉淀悬浊液的试管中滴加氯化铵溶液,可看到沉淀溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况.试判断,违反了泡利原理的是 ,违反了洪特规则的是 .
A. |
B. |
C. |
D. |
E.![]()
F.![]()
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为 ;其最高价氧化物对应水化物的化学式是 .
(3)用符号“>”“<”或“=”表示下列各项关系.
①第一电离能:Na Mg,Mg Ca.
②电负性:O F,F Cl.
③能量高低:ns (n+1)s,ns np.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量浓度的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图,则下列说法正确的是( )

A. 阳极产物一定是Cl2,阴极产物一定是Cu
B. BC段表示在阴极上是H+放电产生了H2
C. AB、BC段阴极反应都为Cu2+ + 2e-= Cu
D. CD段表示阳极上OH一放电破坏了水的电离平衡,产生了H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]较硫酸亚铁不易被氧气氧化,是分析化学中重要的试剂,常用于代替硫酸亚铁。硫酸亚铁铵在 500 ℃时隔绝空气加热完全分解。回答下列问题:
(1)硫酸亚铁铵隔绝空气加热完全分解,发生了氧化还原反应,固体产物可能有FeO和Fe2O3,气体产物可能有NH3、SO3、H2O、N2和__________。
(2)为检验分解产物的成分,设计如下实验装置进行实验,加热A中的硫酸亚铁铵至分解完全。

① A中固体充分加热较长时间后,通入氮气,目的是__________________________。
②为验证A中残留物是否含有FeO,需要选用的试剂有____________(填字母)。
A.KSCN溶液 B.稀硫酸
C.浓盐酸 D.KMnO4溶液
③装置B中BaCl2溶液的作用是为了检验分解产物中是否有________气体生成,若含有该气体,观察到的现象为_______________________________________。
④若A中分解产物有N2,固体残留物只有Fe2O3,Fe2O3的物质的量为b mol,C中沉淀物质的量为a mol,则b________________(填“大于”“小于”或“等于”)a。
⑤实验中,观察到C中有白色沉淀生成,则C中发生的反应为___________________________________________(用离子方程式表示)。
(3)为测定某固体样品中(NH4)2Fe(SO4)2·6H2O的含量,某实验小组做了如下实验:
测定原理:MnO![]() +Fe2++H+―→Mn2++Fe3++H2O(方程式未配平)
+Fe2++H+―→Mn2++Fe3++H2O(方程式未配平)
测定步骤:步骤一:准确称量20.00 g硫酸亚铁铵晶体,配制成100 mL溶液。
步骤二:取所配溶液25.00 mL于锥形瓶中,加稀H2SO4酸化,用0.100 0 mol·L-1 KMnO4溶液滴定至终点,重复两次,平均消耗KMnO4溶液16.00 mL。
①如何判断滴定终点?________________________;
②产品中(NH4)2Fe(SO4)2·6H2O的质量分数为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com