
分析 ①乙醇被氧化,所以负极为乙醇失去电子的过程;
②C4H10在负极发生氧化反应,生成二氧化碳气体和水.
解答 ①燃料乙醇发生失电子的氧化反应,在碱性环境下的电极反应为:C2H6O+16OH--12e-=2CO32-+11H2O,故答案为:C2H6O+16OH--12e-=2CO32-+11H2O;
②C4H10在负极发生氧化反应,生成二氧化碳气体和水,电极反应式为:2C4H10+26CO32--52e-=34CO2+10H2O,故答案为:2C4H10+26CO32--52e-=34CO2+10H2O.
点评 本题考查了原电池原理,明确正负极上得失电子的物质是解本题关键,比较容易.


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:选择题
| A. | 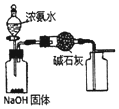 用图装置,制取干燥纯净的NH3 | |
| B. |  用图装置,实验室制备Fe(OH)2 | |
| C. | 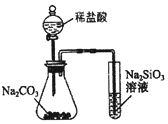 用图所示实验,可比较氯、碳、硅三种元素的非金属性强弱 | |
| D. | 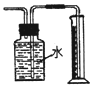 用图装置测量Cu与浓硝酸反应产生气体的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
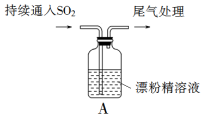 某化学兴趣小组的同学们对SO2通入漂粉精溶液的反应进行实验探究:
某化学兴趣小组的同学们对SO2通入漂粉精溶液的反应进行实验探究:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 进行蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸,如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加 | |
| B. | 提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法 | |
| C. | 1一己醇的沸点比己烷的沸点高,1一己醇和己烷可通过蒸馏初步分离 | |
| D. | 提纯含有少量乙酸的乙酸乙酯;向含有少量乙酸的乙酸乙脂中加入适量饱和Na2CO3溶液,振荡后静置分液,并除去有机相的水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L二氯甲烷的分子数约为NA | |
| B. | 室温下,1L pH=12的碳酸钠溶液中含有Na+的数目为0.02NA | |
| C. | 1L 0.1mol•L-1K2Cr2O7溶液中Cr2O72-的数目小于0.1NA | |
| D. | 电解精炼铜时,若阴极得到的电子数为2NA,则阳极质量一定减少64 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原溶液中含有硫酸铜$\frac{4}{5}$(b+C)g | |
| B. | 原溶液浓度为 $\frac{4(b+C)}{V}$mol/L | |
| C. | 室温时硫酸铜溶解度为$\frac{160C}{50a+9C}$g | |
| D. | 原溶液的溶质质量分数为$\frac{32(b+C)}{3a+b+C}$% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
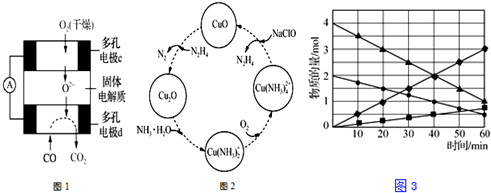
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 电池工作时,锌失去电子 | |
| B. | 电池工作时,电子由正极通过外电路流向负极 | |
| C. | 电池正极的电极反应式为2MnO2(s)+H2O(l)+2e-═Mn2O3(s)+2OH-(aq) | |
| D. | 外电路中每通过0.1 mol电子,锌的质量理论上减少6.5 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com