
| O | - 3 |
| 3.6g |
| 5.0g |
| O | - 3 |


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
A.在氧化还原反应中不一定所有元素的化合价都发生变化
B.只有得氧或失氧的化学反应才是氧化还原反应
C.化合反应和分解反应不可能是氧化还原反应
D.氧化还原反应中,被氧化和被还原的可以是同一种元素
查看答案和解析>>
科目:高中化学 来源: 题型:
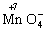 氧化为
氧化为查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关氧化还原反应的叙述正确的是( )
A.在氧化还原反应中不一定所有元素的化合价都发生变化
B.只有得氧或失氧的化学反应才是氧化还原反应
C.化合反应和分解反应不可能是氧化还原反应
D.氧化还原反应中,被氧化和被还原的可以是同一种元素
查看答案和解析>>
科目:高中化学 来源:2014届广西武鸣高中高一上学期段考化学试卷 题型:选择题
下列叙述中,正确的是
A.含氧酸能起氧化作用,无氧酸则不能
B.阳离子只有氧化性,阴离子只有还原性
C.金属阳离子被还原不一定得到金属单质
D.在氧化还原反应中,氧化剂被氧化,还原剂被还原
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com