
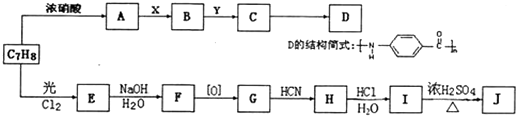
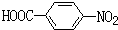
 ;
;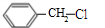 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$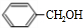 +NaCl;I→J
+NaCl;I→J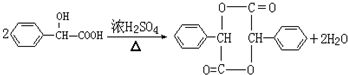 .
.分析 由D的结构简式可知,C发生缩聚反应生成D,故C为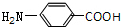 ,甲苯发生硝化反应生成A,A经过系列反应得到C,可知A为
,甲苯发生硝化反应生成A,A经过系列反应得到C,可知A为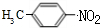 ,由于氨基易被氧化,故应先将甲基氧化为羧基,再将硝基还原为氨基,故X可以是酸性高锰酸钾溶液,Y为Fe/HCl,则B为
,由于氨基易被氧化,故应先将甲基氧化为羧基,再将硝基还原为氨基,故X可以是酸性高锰酸钾溶液,Y为Fe/HCl,则B为 .
.
甲苯在光照条件下发生甲基上的取代反应生成E,物质E为一氯代物,则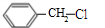 ,
,
E在氢氧化钠水溶液、加热条件下生成卤代烃的水解反应生成F为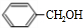 ,F发生氧化反应生成G为
,F发生氧化反应生成G为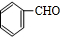 ,G与HCN发生信息中的加成反应生成H为
,G与HCN发生信息中的加成反应生成H为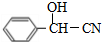 ,H发生水解反应生成I为
,H发生水解反应生成I为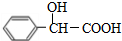 ,I在浓硫酸作用生成含三个六元环的酯类化合物J,应是2分子I发生酯化反应生成环酯,则J为
,I在浓硫酸作用生成含三个六元环的酯类化合物J,应是2分子I发生酯化反应生成环酯,则J为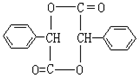 ,据此解答.
,据此解答.
解答 解:由D的结构简式可知,C发生缩聚反应生成D,故C为 ,甲苯发生硝化反应生成A,A经过系列反应得到C,可知A为
,甲苯发生硝化反应生成A,A经过系列反应得到C,可知A为 ,由于氨基易被氧化,故应先将甲基氧化为羧基,再将硝基还原为氨基,故X可以是酸性高锰酸钾溶液,Y为Fe/HCl,则B为
,由于氨基易被氧化,故应先将甲基氧化为羧基,再将硝基还原为氨基,故X可以是酸性高锰酸钾溶液,Y为Fe/HCl,则B为 .
.
甲苯在光照条件下发生甲基上的取代反应生成E,物质E为一氯代物,则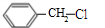 ,
,
E在氢氧化钠水溶液、加热条件下生成卤代烃的水解反应生成F为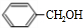 ,F发生氧化反应生成G为
,F发生氧化反应生成G为 ,G与HCN发生信息中的加成反应生成H为
,G与HCN发生信息中的加成反应生成H为 ,H发生水解反应生成I为
,H发生水解反应生成I为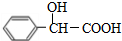 ,I在浓硫酸作用生成含三个六元环的酯类化合物J,应是2分子I发生酯化反应生成环酯,则J为
,I在浓硫酸作用生成含三个六元环的酯类化合物J,应是2分子I发生酯化反应生成环酯,则J为 ,
,
(1)由于酸性KMnO4会氧化C6H5-NH2生成焦油状的复杂物质,故应先将 中甲基氧化为羧基,再将硝基还原为氨基,故X为酸性KMnO4,
中甲基氧化为羧基,再将硝基还原为氨基,故X为酸性KMnO4,
故答案为:②;酸性KMnO4会氧化C6H5-NH2生成焦油状的复杂物质;
(2)由上述分析可知,B的结构简式为 ,故答案为:
,故答案为: ;
;
(3)C→D 是 生成高聚物,同时生成水,属于缩聚反应,G→H是G中醛基与HCN发生加成反应,故答案为:缩聚反应;加成反应;
生成高聚物,同时生成水,属于缩聚反应,G→H是G中醛基与HCN发生加成反应,故答案为:缩聚反应;加成反应;
(4)E→F的反应方程式为: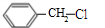 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$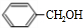 +NaCl;
+NaCl;
I→J的反应方程式为: ,
,
故答案为: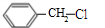 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$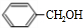 +NaCl;
+NaCl; .
.
(5)C为 ,①苯环上有3个取代基 ②能与FeCl3溶液发生显色反应,说明含有酚羟基,③能发生银镜反应,说明含有醛基,另一个取代基为氨基,利用定一移二法,首先固定醛基,让酚羟基与其临位,移动氨基,有4种可能的结构,若醛基与酚羟基在间位,移动氨基有4种可能的结构,若醛基与酚羟基在对位,移动氨基有2种可能的结构,所以其共有10种同分异构体,故答案为:10.
,①苯环上有3个取代基 ②能与FeCl3溶液发生显色反应,说明含有酚羟基,③能发生银镜反应,说明含有醛基,另一个取代基为氨基,利用定一移二法,首先固定醛基,让酚羟基与其临位,移动氨基,有4种可能的结构,若醛基与酚羟基在间位,移动氨基有4种可能的结构,若醛基与酚羟基在对位,移动氨基有2种可能的结构,所以其共有10种同分异构体,故答案为:10.
点评 本题考查有机物的推断,需要学生熟练掌握官能团的性质与转化,根据反应条件及D的结构,利用正推法、逆推法相结合进行推断,难度中等.


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 用M表示此反应的反应速率γ(M)=0.1a mol•(L•min)-1 | |
| B. | 当混合气体的质量不再发生变化时,说明反应达到平衡状态 | |
| C. | 向平衡后的体系中加入l mol M,平衡向逆反应方向移动 | |
| D. | 向上述平衡体系中再充入l mol X,平衡正向移动,因为此时γ正增大,γ逆减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol任何气体的体积都是约22.4L | |
| B. | 标准状况下,氧气的体积约为22.4L | |
| C. | 标准状况下,1mol氢气、氮气的混合气体,体积约为22.4L | |
| D. | 标准状况下,18g水的体积恰好是22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,2.24L乙炔(H-C≡C-H)中σ键数为0.4NA | |
| B. | 1mol苯分子中共有6NA个原子共平面 | |
| C. | 在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA | |
| D. | 64g铜片投入足量浓H2SO4中生成NA个SO2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平均相对分子质量 | B. | 密度 | ||
| C. | 容器内的压强 | D. | 物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MnO2与浓盐酸反应制Cl2:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl-+Cl2↑+2H2O | |
| B. | 醋酸除去水垢:2H++CaCO3═Ca2++CO2↑+H2O | |
| C. | Na2O2溶于水产生O2:Na2O2+H2O═2Na++2OH-+O2↑ | |
| D. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 现有21.6g由CO和CO2组成的混合气体,在标准状况下其体积为13.44L,回答下列问题:
现有21.6g由CO和CO2组成的混合气体,在标准状况下其体积为13.44L,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NA表示阿伏伽德罗常数,1mol Na被完全氧化生成Na2O2,失去2NA个电子 | |
| B. | Na2O2用作呼吸面具的供氧剂及氧化还原反应 | |
| C. | 苏打是面包发酵粉的主要成分之一 | |
| D. | NaHCO3的热稳定性大于Na2CO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com