
���� ��1����ѧƽ�ⳣ��Ϊ������ƽ��Ũ��ϵ�����ݵij˻��뷴Ӧ��Ũ��Ũ��ϵ�����ݳ˻��ı�ֵ��
��2������Ũ����Qc����ƽ�ⳣ���Ƚϣ���Qc=K�����ڻ�ѧƽ��״̬����Qc��K����Ӧ���淴Ӧ������У���Qc��K����Ӧ������Ӧ������У�
��3��T��ʱ����1L�ܱ������г���A��B��1mol����ƽ��ʱת����BΪxmol����
A��g��+B��g��?2C��g��+2D��s��
��ʼ��mol����1 1 0
ת����mol����x x 2x
ƽ�⣨mol����1-x 1-x 2x
�ٸ���ƽ�ⳣ���з��̼���x����������ƽ��ʱB��ת���ʣ�
���º�ѹ�£�ѹǿ֮�ȵ������ʵ���֮�ȣ���Ӧǰ����������ʵ������䣬��ѹǿ��ȣ�
��4������º��ݵ��ܱ������г���1molA��1molB���ﵽƽ��״̬���������г���2molC��3molD����ЧΪ��ʼ����2molA��2molB��1molD��DΪ���壬��Ӱ��ƽ���ƶ������ڷ�Ӧǰ����������ʵ������䣬A��B�����ʵ���֮��Ϊ1��1������ԭƽ��Ϊ��Чƽ�⣻
��5��������ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ���ƽ�ⳣ������
�ڴ����ӿ췴Ӧ���ʣ���Ӱ��ƽ���ƶ���
��ѹǿP2�ȵ���ƽ�⣬��ѹǿP2��P1����Ӧ���������������䣬ѹǿ��Ӱ��ƽ���ƶ���
�ܻ���������ʵ������䣬�淴Ӧ���л��������������С��ƽ����Է���������С������ƽ��䣮
��� �⣺��1��A��g��+B��g��?2C��g��+2D��s���Ļ�ѧƽ�ⳣ������ʽK=$\frac{{c}^{2}��C��}{c��A����c��B��}$��
�ʴ�Ϊ��$\frac{{c}^{2}��C��}{c��A����c��B��}$��
��2��Ũ����Qc=$\frac{��3��1{0}^{-2}��^{2}}{2.5��1{0}^{-1}��4.0��1{0}^{-2}}$=0.09��K=1��10-2����Ӧ���淴Ӧ������У�
�ʴ�Ϊ�����淴Ӧ������У�$\frac{��3��1{0}^{-2}��^{2}}{2.5��1{0}^{-1}��4.0��1{0}^{-2}}$=0.09��K=1��10-2��
��3��T��ʱ����1L�ܱ������г���A��B��1mol����ƽ��ʱת����BΪxmol����
A��g��+B��g��?2C��g��+2D��s��
��ʼ��mol����1 1 0
ת����mol����x x 2x
ƽ�⣨mol����1-x 1-x 2x
��$\frac{��2x��^{2}}{��1-x������1-x��}$=1��10-2�����x=$\frac{1}{21}$����B��ת����Ϊ$\frac{\frac{1}{21}mol}{1mol}$��100%=4.8%��
���º�ѹ�£�ѹǿ֮�ȵ������ʵ���֮�ȣ���Ӧǰ����������ʵ������䣬���ʱ��ϵ�ڵ�ѹǿ�뷴Ӧǰ��ѹǿ��Ϊ1��1��
�ʴ�Ϊ��4.8��1��1��
��4������º��ݵ��ܱ������г���1molA��1molB���ﵽƽ��״̬���������г���2molC��3molD����ЧΪ��ʼ����2molA��2molB��1molD��DΪ���壬��Ӱ��ƽ���ƶ������ڷ�Ӧǰ����������ʵ������䣬A��B�����ʵ���֮��Ϊ1��1������ԭƽ��Ϊ��Чƽ�⣬��ԭƽ��״̬��ȣ���ʱƽ����������C������������䣬
�ʴ�Ϊ�����䣻
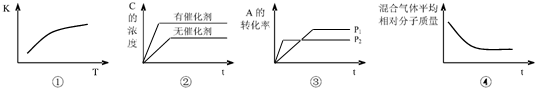
��5��������ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ���ƽ�ⳣ������ͼ����ϣ�����ȷ��
�ڴ����ӿ췴Ӧ���ʣ����̵���ƽ���ˮ�⣬����Ӱ��ƽ���ƶ���ͼ����Ӱ��ƽ���ƶ����ʴ���
��ѹǿP2�ȵ���ƽ�⣬��ѹǿP2��P1����Ӧ���������������䣬ѹǿ��Ӱ��ƽ���ƶ�����ͼ����ѹǿӰ��ƽ���ƶ����ʴ���
�ܻ���������ʵ������䣬�淴Ӧ���л��������������С��ƽ����Է���������С������ƽ��䣬ͼ����ϣ�����ȷ��
��ѡ���٢ܣ�
���� ���⿼�黯ѧƽ����㡢ƽ�ⳣ��Ӧ�á���Чƽ�⡢��ѧƽ��ͼ��Ӱ�����صȣ��ϺõĿ���ѧ���������������������Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� ���˹���������ѧ������Ϊ���Ӽ������ۼ����˹�����AB2��Ӧ�Ļ�ѧ����ʽ�ǣ�2Na2O2+2CO2=2Na2CO3+O2��
���˹���������ѧ������Ϊ���Ӽ������ۼ����˹�����AB2��Ӧ�Ļ�ѧ����ʽ�ǣ�2Na2O2+2CO2=2Na2CO3+O2���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������������Ƶ�����Ϊ����$\frac{40a}{31}$g | |
| B�� | ��λ�����Һ��OH-�������� | |
| C�� | ��Һ��Na+��Ŀ���� | |
| D�� | ��������ˮ��Ӧ�����˼�������ʵ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
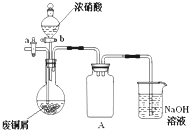 ��ʽ̼��ͭ[Cu2��OH��2CO3]��һ����;�㷺�Ļ���ԭ�ϣ�ʵ�����Է�ͭмΪԭ����ȡ��ʽ̼��ͭ�IJ������£�
��ʽ̼��ͭ[Cu2��OH��2CO3]��һ����;�㷺�Ļ���ԭ�ϣ�ʵ�����Է�ͭмΪԭ����ȡ��ʽ̼��ͭ�IJ������£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 һ���¶��£���2.0L�����ܱ������г���1.0mol PCl5����ӦPCl5��g��?PCl3��g��+Cl2��g����H������һ��ʱ���ﵽƽ�⣬��Ӧ�����вⶨ�IJ���������ͼ������˵����ȷ���ǣ�������
һ���¶��£���2.0L�����ܱ������г���1.0mol PCl5����ӦPCl5��g��?PCl3��g��+Cl2��g����H������һ��ʱ���ﵽƽ�⣬��Ӧ�����вⶨ�IJ���������ͼ������˵����ȷ���ǣ�������| A�� | ��Ӧ��50s��250s�ڵ�ƽ������v��PCl3��=4.0��10-4mol•L-1•s-1 | |
| B�� | ���������������䣬�����¶ȣ�ƽ��ʱc��PCl5��=0.38 mol•L-1����Ӧ�ġ�H��0 | |
| C�� | ���������������䣬���������ݻ���Сһ�룬ƽ�������ƶ�����ѧƽ�ⳣ����С | |
| D�� | ��ͬ�¶��£���ʼʱ�������г���0.5 mol PCl5�����´ﵽƽ��ʱ��0.1 mol��n��PCl3����0.2 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HA������ | B�� | HA�ĵ��뷽��ʽΪHA�TH++A- | ||
| C�� | ����Һ��c��HA��+c��A-��=0.1 mol•L-l | D�� | NaA��Һ�ʼ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
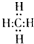 ���ṹʽ��
���ṹʽ��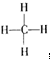 ����˵�����������������������ƽ��ṹ�������Ǣڣ�����д��ţ�
����˵�����������������������ƽ��ṹ�������Ǣڣ�����д��ţ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{c��{H}^{+}��•c��N{H}_{3}•{H}_{2}O��}{c��N{H}_{4}^{+}��}$ | B�� | $\frac{c��N{H}_{4}^{+}��•c��O{H}^{-}��}{c��N{H}_{3}•{H}_{2}O��}$ | ||
| C�� | $\frac{c{H}^{+}}{cO{H}^{-}}$ | D�� | c��H+��•c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
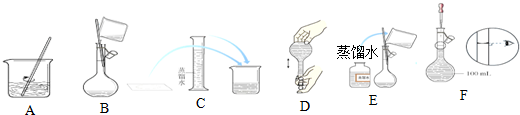
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com