
分析 甲烷与氯气在光照条件下发生取代反应,甲烷中四个氢原子可以逐步被氯原子取代,生成有机物有CH3Cl、CH2Cl2、CHCl3、CCl4;
结构相似,在分子组成上相差一个或若干个CH2原子团的化合物互称同系物,据此分析.
解答 解:甲烷与氯气在光照条件下发生取代反应,甲烷中四个氢原子可以逐步被氯原子取代,故生成有机物有一氯甲烷CH3Cl、二氯甲烷CH2Cl2、三氯甲烷CHCl3和四氯化碳CCl4;
结构相似,在分子组成上相差一个或若干个CH2原子团的化合物互称同系物,故乙烷的同系物必须是同属于烷烃的化合物,如甲烷CH4.
故答案为:CH3Cl、CH2Cl2、CHCl3、CCl4;CH4.
点评 本题考查了甲烷的取代反应的产物和同系物的概念以及书写和判断,难度不大,注意基础的把握.


科目:高中化学 来源: 题型:解答题

| 温度/℃ | 20 | 40 | 60 | 80 |
| 溶解度(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| 溶解度(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
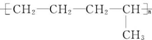 的单体是CH2═CH-CH3、CH2═CH2;(写结构简式)
的单体是CH2═CH-CH3、CH2═CH2;(写结构简式)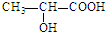 )中的官能团名称是:羟基、羧基;两分子乳酸在浓硫酸加热的条件下,可生成一种环状酯,写出此酯的结构简式:
)中的官能团名称是:羟基、羧基;两分子乳酸在浓硫酸加热的条件下,可生成一种环状酯,写出此酯的结构简式: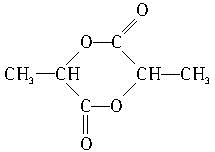 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀. |  |
| 步骤2:取适量滤液于试管中,滴加稀硫酸. | 有白色沉淀生成,说明有Ba2+; |
| 步骤3:取适量步骤1中的沉淀于是试管中,滴加稀盐酸,用带塞导气管塞紧试管,把导气管插入装有澄清石灰水的烧杯中 | 试管中有气泡生成,烧杯中的澄清石灰水变浑浊,结合步骤2说明沉淀是BaCO3 |
| 步骤4:取适量滤液于烧杯中,用pH计测其pH值 | pH>9.6,说明有大量的OH-,综合上面步骤可知试剂由大量Ba(OH)2•8H2O和少量BaCO3组成,假设成立. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
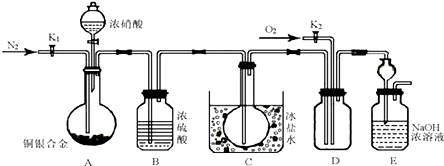
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 要想使AlCl3溶液中的Al3+几乎全部沉淀出来,可以加入过量的氨水 | |
| B. | 向FeCl2溶液中加入氨水,最终会看到红褐色沉淀 | |
| C. | 漂白粉的有效成分是次氯酸钙 | |
| D. | 氢氧化钠、纯碱溶液要存放在带磨砂玻璃塞的试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
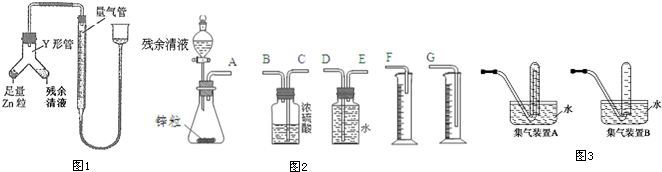
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com