
| A. | CH3CH2 CH3的三个碳原子在一条直线 | |
| B. | CH2=CHCH3三个碳原子共平面 | |
| C. |  七个碳原子共平面 七个碳原子共平面 | |
| D. | CH4所有原子共平面 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 先配制0.10 mol/L CH3COOH溶液,再测溶液的pH,若pH大于1,则可证明醋酸为弱电解质 | |
| B. | 先配制0.01 mol/L和0.10 mol/L的CH3COOH,再分别用pH计测它们的pH,若两者的pH相差小于1个单位,则可证明醋酸是弱电解质 | |
| C. | 取等体积、等pH的CH3COOH的溶液和盐酸分别与足量锌反应,测得反应过程中醋酸产生H2速率较慢且最终产生H2较多,则可证明醋酸为弱电解质 | |
| D. | 配制一定量的CH3COONa溶液,测其pH,若常温下pH大于7,则可证明醋酸是弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
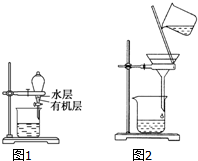
| A. | 分离乙醇和乙酸乙酯的混合物,所用玻璃仪器为分液漏斗、烧杯 | |
| B. | 用如图1所示装置分离CCl4萃取碘水后已分层的有机层和水层 | |
| C. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | |
| D. | 用如图2所示装置除去乙醇中的苯酚 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
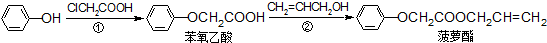
| A. | 步骤①产物中残留的苯酚可用FeCl3溶液检验 | |
| B. | 步骤②产物中残留的CH2=CHCH2OH可用溴水检验 | |
| C. | 苯酚和菠萝酯均可与酸性KMnO4溶液发生反应 | |
| D. | 苯氧乙酸和菠萝酯均可与H2在一定条件下发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸分子中含有羧基,可与NaHCO3溶液反应生成 CO2 | |
| B. | 所有的醇在铜做催化剂加热的条件下,都能与O2 发生氧化 | |
| C. | 甲烷和氯气在光照下的反应与苯的硝化反应的反应类型相同 | |
| D. | 苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素的化学性质随着相对原子质量的递增而呈周期性变化 | |
| B. | 元素周期律的实质是因为元素原子最外层电子数由1→8周期性变化而引起的 | |
| C. | 半径由大到小、氧化性由弱到强的是K+、Mg2+、Al3+、H+,而还原性由弱到强的则是I-、Br-、Cl-、F- | |
| D. | 某元素R的最高价氧化物化学式为R2O5,又知R的气态氢化物中含氢的质量分数为8.8%,则R的相对原子质量为28 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 酸性锌锰干电池和碱性锌锰干电池 | B. | 铅蓄电池 | ||
| C. | 氢气燃料电池和甲烷燃料电池 | D. | 镍镉电池和锂电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ④ | C. | ①④⑤ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
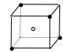 A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,A、D同主族,E和其它元素既不同期也不同主族,B、C、D最高价氧化物的水化物两两混合均能发生反应,A和E可组成离子化合物,其晶体结构示意图如图所示,其中“●”代表阳离子,“○”代表阴离子.
A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,A、D同主族,E和其它元素既不同期也不同主族,B、C、D最高价氧化物的水化物两两混合均能发生反应,A和E可组成离子化合物,其晶体结构示意图如图所示,其中“●”代表阳离子,“○”代表阴离子. H++F-.
H++F-.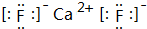 ,其晶体类型为离子晶体.
,其晶体类型为离子晶体.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com