
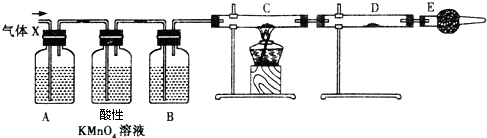
分析 (1)浓H2SO4浓度逐渐变稀,Zn与稀H2SO4反应可产生H2;
(2)装置是气体验证试验,所以需要装置气密性完好;
(3)装置A是验证二氧化硫存在的装置;B装置是干燥气体,防止水蒸气影响氢气与CuO反应产物的检验;E中加入的试剂如果是碱石灰,可以防止空气中的水蒸气进入D中;
(4)氢气和氧化铜反应生成铜和水,水和无水硫酸铜反应生成蓝色的五水硫酸铜.
解答 解:(1)反应过程中浓H2SO4浓度逐渐变稀,Zn与稀H2SO4反应可产生H2,反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑,离子方程式为:Zn+2H+=Zn2++H2↑;
故答案为:Zn+2H+=Zn2++H2↑;
(2)装置是气体验证试验,所以需要装置气密性完好,实验开始先检验装置的气密性;
故答案为:检查装置的气密性;
(3)分析装置图可知,生成的气体中有二氧化硫和氢气,所以装置A是验证二氧化硫存在的装置,选品红溶液进行验证;B装置是干燥气体,防止水蒸气影响氢气与CuO反应产物的检验,B中是液体干燥剂,所以为浓H2SO4;E中加入的试剂如果是碱石灰,可以防止空气中的水蒸气进入D中,避免对氢气与CuO反应产物检验产生干扰;
故答案为:检验SO2;浓H2SO4;防止空气中的水蒸气进入D中;
(4)为了检验氢气的存在,氢气与氧化铜在加热条件下反应生成铜和水,该反应的化学方程式为:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,黑色CuO变成红色的Cu,需用无水硫酸铜检验氢气被氧化的产物水,水和无水硫酸铜反应生成蓝色的五水合硫酸铜,所以可以证明气体X中含有H2的实验现象是:C中黑色CuO变成红色的Cu,D中白色粉末变成蓝色,
故答案为:白色粉末变成蓝色.
点评 本题考查锌和硫酸的反应及产物的检验,题目难度中等,注意掌握浓硫酸的性质,根据需检验气体的性质、检验方法理解检验的先后顺序是解答的关键,侧重于考查学生的分析能力和实验探究能力.


科目:高中化学 来源:2017届吉林省高三上第二次模拟化学试卷(解析版) 题型:选择题
下列离子方程式与所述事实相符且正确的是
A.向FeBr2溶液中通入过量的Cl2:2Fe2++2Br-+2Cl2===2Fe3++Br2+4Cl-
B.用食醋除去水壶内的水垢:CaCO3+2H+ = Ca2++CO2↑+H2O
C.KHCO3与足量澄清石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
D.在强碱性溶液中,次氯酸钠将Mn2+氧化成MnO2:Mn2++ClO-+H2O=MnO2↓+Cl-+2H+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高一9月月考化学卷(解析版) 题型:填空题
向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式__________________。
(2)下列三种情况下,离子方程式与(1)相同的是__________(填序号)。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
若在A项所得溶液中,继续滴加Ba(OH)2溶液,此步反应的离子方程式为:________________

(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用右上图中的 曲线表示(填序号)。
(4)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图所示,向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应。在此实验过程中,小球将 。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
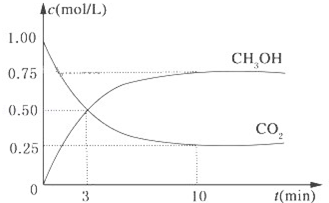 降低大气中CO2的含量及有效地开发利用 CO2,目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.测得CO2和CH3OH(g)的浓度随时间变化如图所示.
降低大气中CO2的含量及有效地开发利用 CO2,目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.测得CO2和CH3OH(g)的浓度随时间变化如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
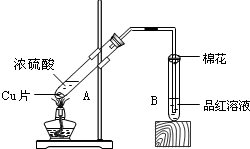 某校化学组的同学用如图装置对铜与浓硫酸在一定条件下的反应进行实验探究,请回答:
某校化学组的同学用如图装置对铜与浓硫酸在一定条件下的反应进行实验探究,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | 25℃~550℃~600℃~700℃ |
| 主要成分 | WO3 W2O5 WO2 W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜与浓硫酸反应生成的白色固体是CuSO4 | |
| B. | ①中灰白色固体不可能含有CuO | |
| C. | ②中的黑色固体可能含有CuS或Cu2S | |
| D. | ④中所得的白色沉淀是BaSO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
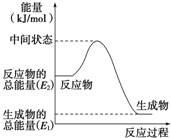 甲醇是人们开发和利用的一种新能源.已知:
甲醇是人们开发和利用的一种新能源.已知:查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高一9月月考化学卷(解析版) 题型:选择题
如图为反应Fe + CuSO4 === FeSO4 + Cu中电子转移的关系图,则图中的元素甲、乙分别表示
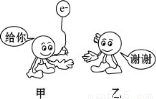
A.Fe Cu
B.Cu S
C.Fe O
D.Fe S
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com