
氟是自然界中广泛分布的元素之一。由于氟的特殊化学性质,它和其他卤素在单质及化合物的制备与性质上存在较明显的差异。
Ⅰ.化学家研究发现,SbF5能将MnF4从离子[MnF6]2-的盐中反应得到,SbF5转化成稳定离子[SbF6]-的盐。而MnF4很不稳定,受热易分解为MnF3和F2。根据以上研究写出以K2MnF6和SbF5为原料,在 423 K 的温度下制备F2的化学方程式:_________________________。
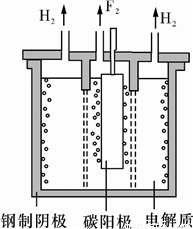
现代工业以电解熔融的氟氢化钾(KHF2)和氟化氢(HF)混合物制备氟单质,电解制氟装置如图所示。
已知KHF2是一种酸式盐,写出阴极上发生的电极反应式________________________。电解制氟时,要用镍铜合金隔板将两种气体产物严格分开的原因是___________。
Ⅱ.①卤化氢的熔沸点随相对分子质量增加而升高,而HF熔沸点高于HCl的原因是________________________。HF的水溶液是氢氟酸,能用于蚀刻玻璃,其化学反应方程式为:________________________
②已知25 ℃时,氢氟酸(HF)的电离平衡常数Ka=3.6×10-4。
某pH=2的氢氟酸溶液,由水电离出的c(H+)=___________mol/L;若将0.01 mol/L HF溶液与pH=12的NaOH溶液等体积混合,则溶液中离子浓度大小关系为:________________________。
③又已知25 ℃时,溶度积常数Ksp(CaF2)=1.46×10-10。现向1 L 0.2 mol/L HF溶液中加入 1 L 0.2 mol/L CaCl2 溶液,通过列式计算说明是否有沉淀产生:______________________
科目:高中化学 来源:2016-2017学年江苏省高一下学期第一次(3月)阶段检测化学试卷(解析版) 题型:选择题
下列有关物质的性质或应用均正确的是( )
A. 工业上分别用电解氧化镁和氧化铝的方法制备镁和铝
B. 铁具有良好的导电性,氯碱工业中可用铁作阳极电解食盐水
C. 电镀银时可选择银接电源正极,镀件接电源的负极
D. 电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高二开学质检(3月)化学试卷(解析版) 题型:选择题
对于可逆反应:2A(g)+B(g) 2C(g)ΔH<0,下列各图正确的是( )
2C(g)ΔH<0,下列各图正确的是( )
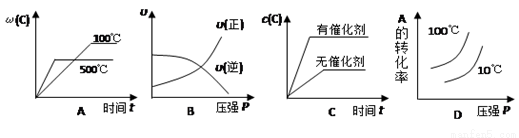
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高一(3月)开学质检化学试卷(解析版) 题型:选择题
宋代著名法医学家宋慈的《洗冤集录》中有一银针验毒的记载,“银针验毒”的原理是4Ag + 2H2S + O2 = 2X + 2H2O,下列说法正确的是
A.X的化学式为AgS B.银针验毒时,空气中氧气失去电子
C.反应中Ag和H2S均是还原剂 D.每生成1mo1X,反应转移2mo1e-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高一(3月)开学质检化学试卷(解析版) 题型:选择题
下列现象或新技术应用中,不涉及胶体性质的是( )
A.在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀
B.使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血
C.清晨,茂密的树林中,常常可以看到从枝叶间透过一道道光柱
D.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三3月联考理科综合化学试卷(解析版) 题型:选择题
某课外兴趣小组进行电解原理的实验探究,做了如下的实验:以铜为电极,按如图所示的装置电解饱和食盐水。
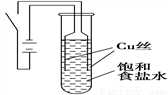
实验现象:接通电源30 s内,阳极附近出现白色浑浊,之后变成橙黄色浑浊,此时测定溶液的pH约为10。一段时间后,试管底部聚集大量红色沉淀,溶液仍为无色。
查阅资料:
物质 | 氯化铜 | 氧化亚铜 | 氢氧化亚铜(不稳定) | 氯化亚铜 |
颜色 | 固体呈棕色,浓溶液呈绿色,稀溶液呈蓝色 | 红色 | 橙黄色 | 白色 |
※ 相同温度下CuCl的溶解度大于CuOH。
下列说法错误的是( )
A. 反应结束后最终溶液呈碱性 B. 阴极上发生的电极反应为:2H2O + 2e- == H2↑+ 2OH-
C. 电解过程中氯离子移向阳极 D. 试管底部红色的固体具有还原性
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省鞍山市高三3月月考理科综合化学试卷(解析版) 题型:简答题
工业上用矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)获取铜和胆矾的操作流程如下:
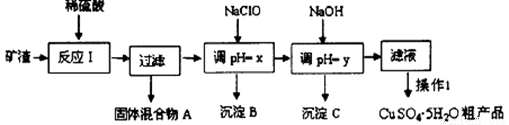
已知:①部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 5.4 | 4.0 | 1.1 | 5.8 |
沉淀完全pH | 6.7 | 5.2 | 3.2 | 8.8 |
②B、C均为单一沉淀
请回答下列问题:
(1)已知Cu2O在酸性条件下发生自身氧化还原反应,写出离子反应方程式______________。
(2)为了加快反应I的速率,可以采取的措施是______________(写1点)。
(3)固体混合物A中的成分是__________________________。
(4)反应I完成后,铁元素的存在形式为_______________(填离子符号);写出生成该离子的离子方程式___________________________________。
(5)x对应的数值范围是_______________________。用NaClO调pH,生成沉淀B的反应的离子方程式为____________________________________。
(6)已知:Ksp[Al(OH)3]=1.1×10-33,当调节溶液的pH为5时,c(Al3+)=_________ mol•L-1
(7)洗涤CuSO4·5H2O粗产品不能用大量水洗,而用冰水洗涤.原因是___________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一下学期第一次月考化学试卷(解析版) 题型:选择题
在N2+3H2 2NH3的可逆反应中,自反应开始至2s末,氨的浓度由0变为0.4mol•L-1,则以氢气的浓度变化表示该反应在2 s内的平均反应速率是
2NH3的可逆反应中,自反应开始至2s末,氨的浓度由0变为0.4mol•L-1,则以氢气的浓度变化表示该反应在2 s内的平均反应速率是
A.0.3 mol•L-1•s-1 B.0.4 mol•L-1•s-1 C.0.6 mol•L-1•s-1 D.0.8 mol•L-1•s-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二3月月考化学试卷(解析版) 题型:选择题
如图所示,各烧杯中盛有海水,铁在其中被腐蚀的速度由快到慢的顺序为
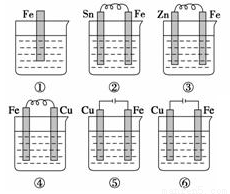
A. ②①③④⑤⑥ B. ⑤④②①③⑥ C. ⑤②④①③⑥ D. ⑤③②④①⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com