
| A、植物油的不饱和程度高于动物油,植物油更易氧化变质 |
| B、除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤、分液 |
| C、过氧化钠中含有离子键和非极性共价键,阴离子与阳离子的物质的量之比为1:1 |
| D、向某溶液中滴入稀盐酸产生使澄清石灰水变浑浊的气体,该溶液不一定含有CO32- |
 ,阴离子为过氧根离子;
,阴离子为过氧根离子; ,阴、阳离子的个数比为1:2,故C错误;
,阴、阳离子的个数比为1:2,故C错误;

科目:高中化学 来源:2014-2015学年内蒙古巴彦淖尔市高三上学期期中考试化学试卷(解析版) 题型:选择题
将1mol NaHCO3和1mol Na2O2固体混合,在加热的条件理使其充分反应,则最后所得固体为
 A.1mol Na2CO3和1mol NaOH B.lmol Na2CO3和2molNaOH
A.1mol Na2CO3和1mol NaOH B.lmol Na2CO3和2molNaOH
C.2mol Na2CO3和2molNaOH D.2mol Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
 的表述不正确的是( )
的表述不正确的是( )| A、该物质能发生加成、取代、氧化反应 |
| B、该物质遇FeC13溶液显色,lmol该物质能与2mo1Br2发生取代反应 |
| C、该物质的分子式为C11H15O3 |
| D、1mol该物质最多消耗Na,NaOH,NaHC03的物质的量之比为2:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
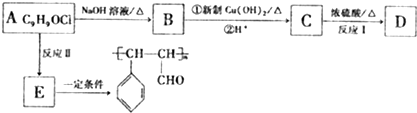
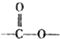 结构的芳香族化介物的同分异构体有
结构的芳香族化介物的同分异构体有查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除去NO中混有的NO2将混合气体先通过足量水,然后用CaCl2干燥 |
| B、配制一定物质的量浓度的Fe(NO3)2溶液:将一定量的Fe(NO3)2溶于适量的硝酸中,再加入水稀释至指定浓度 |
| C、向足量饱和石灰水中加入少CaO,恢复至室温后溶液pH变大 |
| D、工业上分別用电解熔融Al2O3、MgO、NaCl的方法制取Al、Mg、Na |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (l)+H2(g)→
(l)+H2(g)→ (l)△H>0 ①
(l)△H>0 ① (l)+2H2(g)→
(l)+2H2(g)→ (l)△H<0 ②
(l)△H<0 ②| A、反应①、②都属于加成反应 |
| B、l,3一环己二烯比苯稳定 |
| C、反应①、②的热效应说明苯环中含有的并不是碳碳双键 |
| D、反应①、②中的所有有机物均可使溴水褪色,但褪色原理不完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H+) |
| c(OH-) |
| c(H+) |
| c(HA) |
| c(HA) |
| c(A) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| CuO |
| CeO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com