
【题目】目前世界上60%的镁是从海水中提取的,下图是某工厂从海水中提取镁的主要步骤。学生就这个课题展开了讨论。
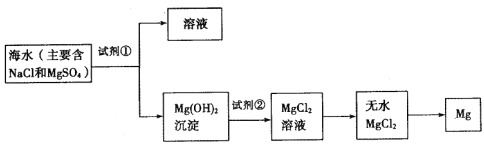
学生就这个课题提出了以下问题:
(一)在海水提镁的过程中如何实现对镁离子的富集,有三个学生提出自己的观点。
学生甲的观点:直接往海水中加入沉淀剂。
学生乙的观点:高温加热蒸发海水后,再加入沉淀剂。
学生丙的观点:利用晒盐后的苦卤水,再加入沉淀剂。
通过分析比较你认为学生_______的观点正确(填学生序号),简述理由:______________________。
(二)在海水提镁的过程中如何实现对镁离子的分离?
(1)为了使镁离子沉淀下来,并充分利用当地的贝壳(主要成分为碳酸钙)资源,加入的足量试剂①是___________(填化学式)。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是_________(填标号字母)
A.蒸馏 B.过滤 C.萃取 D.分液
(3)加入的足量试剂②是______________________(填化学式)。
(4)写出由无水MgCl2制取金属镁的化学方程式________________。
【答案】丙 镁离子富集浓度高;能源消耗小,成本低 Ca(OH)2(或CaO) B HCl MgCl2![]() Mg+Cl2↑
Mg+Cl2↑
【解析】
从含有NaCl和MgCl2的溶液中加入碱,使得Mg2+沉淀生成Mg(OH)2,Mg(OH)2加入盐酸得到MgCl2溶液,最后得到MgCl2固体,电解熔融的MgCl2得到Mg单质。
(一)镁离子的富集过程中,学生甲和学生乙的观点能源消耗大,成本高,学生丙的观点更为合理;
(二) (1)充分利用当地的贝壳(主要成分为碳酸钙)资源,碳酸钙高温分解成CaO,CaO与水作用得Ca(OH)2,使镁离子沉淀下来,可以选择Ca(OH)2或CaO;
(2)加入试剂①后,得到Mg(OH)2沉淀,可以采用过滤的方法分离,故选B;
(3)加入试剂②,将氢氧化镁转化为氯化镁,故试剂②为HCl;
(4)制取金属镁采用电解的方法,其反应方程式为:MgCl2 ![]() Mg+Cl2↑;
Mg+Cl2↑;


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】下列有关氨和铵盐说法正确的是( )

A. 氨和铵盐都易溶于水,都能生成NH![]()
B. 铵盐都能与碱反应,不能与酸反应
C. 实验室制备氨气可用如图所示试剂和装置
D. 铵盐受热分解都能产生氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是一种有机光电材料中间体。由A制备G的一种合成路线如下:
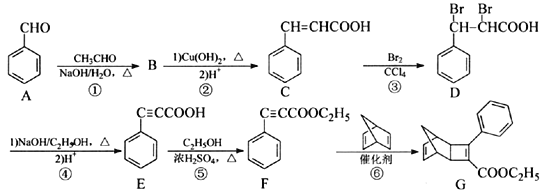
回答下列问题:
(1)F中的官能团名称为______。
(2)B的分子式为C9H8O,写出B的结构简式:______。
(3)反应②~⑥中属于取代反应的是______(填序号)。
(4)写出同时满足下列条件的C的一种同分异构体的结构简式:______。
Ⅰ.能发生银镜反应; Ⅱ.分子中含有苯环且有4种不同化学环境的氢。
(5)请写出以![]() 和CH3C≡CH为原料制备
和CH3C≡CH为原料制备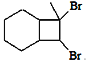 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)______。
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人类研究氢能源从未间断过,而热化学循环分解水制 H2是在水反应体系中加入一种中间物,经历不同的反应阶段,最终将水分解为H2和O2,这是一种节约能源、节省反应物料的技术,下图是热化学循环制氢气的流程:
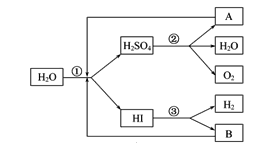
(1)实验测得,1 g H2燃烧生成液态水放出142.9 kJ的热量,则表示氢气燃烧热的热化学方程式为_______。
(2)整个流程参与循环的物质是________和________(填化学式),最难进行的反应是____________(填序号)。
(3)汞虽然有毒,但用途广泛。用汞和溴化钙作催化剂,可以在较低温度下经过下列反应使水分解制氢气和氧气:①CaBr2+2H2O=Ca(OH)2+2HBr↑;②……③HgBr2+Ca(OH)2=CaBr2+HgO+H2O;④2HgO=2Hg+O2↑。反应②的化学方程式为________________________。
(4)合成氨用的H2可以甲烷为原料制得。有关化学反应的能量变化如图所示,则CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为___________。
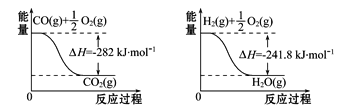
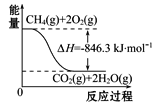
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4NH3+5O2![]() 4NO+6H2O在一定体积的密闭容器中进行,30 s后NO的物质的量浓度增加了3 mol/L,则下列反应速率正确的是( )
4NO+6H2O在一定体积的密闭容器中进行,30 s后NO的物质的量浓度增加了3 mol/L,则下列反应速率正确的是( )
A. v(NO)=0.1 mol·(L·s)-1 B. v(NO)=0.02 mol·(L·s)-1
C. v(NH3)=0.01 mol·(L·s)-1 D. v(NH3)=0.2 mol·(L·s)-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应①CO(g)+CuO(s)![]() CO2(g)+Cu(s)和反应②H2(g)+CuO(s)
CO2(g)+Cu(s)和反应②H2(g)+CuO(s)![]() Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③CO(g)+H2O(g)
Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
A. 反应①的平衡常数K1=c(CO2).c(Cu)/c(CO).c(CuO)
B. 反应③的平衡常数K=K1/K2
C. 对于反应③,恒容时,温度升高,H2浓度减小,则该反应的焓变为正值
D. 对于反应③,恒温恒容下,增大压强,H2浓度一定减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着环境污染的加重和人们环保意识的加强,生物降解材料逐渐受到了人们的关注。以下是PBA (—种生物降解聚酯高分子材料)的合成路线:

己知:①烃A的相对分子质量为84,核磁共振氢谱显示只有1组峰,不能使溴的四氯化碳溶液褪色。
②化合物C中只含一个官能团。
③R1CH=CHR2![]() R1COOH+R2COOH
R1COOH+R2COOH
④
(1)由A生成B的反应类型为_________。
(2)由B生成C的化学方程式为__________。
(3)E的结构简式为______________________。
(4)F的名称为______________(用系统命名法);由D和生成PBA的化学方程式为_______________;若PBA的平均聚合度为70,则其平均相对分子质量为___________。
(5)E的同分异构体中能同时满足下列条件的共有_____种(不含立体异构)。
①链状化合物 ②能发生银镜反应 ③氧原子不与碳碳双键直接相连
其中,核磁共振氢谱显示为2组峰,且峰面积比为2:1的是_________(写结构简式)。
(6)若由1.3—丁二烯为原料(其他无机试剂任选)通过三步制备化合物F,其合成路线为:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.100 0 mol·L-1的盐酸滴定20.00 mL未知浓度的氨水,滴定曲线如图所示,滴加20.00 mL盐酸时所得溶液中c(Cl-)=c(NH4+)+c(NH3·H2O)+c(NH3)。下列说法错误的是

A. 该氨水的浓度为0.100 0 mol·L-1
B. 点①溶液中c(NH4+)+c(NH3·H2O)+c(NH3)=2c(Cl-)
C. 点②溶液中c(NH4+)=c(Cl-)
D. 点③溶液中c(Cl-)>c(H+)>c(NH4+)>c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com