
设nA为阿伏加德罗常数的数值,下列说法正确的是( )
A.常温常压下,8 g O2含有4nA个电子
B.1 L 0.1 mol·L-1的氨水中有nA个NH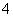
C.标准状况下,22.4 L盐酸含有nA个HCl分子
D.1 mol Na被完全氧化生成Na2O2,失去2nA个电子
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列关于氢氧化铁胶体的叙述,正确的是
A.往氢氧化铁胶体中逐滴加入稀盐酸先出现沉淀后沉淀溶解
B.在含2 mol的氢氧化铁的胶体中含有氢氧化铁胶粒数为2NA
C. 滤纸可将氢氧化铁胶体中的分散质与分散剂分离
D. 氢氧化铁胶体带正电荷
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,正确的是( )
A.同主族金属的原子半径越大,熔点越高
B.稀有气体原子序数越大,沸点越低
C.分子间作用力越弱,该物质的熔点越低
D.同周期元素的原子半径越小,越易失去电子
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D是元素周期表中的四种短周期元素。
| 元素 | 性质或结构信息 |
| A | 单质制成的高压灯,发出的黄光透雾力强、射程远、且其单质燃烧后生成淡黄色固体 |
| B | 工业上通过分离液态空气获得其单质。原子的最外层电子数是其内层电子总数的2.5倍 |
| C | 单质是双原子分子,常温、常压下是淡黄绿色气体,原子的L层再增加1个电子即达到8电子稳定结构 |
| D | +2价阳离子的核外电子排布与氖原子相同 |
请根据表中信息回答下列问题:
(1)表中与元素A属于同一周期的元素是________(填字母),写出其离子的结构示意图________。
(2)已知C单质能与H2O发生置换反应生成O2,写出C单质与水反应的化学方程式__________________。
(3)对元素B的单质或化合物描述正确的是________。
a.元素B的最高正化合价为+6
b.常温常压下,其单质难溶于水
c.单质分子中含有18个电子
d.在一定条件下,氢气能与B单质反应
(4)A和D两种元素中活动性较强的是________(填元素符号),判断依据是________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
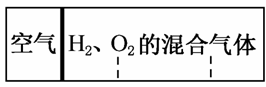
(2012·安徽联考)如图所示,分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容积的1/4)、H2和O2的混合气体,在标准状况下,若将H2、O2的混合气体点燃引爆。活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来H2、O2的体积之比可能为( )
A.2:7 B.5:4
C.2:1 D.7:2
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.1 molCl2与足量Fe反应转移电子数一定为3NA
B.标准状况下,2.24 L NH3中含有共价 键的数目为NA
键的数目为NA
C.1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA
D.标况下,11.2 L SO3所含的分子数目为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
可以说明乙酸是弱酸的事实是
A.乙酸不能使酚酞溶液变红色 B.0.1 mol•L﹣1的乙酸溶液pH>1
C.乙酸能使紫色石蕊试液变红色 D.乙酸和Na2CO3反应可放出CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com