
【题目】下列离子方程式书写正确的是
A.向明矾溶液中滴加Ba(OH)2溶液,使沉淀质量达到最大值:2Al3++3![]() +3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
B.将少量氯化铁溶液滴入硫化钠溶液中:2Fe3++S2-=2Fe2++S↓
C.向Fe(NO3)3溶液中加入过量的HI溶液:2![]() +8H++6I-=3I2+2NO↑+4H2O
+8H++6I-=3I2+2NO↑+4H2O
D.1mol·L-1的NaAlO2溶液和2.5mol·L-1的HCl等体积混合:2![]() +5H+=Al(OH)3↓+Al3++H2O
+5H+=Al(OH)3↓+Al3++H2O
【答案】D
【解析】
A.向明矾溶液中滴加Ba(OH)2溶液,使沉淀质量达到最大值,明矾组成为KAl(SO4)2·12H2O,假设明矾的物质的量为1mol,则n(Al3+)=1mol,n(SO42-)=2mol,滴加Ba(OH)2使Al3+沉淀完全,则产生1molAl(OH)3和1.5molBaSO4沉淀,沉淀的总质量为m1=78g/mol×1mol+233g/mol×1.5mol=427.5g;滴加Ba(OH)2使SO42-沉淀完全,根据量的关系,Al3+全转化为AlO2-,沉淀只有2molBaSO4,沉淀的总质量m2=233g/mol×2mol=466g,m2>m1,其离子方程式为:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O,故A错误;
B.将少量氯化铁溶液滴入硫化钠溶液中,由于铁离子的氧化性和硫离子的还原性,二者会发生氧化还原反应,生成Fe2+和S,由于S2-过量,则Fe2+与S2-结合成FeS沉淀,离子方程式为:2Fe3++3S2-=2FeS↓+S↓,故B错误;
C.Fe(NO3)3溶液中加入过量的HI溶液,铁离子和硝酸根离子都参与氧化还原反应,正确的离子方程式为:Fe3++3NO3-+12H++10I-=Fe2++5I2+3NO↑+6H2O,故C错误;
D.1mol/L的NaAlO2溶液和2.5mol/L的HCl溶液等体积互相均匀混合,设溶液体积为1L,偏铝酸钠的物质的量为1mol,HCl的物质的量为2.5mol,1mol偏铝酸钠消耗1molHCl生成1mol氢氧化铝,剩余的1.5molHCl能够溶解0.5mol氢氧化铝,反应的离子方程式为:2AlO2-+5H+═Al3++Al(OH)3↓+H2O,故D正确;
答案为D。


科目:高中化学 来源: 题型:
【题目】I.现有下列物质:
①HNO3②冰醋酸③氨水④Al(OH)3⑤NaHCO3(s)⑥Cu⑦氯水⑧CaCO3⑨H2CO3⑩盐酸
(1)上述物质中属于强电解质的有__________(填序号),属于弱电解质的有__________(填序号)。
(2)写出下列物质的电离方程式:④__________;⑤__________;⑨__________。
Ⅱ.少量铁粉与100mL0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,可以使用如下方法中的__________(填序号)。
①加H2O②加NaOH固体③滴入几滴浓盐酸④加CH3COONa固体⑤加NaCl溶液⑥滴入几滴硫酸铜溶液⑦升高温度(不考虑盐酸挥发)⑧改用10mL0.1mol/L盐酸.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在研究金矿床物质组分的过程中,通过分析发现了![]() 多金属互化物.
多金属互化物.
![]() 某金属互化物属于晶体,区别晶体和非晶体可通过 ______ 方法鉴别.该金属互化物原子在三维空间里呈周期性有序排列,即晶体具有 ______ 性.
某金属互化物属于晶体,区别晶体和非晶体可通过 ______ 方法鉴别.该金属互化物原子在三维空间里呈周期性有序排列,即晶体具有 ______ 性.
![]() 基态
基态![]() 的核外电子排布式 ______ ;配合物
的核外电子排布式 ______ ;配合物![]() 常温下为液态,易溶于
常温下为液态,易溶于![]() 、苯等有机溶剂.固态
、苯等有机溶剂.固态![]() 属于 ______ 晶体.
属于 ______ 晶体.
![]() 铜能与类卤素
铜能与类卤素![]() 反应生成
反应生成![]() 分子中含有
分子中含有![]() 键的数目为 ______ ;
键的数目为 ______ ;
类卤素![]() 对应的酸有两种,理论上硫氰酸
对应的酸有两种,理论上硫氰酸![]() 的沸点低于异硫氰酸
的沸点低于异硫氰酸![]() 的沸点,其原因是 ______ ;
的沸点,其原因是 ______ ;
![]() 立方
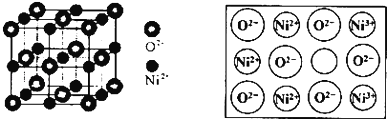
立方![]() 氧化镍
氧化镍![]() 晶体的结构如图所示,其晶胞边长为apm,列式表示NiO晶体的密度为 ______
晶体的结构如图所示,其晶胞边长为apm,列式表示NiO晶体的密度为 ______ ![]() 不必计算出结果,阿伏加德罗常数的值为
不必计算出结果,阿伏加德罗常数的值为![]() 人工制备的NiO晶体中常存在缺陷
人工制备的NiO晶体中常存在缺陷![]() 如图 一个
如图 一个![]() 空缺,另有两个
空缺,另有两个![]() 被两个
被两个![]() 所取代,其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化.已知某氧化镍样品组成
所取代,其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化.已知某氧化镍样品组成![]() ,该晶体中
,该晶体中![]() 与
与![]() 的离子个数之比为 ______ .
的离子个数之比为 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】太阳能电池的发展已经进入了第三代。第三代就是铜铟镓硒CIGS等化合物薄膜太阳能电池以及薄膜硅系太阳能电池。完成下列填空:
(1)亚铜离子(Cu+)基态时的电子排布式为____________;
(2)硒为第四周期元素,相邻的元素有砷和溴,则这3种元素的第一电离能I1从大到小顺序为(用元素符号表示)_______________________________;用原子结构观点加以解释_________________________。
(3)与镓元素处于同一主族的硼元素具有缺电子性(价电子数少于价层轨道数),其化合物可与具 有孤对电子的分子或离子生成加合物,如BF3能与NH3反应生成BF3NH3 。BF3NH3中B原子的杂化轨道类型为__________,N原子的杂化轨道类型为 ______________ ,B与 N之间形成 __________________ 键。
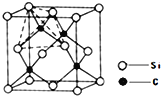
(4)单晶硅的结构与金刚石结构相似,若将金刚石晶体中一半的C原子换成Si原子且同种原子不成键,则得如图所示的金刚砂(SiC)结构;金刚砂晶体属于____________(填晶体类型)在SiC结构中,每个C原子周围最近的C原子数目为 ______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇又称“木醇”,是无色有酒精气味易挥发的有毒液体。甲醇是重要的化学工业基础原料和液体燃料,可用于制造甲醛和农药,并常用作有机物的萃取剂和酒精的变性剂等。
(1)工业上可利用CO2和H2生产甲醇,方程式如下:
CO2(g)+3H2(g)![]() CH3OH(l)+H2O (g) △H=Q1kJ·mol-1
CH3OH(l)+H2O (g) △H=Q1kJ·mol-1
又查资料得知:①CH3OH(l)+1/2 O2(g)![]() CO2(g)+2H2(g) △H=Q2kJ·mol-1
CO2(g)+2H2(g) △H=Q2kJ·mol-1
②H2O(g)=H2O(l) △H= Q3kJ·mol-1,则表示甲醇的燃烧热的热化学方程式为______。
某同学设计了一个甲醇燃料电池,并用该电池电解200mL一定浓度的NaCl与CuSO4混合溶液,其装置如图:
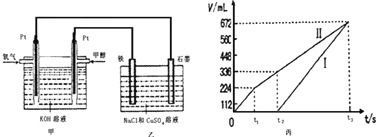
(2)为除去饱和食盐水中的铵根离子,可在碱性条件下通入氯气,反应生成氮气。该反应的离子方程式为___________________________________。
(3)过量氯气用Na2S2O3除去,反应中S2O32-被氧化为SO42-。若过量的氯气为1×10-3mol,则理论上生成的SO42-为_____________mol。
(4)写出甲中通入甲醇这一极的电极反应式______________________。
(5)理论上乙中两极所得气体的体积随时间变化的关系如丙图所示(已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式____________,原混合溶液中 NaCl的物质的量浓度为___________mol/L。(设溶液体积不变)
(6)当向上述甲装置中通入标况下的氧气336mL时,理论上在铁电极上可析出铜的质量为_____________g。
(7)若使上述电解装置的电流强度达到5.0A,理论上每分钟应向负极通入气体的质量为_____________克。(已知1个电子所带电量为1.6×10-19C,计算结果保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A. 使酚酞变红色的溶液中:Na+、Al3+、SO42-、Cl-
B. ![]() =1×10-13mol·L-1的溶液中:NH4+、Ca2+、Cl-、NO3-
=1×10-13mol·L-1的溶液中:NH4+、Ca2+、Cl-、NO3-
C. 与Al反应能放出H2的溶液中:Fe2+、K+、NO3-、SO42-
D. 水电离的c(H+)=1×10-13mol·L-1的溶液中:K+、Na+、AlO2-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知难溶性物质K2SO4·MgSO4·2CaSO4在水中存在如下平衡:K2SO4·MgSO4·2CaSO4 (s)![]() 2Ca2++2K++Mg2++4SO42-。不同温度下,K+的浸出浓度与溶浸时间的关系如图所示,则下列说法错误的是
2Ca2++2K++Mg2++4SO42-。不同温度下,K+的浸出浓度与溶浸时间的关系如图所示,则下列说法错误的是

A.该平衡的Ksp=c2(Ca2+)·c2(K+)·c(Mg2+)·c4(SO42-)B.向该体系中加入饱和K2SO4溶液,溶解平衡向左移动 C.升高温度,溶浸速率增大,平衡向正反应方向移动 D.向该体系中加入饱和NaOH溶液,溶解平衡不发生移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定环境中能大量共存的是( )
A.在 =1013的溶液中:NH4+、Ca2+、Cl-、K+
=1013的溶液中:NH4+、Ca2+、Cl-、K+
B.由水电离出的c(H+)=1×10-13mol/L的溶液中:Na+、HCO3-、Cl-、K+
C.无色溶液中可能大量存在Al3+、NH4+、Cl-、S2-
D.中性溶液中可能大量存在Fe3+、K+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的若干种,离子浓度都为
中的若干种,离子浓度都为![]() 往该溶液中加入过量的
往该溶液中加入过量的![]() 和盐酸的混合溶液,无白色沉淀生成。某同学另取少量原溶液,设计并完成如下实验:
和盐酸的混合溶液,无白色沉淀生成。某同学另取少量原溶液,设计并完成如下实验:

则关于原溶液的判断中正确的是![]()
A.无法确定原溶液中是否存在![]()
B.肯定存在的离子是![]() 、
、![]() ,是否存在
,是否存在![]() 、
、![]() 需要通过焰色反应来确定
需要通过焰色反应来确定
C.肯定不存在的离子是![]() 、
、![]() 、
、![]() ,是否含
,是否含![]() 另需实验验证
另需实验验证
D.若步骤中![]() 和
和![]() 溶液改用
溶液改用![]() 和盐酸的混合溶液,则对溶液中离子的判断无影响
和盐酸的混合溶液,则对溶液中离子的判断无影响
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com