
【题目】下列描述中,不符合生产实际的是( )
A. 电解MgCl2溶液获取金属镁,用石墨作阳极
B. 电解法精炼粗铜,用纯铜作阴极
C. 电解饱和食盐水制烧碱,用涂镍碳钢网作阴极
D. 在镀件上电镀锌,用锌作阳极
科目:高中化学 来源: 题型:
【题目】已知常温时HClO的Ka=3.0×10-8,HF的Kb=3.5×10-4。现将pH和体积都相同的次氯酸和氢氟酸溶液分別加蒸馏水稀释,pH随溶液体积的变化如图所示,下列叙述正确的是( )
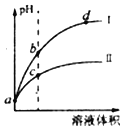
A. 曲线Ⅰ为次氯酸稀释时pH变化曲线
B. 取a点的两种酸溶液,中和相同体积、相同浓度的NaOH溶液,消耗氢氟酸的体积较小
C. b点溶液中水的电离程度比c点溶液中水的电离程度小
D. 从b点到d点,溶液中![]() 保持不变(HR代表HClO或HF)
保持不变(HR代表HClO或HF)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液中有0.2mol XO4﹣ , 加入0.3mol Na2SO3恰好反应,已知Na2SO3被氧化成Na2SO4 , 则还原产物中X的化合价为( )
A.0
B.+1
C.+3
D.+4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,可逆反应A+B![]() mC变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,问:
mC变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,问:
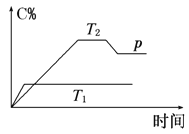
(1)温度T1________T2(填“大于”“等于”或“小于”)。
(2)正反应是________反应(填“吸热”或“放热”)。
(3)如果A、B、C均为气体,则m________2(填“大于”“等于”或“小于”)。
(4)当温度和容积不变时,如在平衡体系中加入一定量的某稀有气体,则体系的压强________(填“增大”“减小”或“不变”),平衡___ _____移动(填“向正反应方向”“向逆反应方向”或“不”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钻(Co)及其化合物在工业上有广泛应用。为从某工业废料中回收钴,某学生设计流程如图(废料中含有Al、Li、Co2O3和Fe2O3等物质)。
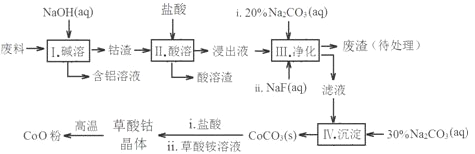
已知:LiF难溶于水,Li2CO3微溶于水。
请回答:
(1)写出I中发生反应的化学方程式并用单线桥标记电子转移的方向和数目________。
(2)写出步骤中Co2O3与盐酸反应生成Cl2的离子方程式_______________。
(3)步骤II所得废渣的主要成分除了LiF外,还有________________。
(4)NaF与溶液中的Li+形成LiF沉淀,此反应对步骤IV所起的作用是___________。
(5)在空气中加热10.98g草酸钴晶体(CoC2O42H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表。己知:M(CoC2O42H2O)=183g/mol。
温度范围/℃ | 固体质量/g |
150--210 | 8.82 |
290--320 | 4.82 |
890--920 | 4.5 |
经测定,加热到210℃时,固体物质的化学式为_____。加热到210--290℃过程中产生的气体只有CO2,此过程发生反应的化学方程式是_________。温度高于890℃时,固体产物发生分解反应,固体产物为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关离子方程式或离子共存的叙述正确的是
A. 用肥皂(主要成份C17H35COONa)水检验含有较多钙离子的硬水:2C17H35COO-+Ca2+===(C17H35COO)2Ca↓
B. 将磁性氧化铁溶于氢碘酸:Fe3O4+8H+=2Fe3++Fe2++4H2O
C. 常温下,在![]() =0.1的溶液中:Na+、K+、SO42-、HCO3-能大量共存
=0.1的溶液中:Na+、K+、SO42-、HCO3-能大量共存
D. 在NaC1O溶液中:SO32-、OH-、C1-、K+能大量共存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解精炼铜的阳极泥主要成分为Cu2Te、Ag2Se,工业上从其中回收硒(Se)、碲(Te)的一种工艺流程如下:
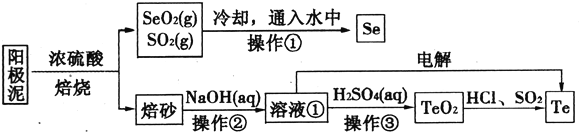
已知:I.TeO2是两性氧化物、微溶于水;
Ⅱ.元素碲在溶液中主要以Te4+、TeO32-、HTeO3-等形式存在;
Ⅲ.25℃时,亚碲酸(H2TeO3)的Ka1=1×10-3,Ka2=2×10-8。
(1)NaHTeO3的溶液的pH____7(填“>”、“=”或“<”)。
(2)SeO2与SO2通入水中反应的化学方程式为________。操作①的名称为__________。
(3)焙砂中碲以TeO2形式存在。溶液①中的溶质主要成分为NaOH、_______。工业上通过电解溶液①也可得到单质碲。已知电极均为石墨,则阴极的电极反应式为____________。
(4)向溶液①中加入硫酸,控制溶液的pH为4.5~5.0,生成TeO2沉淀。如果H2SO4过量,将导致碲的回收率偏低,其原因是________________________。
(5)将纯净的TeO2先溶于盐酸得到四氯化碲溶液,然后将SO2通入到溶液中得到Te单质。由四氯化碲得到Te单质的离子方程式为__________________。
(6)上述流程中可循环利用的物质有__________________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由CO、H2和O2组成的混和气体60mL,在一定条件下恰好完全反应,测得生成物在101kPa120℃下对氢气的相对密度为18.75,则原混和气体中H2所占的体积分数为( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是原子序数依次增大的五种短周期主族元素,其中A的原子序数是B和D原子序数之和的1/4,C元素的最高价氧化物的水化物是一种中强碱,甲和丙是D元素的两种常见氧化物,乙和丁是B元素的两种常见同素异形体,0.005mol/L戊溶液的pH=2,它们之间的转化关系如图所示(部分反应物省略),下列叙述正确的是( )
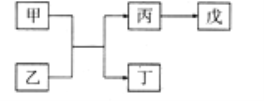
A. C、D两元素形成化合物属共价化合物
B. C、D的简单离子均能促进水的电离
C. A、D分别与B元素形成的化合物都是大气污染物
D. E的氧化物水化物的酸性大于D的氧化物水化物的酸性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com