
【题目】加碘盐的主要成分是NaCl,还添加了适量的KIO3,下列说法中正确的是
A. KIO3和NaCl为离子化合物,均只含离子健
B. KIO3中阳离子的结构示意图为
C. KIO3只有氧化性,无还原性
D. 23Na37Cl中质子数和中子数之比是7:8
科目:高中化学 来源: 题型:
【题目】I.把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用下图所示的坐标曲线来表示。

请回答下列问题。
(1)曲线由O→a段不产生氢气的原因是____________________。
有关反应的化学方程式为_________________________。
(2)曲线由a→c段,产生氢气的速率增加较快的主要原因是_______________________________。
(3)曲线由c以后产生氢气的速率逐渐下降的主要原因是_______________________________。
II.某同学在用稀硫酸与锌反应制取氢气的实验中,发现加入少量硫酸铜溶液可以加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有:______________、_________________;
(2) 硫酸铜溶液可以加快氢气生成速率的原因:__________________;
(3) 实验中现有Na2SO4、MgSO4、 Ag2SO4、 K2SO4四种溶液,可与上述实验中CuSO4溶液起相似作用的是:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、W、D、E,Y为短周期元素,且原子序数依次增大,A是周期表中原子半径最小的,B的原子序数为7,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。Y是短周期中原子序数最大的主族元素。
(1)W2-离子的结构示意图为__________,E元素在周期表中的位置为_________,写出E的最高价氧化物的水化物与D的最高价氧化物的水化物反应的离子方程式_______________________________。
(2)A2W2的电子式为__________,在酸性条件下A2W2可以将Fe2+氧化成Fe3+,写出该反应的离子方程式__________________________________________。当消耗2mol A2W2时,转移的电子数为____________________。
(3)下列事实能说明Y元素的非金属性比硫(S)元素的非金属性强的是__________;
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4) 用电子式表示B的最简单氢化物的形成过程___________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面为元素周期表的一部分,根据元素① ~⑧在表中的位置回答下列问题
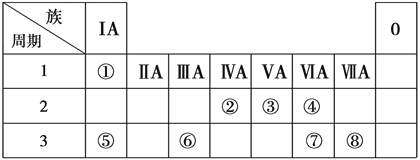
(1)元素④的原子结构示意图为___________,元素⑦在自然界的存在形态是__________
(2)用电子式表示元素⑤⑧形成化合物的过程_____________
(3)元素①③形成的最简单氢化物化学式是__________,写出实验室制备此物质的化学方程式___________
(4)元素⑥的单质与磁性氧化铁反应的化学方程式___________
(5)由元素②形成的只有三种同分异构体的烷烃是_________(填化学式),这三种同分异构体的结构简式分别是CH3CH2CH2CH2CH3______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 在标准状况下,22.4L水所含分子数目为NA
B. 11.2L HCl气体其物质的量为0.5mol
C. 9克Al转变成Al3+时,得到电子数目为NA
D. 常温时时28g氮气所含氮原子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某元素位于周期表的第三周期 VIIA 族,由此得出的推论错误的是
A.该元素原子核外有 3 个电子层
B.该元素最外层有 7 个电子
C.该元素容易失去电子
D.该元素容易得到电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚苹果酸(PMLA)可作为目的合成药物的载体,它的一种化学合成路线如下:
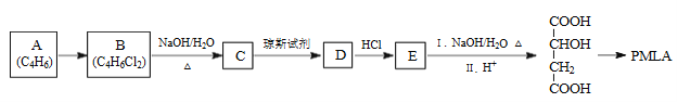
己知:琼斯试剂能选择性氧化含不饱和碳的醇,而醇中的碳碳双键或三键不受影响:
![]()
回答下列问题:
(1)A的化学名称是____________。
(2)C的结构简式是____________, D生成E的反应类型是____________。
(3)E中官能团的名称是____________。在浓硫酸和加热条件下,1mol苹果酸最多能与____________mol乙醇反应。
(4)聚酯PLMA有多种结构,其中一种的主链中有-CH2-,写出由苹果酸在一定条件下制取该种PMLA的化学方程式:_______________________。
(5)化合物F是B与氢气的加成产物,F的同分异构体共有____________种(不含立体异构,不包括F),写出其中一种核磁共振氢谱为2组峰的结构简式:____________。
(6)參照上述合成路线,以异戊二烯[CH2=C(CH3)CH=CH2]为原料(无机试剂任选)设计制备![]() 的合成路线:____________________。
的合成路线:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案中,能达到相应实验目的的是
选项 | 方案 | 目的 |
A |
| 验证氧化性::Cl2>Br2 |
B |
| 验证溶解度:AgCl>Ag2S |
C |
| 检验SO2、CO2混合气体中有CO2 |
D |
| 比较乙醇中羟基氢原子和水分子中氢原子的活泼性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途具有对应关系的是
A.SO2具有氧化性,可用于漂白纸浆
B.NH4HCO3受热易分解,可用作氮肥
C.明矾溶于水产生的硫酸根离子有氧化性,可用于净水
D.常温下铁能被浓硝酸钝化,可用铁质容器贮运浓硝酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com