
分析 (1)分析表明化合物甲中钙、氯元素的质量分数分别为52.36%、46.33%,还有一种元素,根据反应中元素守恒知,另一种元素为氢元素,则其钙原子、氯原子和氢原子个数之比=$\frac{52.36%}{40}$:$\frac{46.33}{35.5}$:$\frac{1-52.36%-46.33%}{1}$=1:1:1,化合物乙的水溶液显酸性,则为氯化氢;
(2)甲和水反应生成氢气,同时生成氯化钙、氢氧化钙;
(3)二氧化锰和浓盐酸之间加热反应可以生成氯化锰、水以及氯气,氯化亚铁易被氧化为氯化铁,并且易水解,据此回答;
(4)氯化钙发生化合反应生成CaCl,氯化钙作氧化剂,则钙作还原剂.
解答 解:(1)分析表明化合物甲中钙、氯元素的质量分数分别为52.36%、46.33%,还有一种元素,根据反应中元素守恒知,另一种元素为氢元素,则其钙原子、氯原子和氢原子个数之比=$\frac{52.36%}{40}$:$\frac{46.33}{35.5}$:$\frac{1-52.36%-46.33%}{1}$=1:1:1,化学式为:CaHCl,不能成功制得+1价Ca的化合物,钙元素的化合价是+2价,生成甲的化学反应方程式CaCl2+H2=CaHCl+HCl,
故答案为:CaCl2+H2=CaHCl+HCl;
(2)CaHCl和水反应生成氢气,同时生成氯化钙、氢氧化钙,反应方程式为:2CaHCl+2H2O=CaCl2+Ca(OH)2+2H2↑,
故答案为:2CaHCl+2H2O=CaCl2+Ca(OH)2+2H2↑;
(3)二氧化锰和浓盐酸之间加热反应可以生成氯化锰、水以及氯气,实质是:2Cl-+MnO2+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,氯化亚铁易被氧化为氯化铁,加入铁粉防止氧化,并且氯化亚铁易水解,应保持FeCl2溶液呈酸性.
故答案为:2Cl-+MnO2+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;保持FeCl2溶液呈酸性,并加入铁粉防止氧化;
(4)氯化钙发生化合反应生成CaCl,氯化钙作氧化剂,则钙作还原剂,反应方程式为:Ca+CaCl2=2CaCl,故答案为:Ca+CaCl2=2CaCl.
点评 本题考查了物质间的反应,明确物质的性质是解本题关键,性质决定用途,是一道性质实验方案的设计题,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 由该氯原子构成氯分子(Cl2)的相对分子质量为$\frac{24a}{b}$ | |
| B. | mg该氯原子的物质的量为$\frac{m}{aNA}$ mol | |
| C. | ng该氯原子所含的电子数为$\frac{17n}{aNA}$ | |
| D. | 1mol该氯原子的质量为aNA g |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
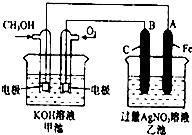 如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O 填写下列空白:
如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O 填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
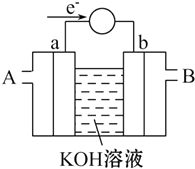 能源问题是当前人类社会面临的一项重大课题,H2、CO、CH3OH都是重要的能源物质,它们的燃烧热依次为285.8kJ/mol、282.5kJ/mol、726.7kJ/mol.请回答:
能源问题是当前人类社会面临的一项重大课题,H2、CO、CH3OH都是重要的能源物质,它们的燃烧热依次为285.8kJ/mol、282.5kJ/mol、726.7kJ/mol.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将SO2通入品红溶液中 | B. | 将Cl2通入KI溶液中 | ||
| C. | 将SO2通入溴水中 | D. | 将H2S通入硝酸溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com