
分析 根据n=$\frac{V}{Vm}$计算甲烷物质的量,根据n $\frac{N}{{N}_{A}}$计算水的物质的量,根据n=$\frac{m}{M}$计算式HCl的物质的量,结合分子式计算含有H原子物质的量,根据 Al2(SO4)3的分子构成确定溶液中SO42-的物质的量.
解答 解:①标准状况下,22.4L CH4的物质的量为 $\frac{22.4L}{22.4L/mol}$=1mol,含有H原子为1mol×4=4mol;
②1.5mol NH3含有H原子为1.5mol×3=4.5mol;
③1.806×1024个H2O的物质的量为$\frac{1.806×1{0}^{24}}{6.02×1{0}^{23}}$=3mol,含有H原子为3mol×2=6mol;
④标准状况下,73g HCl的物质的量为$\frac{73g}{36.5g/mol}$=2mol,含有H原子为2mol×1=2mol,
所含H原子个数由多到少的顺序是:③>②>①>④,在含0.4mol Al2(SO4)3的溶液中,SO42-的物质的量为铝离子物质的量的1.5倍,所以SO42-的物质的量为0.6mol,
故答案为:③>②>①>④;0.6mol.
点评 本题考查物质的量有关计算,比较基础,注意掌握以物质的量为中心计算,注意对化学式意义的理解.


科目:高中化学 来源: 题型:选择题
| 实验 | 现象 | 离子方程式 | |
| A | 稀硫酸滴入含酚酞的Ba(OH)2溶液中 | 白色沉淀生成,溶液由红色变无色 | Ba2++OH-+H++SO${\;}_{4}^{2-}$═BaSO4↓+H2O |
| B | 磁性氧化铁(Fe3O4)溶于氢碘酸 | 磁性氧化铁溶解,溶液变棕黄色 | Fe3O4+8H+═Fe2++2Fe3++4H2O |
| C | Ca(OH)2澄清溶液加到氯水中 | 溶液由黄绿色变为无色 | Cl2+2Ca(OH)2═Cl-+ClO-+Ca2++H2O |
| D | 稀硫酸加到KI淀粉溶液中 | 在空气中放置一段时间后,溶液呈蓝色 | 4H++4I-+O2═2I2+2H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 产品标准 | GB5461 |
| 产品等级 | 一级 |
| 配料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 20~50mg/kg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔既是物质的数量单位又是物质的质量单位 | |
| B. | 阿伏加德罗常数是12 kg 12C中含有的碳原子数 | |
| C. | 1 molH2O分子中含有10 mol电子 | |
| D. | 一个NO分子的质量是a g,一个NO2分子的质量是b g,则氧原子的摩尔质量是(b-a)g•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 净物 | 混合物 | 电解质 | 非电解质 | |
| A | 盐酸 | 水煤气 | 硫酸 | 干冰 |
| B | 冰醋酸 | 漂白粉 | 硫酸钡 | 二氧化硫 |
| C | 石墨 | 空气 | 苛性钾 | 碳酸钙 |
| D | 浓硫酸 | 氨水 | 氯化钠 | 氯气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 用以下反应制取氮气:NaNO2+NH4Cl$\underset{\stackrel{65℃}{=}}{△}$NaCl+N2↑+2H20,已知氮化镁易与水反应,Mg3N2+6H2O=2NH3↑+3Mg(OH)2↓在设计装置时必须考虑这一点:
用以下反应制取氮气:NaNO2+NH4Cl$\underset{\stackrel{65℃}{=}}{△}$NaCl+N2↑+2H20,已知氮化镁易与水反应,Mg3N2+6H2O=2NH3↑+3Mg(OH)2↓在设计装置时必须考虑这一点:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 如图所示的反应为放热反应 | |
| B. | 化学反应中有物质变化也有能量变化 | |
| C. | 化学反应具有方向性 | |
| D. | 化学键断裂吸收能量,化学键生成放出能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
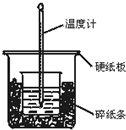 通过测定反应过程中所放出的热量可计算中和热.50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在图示的装置中进行中和反应.回答下列问题:
通过测定反应过程中所放出的热量可计算中和热.50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在图示的装置中进行中和反应.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com