
”¾ĢāÄæ”æ¶ŌÓŚ·“Ó¦11P+15CuSO4+24H2O===5Cu3P+6H3PO4+15H2SO4£¬1 mol P²Ī¼Ó·“Ó¦×ŖŅʵĵē×ÓŹżĪŖ______£¬±»Ńõ»ÆµÄĮ×Óė±»»¹ŌµÄĮ×µÄÖŹĮæ±ČĪŖ______£¬1 mol CuSO4æÉŅŌŃõ»Æ______molµÄĮ×”£
”¾“š°ø”æ![]() 6”Ć5 0.2
6”Ć5 0.2
”¾½āĪö”æ
ŅĄ¾ŻŃõ»Æ»¹Ō·“Ó¦µÄ¹ęĀÉ£¬øĆ·“Ó¦ÖŠ£¬PŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ0¼Ū±äĪŖ©3¼ŪŗĶ+5¼Ū£¬ĶŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ+2¼Ū±äĪŖ+1¼Ū£¬»¹Ō¼Į±»Ńõ»Æ£¬Ńõ»Æ¼Į±»»¹Ō£¬½įŗĻµē×ÓŹŲŗć¹ęĀÉ·ÖĪö¼ĘĖć”£
øĆ·“Ó¦ÖŠ£¬PŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ0¼Ū±äĪŖ©3¼ŪŗĶ+5¼Ū£¬ĶŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ+2¼Ū±äĪŖ+1¼Ū£¬1 mol P²Ī¼Ó·“Ó¦×ŖŅʵĵē×ÓµÄĪļÖŹµÄĮæ=1 mol”Į![]() =
=![]() mol£¬¼“×ŖŅʵĵē×ÓŹżĪŖ
mol£¬¼“×ŖŅʵĵē×ÓŹżĪŖ![]() øö£»øĆ·“Ó¦ÖŠ×÷Ńõ»Æ¼ĮŗĶ»¹Ō¼ĮµÄPµÄĪļÖŹµÄĮæÖ®±ČĪŖ5”Ć6£¬ĖłŅŌ±»Ńõ»ÆŗĶ±»»¹ŌµÄĮ×µÄĪļÖŹµÄĮæÖ®±ČĪŖ6”Ć5£¬ĘäĦ¶ūÖŹĮæĻąµČ£¬ĖłŅŌ±»Ńõ»ÆŗĶ±»»¹ŌµÄĮ×µÄÖŹĮæÖ®±ČĪŖ6”Ć5”£1 mol CuSO4ĶźČ«·“Ó¦×ŖŅʵē×ÓµÄĪļÖŹµÄĮæ=1 mol”Į1=1 mol£¬øł¾Ż×ŖŅʵē×ÓŹŲŗć£¬±»Ńõ»ÆµÄPµÄĪļÖŹµÄĮæ=
øö£»øĆ·“Ó¦ÖŠ×÷Ńõ»Æ¼ĮŗĶ»¹Ō¼ĮµÄPµÄĪļÖŹµÄĮæÖ®±ČĪŖ5”Ć6£¬ĖłŅŌ±»Ńõ»ÆŗĶ±»»¹ŌµÄĮ×µÄĪļÖŹµÄĮæÖ®±ČĪŖ6”Ć5£¬ĘäĦ¶ūÖŹĮæĻąµČ£¬ĖłŅŌ±»Ńõ»ÆŗĶ±»»¹ŌµÄĮ×µÄÖŹĮæÖ®±ČĪŖ6”Ć5”£1 mol CuSO4ĶźČ«·“Ó¦×ŖŅʵē×ÓµÄĪļÖŹµÄĮæ=1 mol”Į1=1 mol£¬øł¾Ż×ŖŅʵē×ÓŹŲŗć£¬±»Ńõ»ÆµÄPµÄĪļÖŹµÄĮæ=![]() =0.2 mol”£
=0.2 molӣ


 ÖĒȤŹī¼ŁĪĀ¹ŹÖŖŠĀĻµĮŠ“š°ø
ÖĒȤŹī¼ŁĪĀ¹ŹÖŖŠĀĻµĮŠ“š°ø Ó¢ÓļŠ”Ó¢ŠŪĢģĢģĬŠ“ĻµĮŠ“š°ø
Ó¢ÓļŠ”Ó¢ŠŪĢģĢģĬŠ“ĻµĮŠ“š°ø Źī¼Ł×÷Ņµ°²»ÕÉŁÄź¶łĶƳö°ęÉēĻµĮŠ“š°ø
Źī¼Ł×÷Ņµ°²»ÕÉŁÄź¶łĶƳö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĮ½ÖÖÖŲŅŖµÄÓŠ»ś»Æ¹¤ŗĻ³ÉÖŠ¼äĢåFŗĶYæÉÓĆ¼×±½ĪŖÖ÷ŅŖŌĮĻ²ÉÓĆŅŌĻĀĀ·ĻßÖĘµĆ£ŗ
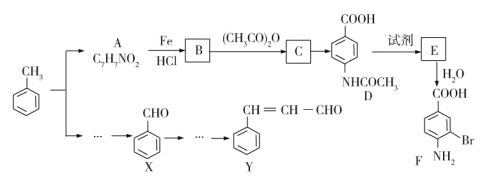
ŅŃÖŖ£ŗ
¢Ł![]()
![]()
![]()
¢Ś2CH3CHO![]() CH3CH(OH)CH2CHO
CH3CH(OH)CH2CHO![]() CH3CH=CHCHO
CH3CH=CHCHO
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Š“³öAµÄ½į¹¹¼ņŹ½___________”£
£Ø2£©B”śCµÄ»Æѧ·½³ĢŹ½ŹĒ________”£
£Ø3£©C”śDµÄ·“Ó¦ĄąŠĶĪŖ__________”£
£Ø4£©1molF×ī¶ąæÉŅŌŗĶ________molNaOH·“Ó¦”£
£Ø5£©ŌŚŗĻ³ÉFµÄ¹ż³ĢÖŠ£¬Éč¼ĘB”śC²½ÖčµÄÄæµÄŹĒ_________”£
£Ø6£©Š“³ö·ūŗĻĻĀĮŠĢõ¼žµÄ3ÖÖAµÄĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½_________”¢______”¢_______”£
¢Ł±½»·ÉĻÖ»ÓŠĮ½ÖÖ²»Ķ¬»Æѧ»·¾³µÄĒāŌ×Ó
¢ŚÄÜ·¢ÉśŅų¾µ·“Ó¦
£Ø7£©ŅŌXŗĶŅŅ“¼ĪŖŌĮĻĶعż3²½æÉŗĻ³ÉY£¬ĒėÉč¼ĘŗĻ³ÉĀ·Ļß______£ØĪŽ»śŹŌ¼Į¼°ČܼĮČĪŃ”£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A.³£ĪĀ³£Ń¹ĻĀ£¬124gP4ÖŠĖłŗ¬P”ŖP¼üŹżÄæĪŖ4NA
B.±ź×¼×“æöĻĀ£¬11.2L¼×ĶéŗĶŅŅĻ©»ģŗĻĪļÖŠŗ¬ĒāŌ×ÓŹżÄæĪŖ2NA
C.17g¼×»ł(”Ŗ14CH3)Ėłŗ¬µÄµē×ÓŹżÄæĪŖ10NA
D.1.5molFeI2Óė22.4LCl2ĶźČ«·“Ó¦Ź±×ŖŅʵĵē×ÓŹżĪŖ2NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æCŹĒŅ»ÖÖ³£¼ūµÄ¹¤ŅµŌĮĻ£¬ŹµŃéŹŅÖʱøCµÄ»Æѧ·½³ĢŹ½ČēĻĀ£¬ĻĀĮŠĖµ·ØÕżČ·µÄ( )
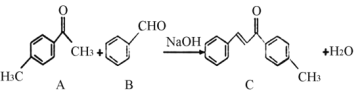
A.l molµÄC×ī¶ąÄÜÓė7 molµÄH2·“Ó¦
B.·Ö×ÓCÖŠĖłÓŠĢ¼Ō×ÓŅ»¶Ø¹²Ę½Ćę
C.æÉŅŌÓĆĖįŠŌKMnO4ČÜŅŗ¼ų±šAŗĶB
D.AµÄĶ¬·ÖŅģ¹¹ĢåÖŠŗ¬ÓŠ±½»·ŗĶČ©»łµÄ½į¹¹ÓŠ14ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĶ¼±ķŹ¾ÅäÖĘ100mL0.100molL©1Na2CO3ČÜŅŗµÄ¼øøö¹Ų¼üŹµŃé²½ÖčŗĶ²Ł×÷£¬»Ų“šĻĀĮŠĪŹĢā£ŗ

£Ø1£©ČōÓĆNa2CO310H2OĄ“ÅäÖĘČÜŅŗ£¬ŠčŅŖÓƵē×ÓĢģĘ½³ĘĮ澧Ģå_____æĖ”£ČōĖłČ”µÄ¾§ĢåŅŃ¾ÓŠŅ»²æ·ÖŹ§Č„ĮĖ½į¾§Ė®£¬ŌņĖłÅäÖʵÄČÜŅŗÅضČĘ«_____”££ØĢī”°“ó/Š””±£©”£
£Ø2£©Š“³öÅäÖĘČÜŅŗÖŠĖłŠčŅŖÓƵ½µÄ²£Į§ŅĒĘ÷µÄĆū³Ę£ŗÉÕ±”¢_____”£
£Ø3£©²½ÖčB³ĘĪŖ×ŖŅĘ£¬²½ÖčA³ĘĪŖ_____£¬Čē¹ūø©ŹÓæĢ¶ČĻߣ¬ÅäÖʵÄÅØ¶Č½«Ę«_____£ØĢī“ó»ņŠ”£©”£²½ÖčD³ĘĪŖ_____£¬Čōƻӊ²½ÖčD£¬ŌņÅäÖʵÄÅضČĘ«_____”££ØĢī”°“ó/Š””±£©”£
£Ø4£©½«ÉĻŹöŹµŃé²½ÖčA©F°“ŹµŃé¹ż³ĢĻČŗó“ĪŠņÅÅĮŠ_____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ
ŃŠ¾æ·¢ĻÖ£¬ŌŚCO2µĶŃ¹ŗĻ³É¼×“¼·“Ó¦£ØCO2+3H2=CH3OH+H2O£©ÖŠ£¬CoŃõ»ÆĪļøŗŌŲµÄMnŃõ»ÆĪļÄÉĆ×Į£×ӓ߻ƼĮ¾ßÓŠøß»īŠŌ£¬ĻŌŹ¾³öĮ¼ŗƵÄÓ¦ÓĆĒ°¾°”£»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Co»łĢ¬Ō×ÓŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ_____________”£ŌŖĖŲMnÓėOÖŠ£¬µŚŅ»µēĄėÄܽĻ“óµÄŹĒ_________£¬»łĢ¬Ō×ÓŗĖĶāĪ“³É¶Ōµē×ÓŹż½Ļ¶ąµÄŹĒ_________________”£
£Ø2£©CO2ŗĶCH3OH·Ö×ÓÖŠCŌ×ÓµÄŌӻƊĪŹ½·Ö±šĪŖ__________ŗĶ__________”£
£Ø3£©ŌŚCO2µĶŃ¹ŗĻ³É¼×“¼·“Ó¦ĖłÉę¼°µÄ4ÖÖĪļÖŹÖŠ£¬·Šµć“Óøßµ½µĶµÄĖ³ŠņĪŖ_________£¬ŌŅņŹĒ______________________________”£
£Ø4£©ĻõĖįĆĢŹĒÖʱøÉĻŹö·“Ó¦“߻ƼĮµÄŌĮĻ£¬Mn(NO3)2ÖŠµÄ»Æѧ¼ü³żĮĖ¦Ņ¼üĶā£¬»¹“ęŌŚ________”£
£Ø5£©MgO¾ßÓŠNaClŠĶ½į¹¹£ØČēĶ¼£©£¬ĘäÖŠŅõĄė×Ó²ÉÓĆĆęŠÄĮ¢·½×īĆܶѻż·½Ź½£¬XÉäĻßŃÜÉ䏵Ńé²āµĆMgOµÄ¾§°ū²ĪŹżĪŖa=0.420nm£¬Ōņr(O2-)ĪŖ________nm”£MnOŅ²ŹōÓŚNaClŠĶ½į¹¹£¬¾§°ū²ĪŹżĪŖa' =0.448 nm£¬Ōņr(Mn2+)ĪŖ________nm”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æNa2S2O4”¤2H2OŹĒČ¾ĮĻ¹¤ŅµÖŠ³£ÓƵĻ¹Ō¼Į£¬Ė×³Ę±£ĻÕ·ŪĖüæÉČÜÓŚĒāŃõ»ÆÄĘČÜŅŗ²¢ĪČ¶Ø“ęŌŚ£¬ÄŃČÜÓŚŅŅ“¼£¬ŹÜČČŅ×·Ö½ā£¬Öʱø±£ĻÕ·ŪµÄĮ÷³ĢČēĻĀ:
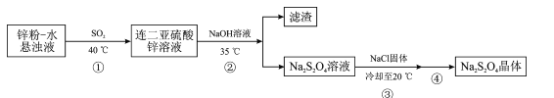
»Ų“šĻĀĮŠĪŹĢā:
(1)±£ĻÕ·ŪµÄÖʱø¹ż³ĢŅŖŌŚĪŽŃõĢõ¼žĻĀ½ųŠŠ£¬ŌŅņŹĒ__________
(2)ČōÓĆNa2SO3¹ĢĢåŗĶĖį·“Ó¦ÖʱøSO2ĘųĢ壬ĻĀĮŠ×īŹŹŅĖŃ”ÓƵÄĖįŹĒ____(Ģī±źŗÅ)
A.ÅØŃĪĖį B.Ļ”ĻõĖį C.70%ĮņĖį D.98%ĮņĖį
(3)²½Öč¢ŚŠčŅŖæŲÖĘĪĀ¶ČŌŚ35”ęµÄŌŅņŹĒ__________ŅŃÖŖpH>11Ź±£¬Zn(OH) 2×Ŗ»ÆĪŖ![]() £¬ĪŖĮĖŹ¹Zn2+³ĮµķĶźČ«,Ōņ¼ÓČėĒāŃõ»ÆÄĘČÜŅŗµ÷½ŚČÜŅŗµÄpH·¶Ī§ŹĒ______________(25”ꏱKsp[Zn(OH)2]=1.0”Į1017£¬35”ꏱKspÓėKwµÄ±ä»ÆæÉŗöĀŌ)
£¬ĪŖĮĖŹ¹Zn2+³ĮµķĶźČ«,Ōņ¼ÓČėĒāŃõ»ÆÄĘČÜŅŗµ÷½ŚČÜŅŗµÄpH·¶Ī§ŹĒ______________(25”ꏱKsp[Zn(OH)2]=1.0”Į1017£¬35”ꏱKspÓėKwµÄ±ä»ÆæÉŗöĀŌ)
(4)²½Öč¢ŪÖŠ¼ÓČėŅ»¶ØĮæNaCl¹ĢĢåµÄÄæµÄŹĒ____
(5)²½Öč¢ÜµÄ²Ł×÷ŹĒ__________¾øÉŌļµĆNa2S2O4”¤2H2Oѳʷ
(6)ĪŖĮĖ²ā¶ØNa2S2O4”¤2H2Oѳʷ“æ¶Č£¬Č”mgѳʷČܽāŌŚ×ćĮæµÄ¼×Č©ČÜŅŗÖŠ£¬ÅäÖĘ³É100.00mLČÜŅŗČ”10.00mLČÜŅŗӌ׶ŠĪĘæÖŠ£¬ÓĆcmol/Lµā±ź×¼ŅŗµĪ¶ØÖĮÖÕµć£¬Ļūŗıź×¼ŅŗµÄĢå»żĪŖVmL²ā¶Ø¹ż³ĢÖŠ£¬·¢ÉśµÄ·“Ó¦£ŗNa2S2O4+2HCHO+H2OØTNaHSO3CH2O+NaHSO2CH2O£¬NaHSO2CH2O+2I2+2H2OØTNaHSO4+HCHO+4HI£¬Ōņѳʷ֊Na2S2O4”¤2H2OµÄ“æ¶ČĪŖ____
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©ĻÖÓŠĻĀĮŠ10ÖÖĪļÖŹ£ŗ¢ŁAl ¢ŚĻ”ĻõĖį ¢ŪŅŅĖį ¢ÜŅŗ°± ¢Żøɱł ¢ŽNaCl ¢ßNaOHČÜŅŗ ¢ąBaCO3 ¢į¾Ę¾« ¢āHClĘųĢ壬Ķź³ÉĻĀĆęµÄĢīæÕ£¬Ö»ĢīŠņŗÅ
ŹōÓŚ·Ēµē½āÖŹµÄŹĒ___£»ŹōÓŚĒæµē½āÖŹµÄŹĒ___£»ŹōÓŚČõµē½āÖŹµÄŹĒ___£»Äܵ¼µēµÄĪļÖŹŹĒ___”£
£Ø2£©ŅŃÖŖŌŚ³£ĪĀ³£Ń¹ĻĀ£ŗ
¢Ł2CH3OH(l)+2O2(g)ØT2CO(g)+4H2O(g) ”÷H=©akJmol©1
¢Ś2CO(g)+O2(g)ØT2CO2(g) ”÷H=©bkJmol©1
¢ŪH2O(g)ØTH2O(l) ”÷H=©ckJmol©1
Ōņ±ķŹ¾CH3OH(l)Č¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½ĪŖ___”£
£Ø3£©Na2CO3µČČÜŅŗ²»ÄÜ“ę·ÅŌŚÄ„æŚ²£Į§ČūµÄŹŌ¼ĮĘæÖŠ£¬ĘäŌŅņŹĒ£Ø½įŗĻĄė×Ó·½³ĢŹ½ĖµĆ÷£©£ŗ___£»°ŃČżĀČ»ÆĢśČÜŅŗÕōøɲ¢³ä·Ö×ĘÉÕ£¬×īŗóµĆµ½µÄ¹ĢĢå²śĪļŹĒ___£Ø»ÆѧŹ½£©£»Ļą¹Ų·“Ó¦µÄ»Æѧ·“Ó¦·½³ĢŹ½ŹĒ£ŗ___”¢___£»ÅäÖĘFeCl2ČÜŅŗŹ±£¬Ó¦¼ÓČė___£¬ŅŌŅÖÖĘFe2+µÄĖ®½ā”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫µČĪļÖŹµÄĮæµÄAŗĶB£¬»ģŗĻÓŚ2 LµÄĆܱÕČŻĘ÷ÖŠ£¬·¢ÉśČēĻĀ·“Ó¦£ŗ3A£Øg£©+B(g) ![]() xC(g)+2D(g)”£2minŗ󣬲āµĆDµÄÅضČĪŖ
xC(g)+2D(g)”£2minŗ󣬲āµĆDµÄÅضČĪŖ![]() mol/L ,
mol/L ,![]() £¬CµÄ·“Ó¦ĖŁĀŹŹĒ
£¬CµÄ·“Ó¦ĖŁĀŹŹĒ![]() mol/(L”¤min)”£Ōņ£ŗ
mol/(L”¤min)”£Ōņ£ŗ
¢ŁxµÄÖµŹĒ__________£»
¢ŚBµÄĘ½¾ł·“Ó¦ĖŁĀŹŹĒ____________£»
¢ŪAŌŚ2minÄ©µÄÅØ¶ČŹĒ________________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com