
【题目】下图是一种正投入生产的大型蓄电系统,放电前,被膜隔开的电解质为Na2S2和NaBr3,放电后分别变为Na2S4和NaBr。下列叙述正确的是( )
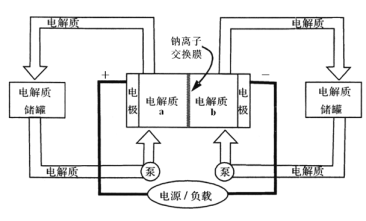
A. 放电时,负极反应为3NaBr-2e-=NaBr3+2Na+
B. 充电时,阳极反应为2Na2S2-2e-=Na2S4+2Na+
C. 放电时,Na+经过离子交换膜,由b池移向a池
D. 用该电池电解饱和食盐水,产生2.24 L H2时,b池生成17.40gNa2S4
【答案】C
【解析】
由题意可知,放电时,负极上Na2S2被氧化为Na2S4,正极上NaBr3被还原为NaBr,则左储罐电解质为NaBr3/NaBr,右储罐电解质为Na2S2/Na2S4。
A、放电时,负极上Na2S2被氧化为Na2S4,电极反应式为:2Na2S2-2e- =Na2S4+2Na+,故A错误;
B、充电时,电池的正极与电源正极相连,作阳极,阳极上NaBr被氧化为NaBr3,电极反应式为:3NaBr-2e-=NaBr3+2Na+,故B错误;
C、放电时,阳离子向正极移动,则离子Na+经过离子交换膜,由b池移向a池,故C正确;
D、没有确定是否为标准状况,无法计算氢气的物质的量,则无法计算b池生成Na2S4质量,故D错误;
答案选C。


 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、W是元素周期表中前36号元素,它们的原子序数依次增大。A的质子数、电子层数、最外层电子数均相等,B元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子总数相同,D的基态原子核外成对电子数是成单电子数的3倍,E4+与氩原子的核外电子排布相同。W是第四周期d区原子序数最大的元素。请回答下列问题:
(1)填元素名称, C:________写出E的价层电子排布式_________,W在周期表中的位置:___________________
第二周期基态原子未成对电子数与W相同且电负性最小的元素是________(填元素符号).
(2)W(BD)n为无色挥发性剧毒液体,熔点﹣25℃,沸点43℃.不溶于水,易溶于乙醇、乙醚、苯等有机溶剂,呈四面体构型,W(BD)n的中心原子价电子数与配体提供电子总数之和为18,则n=________,BD分子的结构式是________
(3)3﹣氯﹣2﹣丁氨酸的结构简式为:![]() ,一个该有机物分子中含有_____个手性碳原子.
,一个该有机物分子中含有_____个手性碳原子.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将![]() 和
和![]() 置于一容积为2L的密闭容器中发生反应:
置于一容积为2L的密闭容器中发生反应:![]() ,反应过程中
,反应过程中![]() 、
、![]() 和
和![]() 的物质的量变化如下图:
的物质的量变化如下图:

(1)该反应化学平衡常数K的表达式为________。随着温度升高,平衡常数________(选填“增大”、“减小”或“不变”)。计算![]() 的平均反应速率
的平均反应速率![]() ________。
________。
(2)下列说法不能表明该反应达到平衡状态的是________。
a.容器内的压强不再变化 b.容器内气体的密度不再变化
c.![]() d.3mol H-H键断裂的同时,有6mol N-H键生成
d.3mol H-H键断裂的同时,有6mol N-H键生成
(3)0-10min、10-20min两个时间段内,![]() 的平均反应速率之比为________。在第10min可能改变的条件是__________________________________________。
的平均反应速率之比为________。在第10min可能改变的条件是__________________________________________。
(4)反应进行至25min时,曲线发生变化的原因是__________________________________________________.为使反应速率减小,且平衡向正反应方向移动,可采取的措施是________。
a.增大容器的体积 b.降低温度 c.使用催化剂
(5)在图中画出25min-40min时间段内![]() 的物质的量的变化图像(画在上图中)。__________________
的物质的量的变化图像(画在上图中)。__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A(C2H4)是基本的有机化工原料。用A和常见的有机物可合成一种醚类香料和一种缩醛类香料。具体合成路线如图所示(部分反应条件略去):
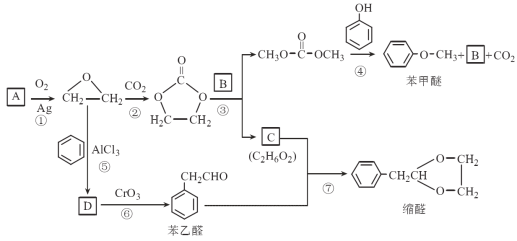
已知以下信息:
①![]()
②D为单取代芳香族化合物且能与金属钠反应;每个D分子中只含有1个氧原子,D中氧元素的质量分数约为13.1%。
回答下列问题:
(1)A的名称是______,图中苯甲醚的分子式是________。
(2)B的结构简式为____________________,D中含有的官能团名称是________。
(3)②的反应类型是____________________。
(4)⑦的化学方程式为__________________________________________________。
(5)请写出满足下列条件的苯乙醛的所有同分异构体的结构简式:含有苯环和![]() 结构,核磁共振氢谱有4组峰,峰面积之比为3∶2∶2∶1。____________
结构,核磁共振氢谱有4组峰,峰面积之比为3∶2∶2∶1。____________
(6)参照 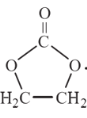 的合成路线,设计一条由2-氯丙烷和必要的无机试剂制备
的合成路线,设计一条由2-氯丙烷和必要的无机试剂制备 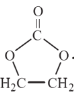 的合成路线____________(注明必要的反应条件)。合成路线流程图示例如下:CH3CH2OH
的合成路线____________(注明必要的反应条件)。合成路线流程图示例如下:CH3CH2OH![]() CH2=CH2
CH2=CH2![]() BrCH2-CH2Br
BrCH2-CH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知a An+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是( )
A. 原子序数:b>a>c>dB. 最高价氧化物对应水化物的碱性:B>A
C. 四种离子的电子层结构相同,因而离子的性质也相同D. 气态氢化物的稳定性:D>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应![]() ,在容积固定的密闭容器中达到平衡状态的标志是( )
,在容积固定的密闭容器中达到平衡状态的标志是( )
①单位时间内生成![]() 的同时生成
的同时生成![]()
②单位时间内生成![]() 的同时生成
的同时生成![]()
③用![]() 表示的反应速率之比为
表示的反应速率之比为![]() 的状态
的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的物质的量不再改变的状态
A.①④⑥⑦B.②③⑤⑦C.①③④⑤D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.1mol Na2CO3与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH的关系如图所示。下列有关溶液中离子浓度关系叙述正确的是

A. W点所示的溶液中:c(Na+)>c(CO32-)= c(HCO3-)>c(OH-)>c(H+)
B. pH=4的溶液中:c(H2CO3)+c(HCO3-)+ c(CO32-)=0.1mol/L
C. pH=8的溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
D. pH=11的溶液中:c(Na+)+c(H+)=c(OH-)+c(Cl-)+c(CO32-)+c(HCO3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正确表示下列反应的离子反应方程式为
A.向FeBr2溶液中通入足量氯气:2Fe2++4Br﹣+3Cl2═2 Fe3++2 Br2+6Cl﹣
B.向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42﹣沉淀完全:![]()
C.![]() 稀溶液与过量的KOH溶液反应:
稀溶液与过量的KOH溶液反应:![]()
D.醋酸除去水垢:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组制取氯气并进行氯气的性质实验,其装置如图所示,回答下列问题:
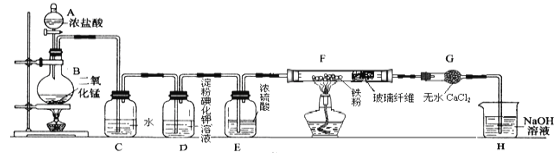
(1)仪器A的名称是 ______,实验中制备氯气的反应方程式为 ____________________。
(2)C中发生反应的化学方程式为 ______ .若将干燥的有色布条放入C中,观察到的现象是 ______,原因是 ___________________________。
(3)实验中观察到D溶液变蓝色,查资料得知淀粉碘化钾溶液是淀粉和碘化钾(KI)的混合溶液,写出D装置中发生反应的离子方程式______________________。
(4)F中氯气与铁粉反应制备无水三氯化铁,查资料知该化合物呈棕红色、易吸水潮解, 100℃左右时升华.双通管F中玻璃纤维(不参与反应)的作用是 ______ ;在F和H装置之间安装G装置的目的是____。
(5)H中NaOH溶液的作用是 _______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com