
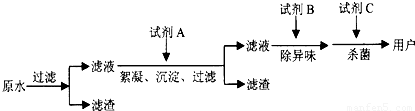
 ×2.4×10-3mol=6×10-4mol,1L水样消耗的氧气是质量是:
×2.4×10-3mol=6×10-4mol,1L水样消耗的氧气是质量是: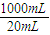 ×6×10-4mol×32g/mol=0.96g=960mg,
×6×10-4mol×32g/mol=0.96g=960mg,

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
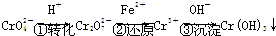
2- 4 |
2- 7 |
2- 7 |
2- 4 |
2- 7 |
2- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:
![]() 水是生命之源,2005年12月发生在我省的北江水污染事件再次提醒人们保护水资源的必要性和紧迫性。
水是生命之源,2005年12月发生在我省的北江水污染事件再次提醒人们保护水资源的必要性和紧迫性。
![]() (1)据报道,北江水污染事件是由于某冶炼厂设备检修期间排放的废水所致,推测其主要污染物是 。如果有害废水已经在河流中扩散,为了尽量减少危害,对河水的处理应该采取的措施是
(1)据报道,北江水污染事件是由于某冶炼厂设备检修期间排放的废水所致,推测其主要污染物是 。如果有害废水已经在河流中扩散,为了尽量减少危害,对河水的处理应该采取的措施是
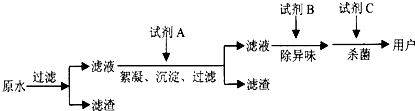
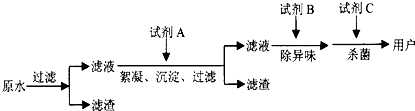
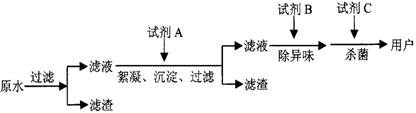
![]() (2)自来水的生产流程如图,其中的试剂A、B、C分别可以选择 、 、 。
(2)自来水的生产流程如图,其中的试剂A、B、C分别可以选择 、 、 。
(3)电镀厂排放的废水中含铬(以Cr2O72-形式存在),常用电解的方法处理。电解时,以铁为阳极,生成的Fe2+将Cr2O72-还原为Cr3+,产物再与电解时生成的OH-形成氢氧化物沉淀而除去。
①两个电极上发生的反应分别为:阳极 ,阴极 。
②溶液中发生的总反应为(用离子方程式表示) 。
(4)化学需氧量(COD)是水体质量的控制项目这一,它是量废水中还原性污染物的重要指标。COD是指用强氧化剂(我国采用K2Cr2O7)处理一定量水样时消耗的氧化剂的量,并换算成以O2作为氧化剂时,1L水样所消耗O2的质量(mg?L-1)。现取某池塘水样20.00mL,反应消耗10.00mL0.0400mol?L-1K2Cr2O7溶液(反应后转化为Cr3+)。该水样的COD为 mg?L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com