

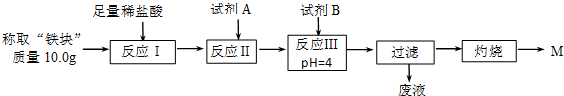
| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| ��ʼ����ʱ��pH | 7.5 | 2.8 | 4.2 | 9.6 |
| ������ȫʱ��pH | 9.0 | 4.0 | 5 | 11 |
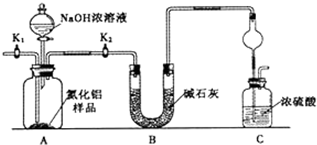
���� ��1����ȡ��Ӧ��ġ����顱����ȡ��������������ͼ2װ�õ�������NaOH��Һ��ַ�Ӧ����������������������Լ���õ���Ӧ���������ʵ������õ����������ĺ�����
�������ܵ����߲��ֵײ��������ܣ����ʵ�����߿�֪�Ǽ�ʽ�ζ��ܵIJ��ֽṹ��
�۶������ܶ���ʱ�����ȵ�ʵ��װ�ûָ��������ٽ�����һ��������Ȼ�����������ʹ����Һ����ƽ��������ʱ�����밼Һ����ʹ���ƽ��
��װ��ʹ�÷�Һ©������Һ��������ƿ��ѹǿ��������Һ�����л��ų���Һ�����࣬���²ⶨ���ƫ�ߣ�
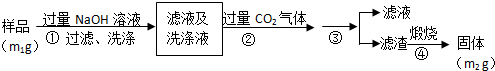
��2���ٸ��������֪����ʵ��Ҫ����������á����顱�ijɷ֣���Ҫͨ��ʵ�����̣�����Ԫ����ȫ�����������ݱ����֪��Ҫʹ��Ԫ����ȫ����������þ���������轫Fe2+ת��ΪFe3+��Ȼ�������
��������ȫ�ı�־������ǰ��������������������0.1g��
�۸���10.0g�������е���Ԫ������ȫ�������պ�ɫ��δM�У�������ԭ�ӵ��غ������㣻��������ù��˹���ֱ��ϴ�ӡ���ɡ����������㡰���顱�Ĵ��ȣ�
��� �⣺��1����ȡ��������������ͼ1ʵ��װ�ý������ȷ�Ӧ����ȴ��õ������顱����ȡ��Ӧ��ġ����顱����ȡ��������������ͼ2װ�õ�������NaOH��Һ��ַ�Ӧ����������������������Լ���õ���Ӧ���������ʵ������õ����������ĺ�������ʵ���ʵ��Ŀ���ǣ�������Ʒ�����ĺ�����
�ʴ�Ϊ������
�������ܵ����߲��ֵײ��������ܣ����ʵ�����߿�֪�Ǽ�ʽ�ζ��ܵIJ��ֽṹ�����Ը�����������Ϊ��ʽ�ζ��ܣ��ʴ�Ϊ����ʽ�ζ��ܣ�
�۸���PV=nRT��Ϊ��֤���������������ǵ�ʱ����ѹ�µ�������ڶ���ʱӦע�⣺�ٽ�ʵ��װ�ûָ������£���ʹ����������Һ����ƽ����Ϊ��ƽ˵������Һ���ϵ�ѹǿ��һ���ģ����������������������ǵ�ʱ����ѹ�µ�������������밼Һ����ʹ���ƽ�����ӻ����ӻ�������������ڶ���ʱ�������ҹ�Һ����ƽ֮ǰ�IJ����ǻָ������£�
�ʴ�Ϊ���ָ������£�
�ܵ�Һ©������ƽ��ѹǿ��Һ��˳��������ƿ֮���������ʵ���������ã����װ��ʹ�÷�Һ©������Һ��������ƿ��ѹǿ������ƿ���ų�Һ�����࣬�������ĸ����ʰٷֺ�������ƫ��
�ʴ�Ϊ��ƫ��
��3���ٸ��ݱ����֪��Ҫʹ��Ԫ����ȫ�����������Ӻ�þ���Ӳ��������轫Fe2+ת��ΪFe3+������Ҫ����H2O2��Ȼ�����4��pH��4.2���ɽ�Fe3+������Al3+��Mg2+������������pHѡ�õ��Լ�����������������Ϊ�������ɫ��δM������ƫ��Ҳ������MgCO3���壬��ΪMgCO3�������ʱ���������ù���M������ƫ��Ӧѡ�ð�ˮ���ʴ�Ϊ��C��D��
��������ȫ�ı�־������ǰ��������������������0.1g���ʴ�Ϊ��ǰ��������������������0.1g��
�����պ�ɫ��δMΪFe2O3������10.0g�������е���Ԫ������ȫ����12.0gFe2O3�У�����ԭ�ӵ�����Ϊ��m��Fe��=$\frac{12.0g}{160g/mol}$��2��56gmol=8.4g���ʸá����顱�Ĵ���=$\frac{8.4g}{10.0g}$��100%=84%���ʴ�Ϊ��84%��
���� �����ۺϿ��������ȷ�Ӧ�Լ��������������������ӵ�ת���Լ����ӵij�������Ҫ��ʵ����̷����жϣ������ļ��������ڣ��ۺ��Խ�ǿ���ѶȽϴ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѧ��Ӧ�Ĺ��̣��������Ǿɻ�ѧ�����Ѻ��»�ѧ���γɵĹ��� | |
| B�� | ��ѧ������ʹ�������ϣ�Ҳ����ʹԭ������ | |
| C�� | ԭ���к�������Ų��������Ա仯�Dz���Ԫ�������ɵĸ���ԭ�� | |
| D�� | ���ؾ���ͬλ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH3 | B�� | CO2 | C�� | H2O | D�� | SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
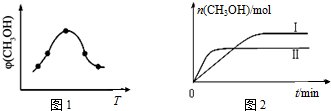
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2���һ����� | B�� | 2��3��3���������� | ||
| C�� | 2����-3-���� | D�� | 2��3-���һ�-1-��ϩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 N��BԪ�ؼ��仯�����ڹ�ũ�������к���Ҫ��Ӧ�ã�
N��BԪ�ؼ��仯�����ڹ�ũ�������к���Ҫ��Ӧ�ã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaCl��Һ | B�� | Na2CO3��Һ | C�� | Na2SO4��Һ | D�� | AgNO3��Һ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com