
|
| 1 |
| 2 |
|


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
(6分)氢氧化铜悬浊液中存在如下平衡:Cu(OH)2 (s)Cu2+(aq)+2OH-(aq),常温下其Ksp=c(Cu2+) · c2(OH-)=2×10-20mol2·L-2。
(1)某硫酸铜溶液里c(Cu2+)=0.02mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH使之大于 。
(2)要使0.2mol/L硫酸铜溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入氢氧化钠溶液使溶液pH为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)氢氧化铜悬浊液中存在如下平衡:Cu(OH)2 (s)Cu2+(aq)+2OH-(aq),常温下其Ksp=
![]() =
=![]() 。
。
①某硫酸铜溶液里Cu2+浓度0.02mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH使之大于 。
②要使0.2mol/L硫酸铜溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入氢氧化钠溶液,使溶液中OH-浓度为 。
(2)用标准的NaOH滴定未知浓度的盐酸,盐酸装在锥形瓶中,并滴入酚酞为指示剂,NaOH溶液装在 (填仪器名称)中。造成测定结果偏高的原因可能是 。
A. 未用标准液润洗,就装入标准液
B. 滴定前读数时仰视,滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C. 盛装未知液的锥形瓶用待测液润洗
D. 滴定过程中,锥形瓶中有数滴溶液溅出
E. 终点时,溶液显浅红色,且半分钟内没有褪去
查看答案和解析>>
科目:高中化学 来源:2012届福建省高二下学期第一学段考试化学试卷 题型:填空题
(6分) 氢氧化铜悬浊液中存在如下平衡:
Cu(OH)2 (s) Cu2+(aq)+2OH-(aq),常温下其Ksp=2×10-20则:
Cu2+(aq)+2OH-(aq),常温下其Ksp=2×10-20则:
(1)某硫酸铜溶液里c(Cu2+)=0.02mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH大于 。
(2)除去CuCl2溶液中少量的Fe2+,可以按照下面的流程进行:
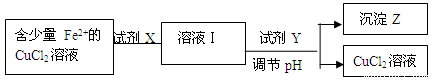
已知Fe2+ 、Cu2+ 、Fe3+ 三种离子开始沉淀和完全沉淀时溶液pH值如下:
|
金属 离子 |
pH |
|
|
开始沉淀 |
完全沉淀 |
|
|
Fe2+ |
7.6 |
9.6 |
|
Cu2+ |
4.4 |
6.4 |
|
Fe3+ |
2.7 |
3.7 |
①下列物质中适合作为试剂X的是
A.H2O2 B.KMnO4 C.HNO3 D.Cl2
②加入的Y及调节的pH范围是
A.CuCO3 3.7~4.3 B.CuO 3.7~6.4
C.NaOH 3.7~4.2 D.NH3·H2O 3.7~4.0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com