
【题目】实验室制取乙烯的传统做法是采用浓硫酸做催化剂,由于浓硫酸具有具有脱水性和强氧性,生成乙烯同时产生CO2和SO2气体会影响乙烯的性质实验.某同学查阅相关资料后发现,可用脱水性更强的P2O5代替浓硫酸浓硫酸作为该实验的催化剂.为验证这一说法,该同学利用以下装置进行实验探究,观察并记录现象如下: 
实验一 | 实验二 | |
实验药品 | 4g P2O5、8mL无水乙醇 | |
实验条件 | 酒精灯加热 | 水浴加热 |
实验现象 | 无水乙醇加入时,圆底烧瓶B中P2O5溶于乙醇,立即产生白雾,当用酒精灯加热后,有气泡产生,并逐渐沸腾,生成粘稠状液体,集气瓶C中有无色液体产生. | 无水乙醇加入时,圆底烧瓶B中P2O5溶于乙醇立即产生白雾,当用水浴加热后,无气泡产生,生成粘稠状液体,集气瓶C中有无色液体产生. |
请回答下列问题:
(1)写出装置中仪器A的名称;
(2)装置中B、C之间长导管的作用是 , 浓硫酸的作用是;
(3)实验二中,完成水浴加热必需的玻璃仪器有、;
(4)实验一、二中当加入无水乙醇时,均有白雾产生,请简述产生白雾的原因:;
(5)经检验集气瓶C中无色液体为磷酸三乙酯,请在图中虚线框内画出实验装置(含试剂)用于验证生成的乙烯;
(6)根据实验现象判断以P2O5作为催化剂获得乙烯的反应条件是 .
【答案】
(1)分液漏斗
(2)导气、冷凝;干燥气体
(3)大烧杯;酒精灯
(4)P2O5溶解于乙醇,迅速放出大量的热,局部温度较高,使得少量乙醇气化,形成白雾
(5)
(6)加热至较高温度
【解析】解:(1.)根据图示可知,仪器A为分液漏斗,所以答案是:分液漏斗;
(2.)装置中B、C之间长导管可以起到导气、冷凝的作用;浓硫酸具有吸水性,能够干燥反应产生的气体,所以答案是:导气、冷凝;干燥气体;
(3.)水浴加热过程中,反应装置需要放在盛有水的大烧杯中,用酒精灯加热,所以必需的玻璃仪器为大烧杯和酒精灯,所以答案是:大烧杯;酒精灯;
(4.)由于P2O5溶解于乙醇后迅速放出大量的热,导致局部温度较高,使得少量乙醇气化,所以形成白雾,所以答案是:P2O5溶解于乙醇,迅速放出大量的热,局部温度较高,使得少量乙醇气化,形成白雾;
(5.)可以用溴水具有乙烯,实验装置图为:  ,答案为:
,答案为:  ;
;
(6.)实验二中水浴加热生成了磷酸三乙酯,而实验一中用酒精灯直接加热生成了乙烯,说明以P2O5作为催化剂获得乙烯需要在较高温度下才能进行,所以答案是:加热至较高温度.


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)室温下,0.1 mol/L NaClO溶液的pH0.1 mol/L Na2SO3溶液的pH. (选填“大于”、“小于”或“等于”).浓度均为0.1 mol/L 的Na2SO3和Na2CO3的混合溶液中,SO32﹣、CO32﹣、HSO3﹣、HCO3﹣ 浓度从大到小的顺序为 .
已知:H2SO3 K1=1.54×10﹣2 K2=1.02×10﹣7 HClO K1=2.95×10﹣8
H2CO3 K1=4.3×10﹣7 K2=5.6×10﹣11
(2)用标准碘溶液滴定容有SO2的水溶液,以测定水中SO2的含量,应选用作指示剂,达到滴定终点的现象是 .
(3)常温下,将amol/lCH3COONa溶于水配成溶液,向其中滴加等体积bmolL﹣1的盐酸使溶液呈中性(不考虑醋酸和盐酸的挥发),用含a和b的代数式表示醋酸的电离平衡常数Ka= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应速率是化学反应原理的重要组成部分.请回答下列问题:
(1)已知一定条件下发生反应:2SO2(g)+O2(g)2SO3(g)△H<0,在反应过程中,正反应速率的变化如图所示,请根据速率的变化回答采取的措施(改变的条件). 
(2)探究反应条件对0.l0mol/L,Na2S2O3溶液与稀H2SO4反应速率的影响.其设计与测定结果如表:
编号 | 反应温度/℃ | Na2S2O3浓液/mL | 甲 | 0.1mol/LH2SO4溶液/mL | 乙 |
① | 25℃ | 10.0 | 0 | 10.0 | |
② | 25℃ | 5.0 | a | 10.0 | |
③ | 45℃ | 10.0 | 0 | 10.0 |
上述实验①③是探究对化学反应速率的影响;若上述实验①②是探究浓度对化学反应速率的影响,则表格中“甲”为 , a为;乙是实验需要测量的物理量,则表格中“乙”为 .
(3)已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在开始一段时间内,反应速率较小,溶液褪色不明显;但不久突然褪色,反应速率明显增大. ①针对上述现象,某同学认为该反应放热,导致溶液温度上升,反应速率增大.从影响化学反应速率的因素看,你猜想还可能是的影响.
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,可以在反应一开始时加入(填字母序号).
A.硫酸钾B.氯化锰c.硫酸锰D.水.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。
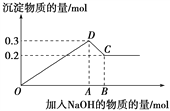
(1)写出代表各线段发生的反应的离子方程式:
OD段________________________________________________,
DC段________________________________________________。
(2)原溶液中Mg2+、Al3+的物质的量浓度之比为________。
(3)图中C点表示当加入______mol NaOH时,Al3+已经转化为_____,Mg2+已经转化为______。
(4)图中线段OA∶AB=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组混合液:①乙酸乙酯和碳酸钠溶液;②乙醇和丁醇;③溴化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏
B.萃取、蒸馏、分液
C.分液、蒸馏、萃取
D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示某化学反应过程中,生成物的量与时间的关系,图中a、b、c三条曲线不能反映下列哪种因素对生成物的量的影响( )

A. 不同的温度 B. 不同的pH值
C. 不同的底物浓度 D. 不同的酶浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.共价化合物中可能含有离子键
B.Ca2+、K+、Cl﹣、S2﹣四种粒子的离子半径依次减小
C.![]() Po、
Po、 ![]() Po、
Po、 ![]() Po三种原子的核外电子数分别为124、125、126
Po三种原子的核外电子数分别为124、125、126
D.第ⅥA族元素氧、硫、硒对应的氢化物H2O、H2S、H2Se的稳定性依次减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学学习小组对某镁铝合金进行了如下实验研究,请你参与并完成有关问题。
【实验药品】:
12.6g镁铝合金,200ml a mol/L稀硫酸,520ml 4 mol/L NaOH溶液。
【实验步骤】:
①将12.6g镁铝合金与200mL a mol/L的稀硫酸在如图所示装置中充分反应至反应完毕,并收集生成的全部气体。

②向b内的混合液中逐滴加入520ml 4 mol/L氢氧化钠溶液并充分混合,当氢氧化钠溶液加至500mL时生成的沉淀量最大。
【问题讨论】:
(1)仪器b的名称是___________________。
(2)根据实验目的可知,12.6g镁铝合金与200mL a mol/L的稀硫酸反应时,应该过量的物质是____________(填“镁铝合金”或“稀硫酸”),以保证另一种物质能够完全反应无剩余;若标准状况下,由实验步骤①得到的气体为13.44L,则合金中镁的质量分数为__________________________(保留到0.1%)。
(3)实验步骤②中,当b内混合液中因滴加氢氧化钠溶液至生成的沉淀量最大时,此时所得溶液中的溶质是__________________(填化学式)。
(4)实验步骤①结束后,读取量筒所呈现的数据时,需要注意的三个问题是:一是要冷却到室温,二是要_____________________________,三是要视线与量筒内的凹液面相平。
(5)在“a mol/L稀硫酸”中的a的值为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,①5gH2 ②11.2LO2 ③2molH2O ④6.02×1023个 CO2分子。
(1)5gH2 的物质的量是__________,体积是__________;
(2)6.02×1023个 CO2分子的物质的量是__________,质量是__________,
(3)所含分子数最多的是_________(请用序号回答,后同);
(4)所含原子数最多的是_________;
(5)质量最大的是_________;
(6)体积最大的是_________;
(7)气体密度最大的是_________;
(8)体积最小的是_________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com