
氨气是一种重要的化工产品及工业原料。
I.某温度下,合成氨反应的平衡常数K=3.0×103(mol/L)-1,
(1)写出其对应的化学方程式____________________________________________________ 。
(2)某温度下,如果在体积恒定为10L的密闭容器中充入:0.1molN2、0.1molH2和2molNH3则反应_______(填“正向进行”或“逆向进行”或“达到平衡”)。
(3)该温度下,在体积恒定为10L的四个密闭容器中分别充入下列物质,反应达到平衡后,N2的转化率最大的是___________________。
a.10molN2、30molH2和20molNH3 b.10molN2和30molH2
c.20molN2和60molH2 d.10molN2和28molH2
II.氨气极易溶于水,氨水是氨气溶于水而形成的溶液,回答下列问题:
(4)在氨水溶液中加水稀释的过程,NH3·H2O的电离程度___________(填“增大”“减小”或“不变”), ___________(同上)。
___________(同上)。
(5)室温下,a mol/L的(NH4)2SO4水溶液的pH=5,原因是溶液中存在平衡________________________(用离子方程式表示)。并计算该平衡的平衡常数表达式为________________________(用含代数a的较为精确的数学表达式表示,不必化简,不做近似运算)。
(6)室温下,向浓度均为0.1mol/L的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为_________________________________________。
(已知:室温时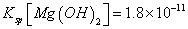 mol3
mol3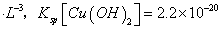 mol3.L-3).
mol3.L-3).
【答案】Ⅰ. (1)1/2 N2 + 3/2 H2 NH3(2分) (2)正向进行(2分) (3)c(2分)
NH3(2分) (2)正向进行(2分) (3)c(2分)
Ⅱ.(4)增大(1分) 不变 (2分)
(5)NH4++H2O NH3•H2O+H+ (2分) 10-5(10-5-10-9)/2a+10-9-10-5 mol·L-1(2分)
NH3•H2O+H+ (2分) 10-5(10-5-10-9)/2a+10-9-10-5 mol·L-1(2分)
(6)Cu(OH)2(1分) Cu2++2NH3·H2O=Cu(OH)2 ↓+2NH4+(2分)
【解析】
试题分析:(1)化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,则根据平衡常数可知反应的化学方程式为1/2 N2 + 3/2 H2 NH3。
NH3。
(2)在体积恒定为10L的密闭容器中充入:0.1molN2、0.1molH2和2molNH3则产生浓度熵为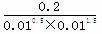 =2000<3000,所以反应向正反应方向进行。
=2000<3000,所以反应向正反应方向进行。
(3)a与b相比,a中含有大量的氨气,因此b中氨气的转化率大于a中。b与d相比,b中氢气浓度大,大转化率高;由于正方应是体积减小的可逆反应,所以增大压强平衡向正反应方向进行,c与b相比,相当于是在b的基础上增大压强,氮气转化率增大,答案选c。
(4)稀释促进氨水的电离,电离程度增大。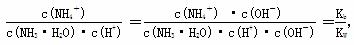 ,因此比值不变。
,因此比值不变。
(5)铵根水解溶液显酸性,方程式为NH4++H2O NH3•H2O+H+。室温下,在a mol•L-1的(NH4)2SO4水溶液中pH=5,溶液中c(H+)=10-5mol/L,故溶液中c(OH-)=10-9mol/L,根据电荷守恒有:c(NH4+)+c(H+)=c(OH-)+2c(SO42-),即c(NH4+)+10-5mol/L=10-9mol/L+2amol/L,则c(NH4+)=(2a+10-9-10-5)mol/L,根据物料守恒计算溶液中c(NH3•H2O)=2amol/L-(2a+10-9-10-5)mol/L=(10-5-10-9)mol/L,故NH4++H2O
NH3•H2O+H+。室温下,在a mol•L-1的(NH4)2SO4水溶液中pH=5,溶液中c(H+)=10-5mol/L,故溶液中c(OH-)=10-9mol/L,根据电荷守恒有:c(NH4+)+c(H+)=c(OH-)+2c(SO42-),即c(NH4+)+10-5mol/L=10-9mol/L+2amol/L,则c(NH4+)=(2a+10-9-10-5)mol/L,根据物料守恒计算溶液中c(NH3•H2O)=2amol/L-(2a+10-9-10-5)mol/L=(10-5-10-9)mol/L,故NH4++H2O NH3•H2O+H+的平衡常数的表达式为
NH3•H2O+H+的平衡常数的表达式为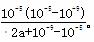 。
。
(6)溶度积常数越小的物质越先沉淀,氢氧化铜的溶度积小于氢氧化镁的溶度积,所以氢氧化铜先沉淀,铜离子和氨水反应生成氢氧化铜沉淀和铵根离子,离子方程式为Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+。
考点:考查平衡常数计算与应用、外界条件对电离平衡的影响、盐类水解以及溶度积常数应用等


科目:高中化学 来源: 题型:
Ⅰ.(12分)现有下列物质:①HNO3 ②冰醋酸 ③氨水 ④Al(OH)3 ⑤NaHCO3(s) ⑥Cu ⑦氯水 ⑧CaCO3 ⑨H2CO3 ⑩盐酸
(1)上述物质中属于强电解质的有________,属于弱电解质的有________。
(2)写出下列物质的电离方程式:
②、______________________;④、______________________;
⑤、______________________;⑨、 。
Ⅱ.(4分)化学反应4A(s)+3B(g)  2C(g)+D(g)经10 minC的浓度增加0.6 mol/L。
2C(g)+D(g)经10 minC的浓度增加0.6 mol/L。
(1)用B表示的反应速率是________ 。
(2)分别用B、C、D表示的反应速率其比值是________ 。
III.(8分)完成下列问题:
(1)汽油的重要成分是辛烷(C8H18),1molC8H18(l)在与O2(g)中燃烧,生成CO2(g)和H2O(l),放出5518KJ热量,该反应热化学方程式为:
。
(2)已知金刚石和石墨分别在氧气中完全燃烧的热化学方程式为:
C(金刚石、s)+O2(g)=CO2(g) △H=-395.41kJ/mol
C(石墨、s)+O2(g)=CO2(g) △H=-393.51kJ/mol
则石墨转化为金刚石的热化学方程式为:________ ,由此看来金刚石的稳定性 (填“大于”、“小于”、“不确定”)石墨的稳定性。
(3)发射卫星用N2H4为燃料,NO2为氧化剂,两者反应。已知:
N2(g) +2O2(g) =2NO2(g) ⊿H=67.7kJ/mol
N2H4(g) +O2(g) = N2(g) +2H2O(g) ⊿H=-534kJ/mol
H2 O (l) =H2O (g) ΔH=44 kJ/mol
1molN2H4(g)与 NO2(g)完全反应生成N2和H2 O (l)时放出热量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;
③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是
A.②④③⑤① B.③②④①⑤ C.③④②⑤① D.②④⑤③①
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是
A.钠与水反应:Na+2H2O=Na++2OH-+H2↑
B.硅酸钠溶液与醋酸溶液混合: +
+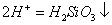
C.0.01mol/LNH4Al(SO4)2溶液与0.02mol/LBa(OH)2溶液等体积混合:
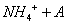 1
1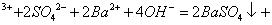 A1
A1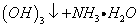
D.向次氯酸钙溶液通入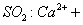
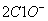 +
+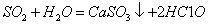
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,浓度均为0.1 mol/L的6种盐溶液pH如下:

下列说法正确的是
A. Cl2和Na2CO3按物质的量之比1:1反应的化学方程式为Cl2+Na2CO3+H2O=HClO+NaHCO3+NaCl
B.相同条件下电离程度比较:HCO3->HSO3->HClO
C.6种溶液中,Na2SiO3溶液中水的电离程度最小
D.NaHSO3溶液中离子浓度大小顺序为c(Na+)>c(H+)>c(HSO3-)>c(SO32-)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解下列物质的溶液,一段时间后,再加入一定质量的另一种物质(括号内),溶液能与原来溶液完全相同的是( )
A.CuCl2[CuO] B.NaOH[Na2O] C.NaCl[HCl] D.CuSO4[Cu(OH)2]
查看答案和解析>>
科目:高中化学 来源: 题型:
在体积恒定的密闭容器中发生反应N2O4(g)  2NO2(g);ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
2NO2(g);ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
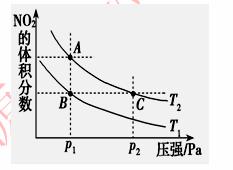
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A点深,C点浅
C.由状态B到状态A,可以用升温的方法
D.A、C两点气体的平均相对分子质量:A>C
查看答案和解析>>
科目:高中化学 来源: 题型:
下列应用或事实与胶体的性质没有关系的是( )
A.在河流入海口处易形成三角州 B.用石膏或盐卤点制豆腐
C.尿毒症患者做“血液透析”
D.在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
化学用语是化学学科的特色语言,化学用语可以准确表述化学现象、变化以及本质。完成下列有关方程式。
(1)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO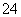 ,常用作脱氯剂,该反应的离子方程式为______________________________________________________;
,常用作脱氯剂,该反应的离子方程式为______________________________________________________;
(2)酸性高锰酸钾溶液与过氧化氢溶液反应的离子方程式:
________________________________________________________________________。
(3)化学反应多姿多彩,把SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时向溶液中滴加氯化钡溶液,有白色沉淀产生。请写出上述变化中溶液由棕黄色变为浅绿色,但立即又变为棕黄色所涉及的两个离子方程式:
________________________________、________________________________________。
(4)向含有n mol 溴化亚铁的溶液中通入等物质的量的的氯气,请写出离子方程式:
_________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com