
【题目】新旧动能转换工程之一是新能源新材料的挖掘和应用。乙二醇是重要的化工原料, 煤基合成气(CO、 H2)间接制乙二醇具有转化率高、回收率高等优点,是我国一项拥有自主知识产权的世界首创技术,制备过程如下:
反应 I: 4NO(g)+4CH3OH(g)+O2(g) ![]() 4CH3ONO(g)+2H2O(g) △H1 = a kJ·mol-1
4CH3ONO(g)+2H2O(g) △H1 = a kJ·mol-1
反应 II: 2CO(g)+2CH3ONO(g) ![]() CH3OOCCOOCH3(l) + 2NO(g) △H2= b kJ·mol-1
CH3OOCCOOCH3(l) + 2NO(g) △H2= b kJ·mol-1
反应 III: CH3OOCCOOCH3(1)+4H2(g) ![]() HOCH2CH2OH(1)+2CH3OH(g) △H3= c kJ·mol-1
HOCH2CH2OH(1)+2CH3OH(g) △H3= c kJ·mol-1
(1)请写出煤基合成气[n(CO): n(H2)= 1:2]与氧气间接合成乙二醇的总热化学方程式________,已知该反应在较低温条件下能自发进行,则该反应的△H ____0(填“>”“<”或“=”)。
(2)一定温度下,在 2 L 的密闭容器中投入物质的量均为 0.4mol的CO 和 CH3ONO发生反应 II,10min 达到平衡时CO的体积分数与NO的体积分数相等。
①下列选项能判断反应已达到化学平衡状态的是________。
a. CO 的质量不再变化 b. 混合气体的密度不再变化
c.单位时间内生成 CO 和 NO 的物质的量相等 d. CO 和 CH3ONO 的浓度比不再变化
②10min 内该反应的速率 ν(NO)=____________;该温度下化学平衡常数 K=_________。若此时向容器中再通入0.4 mol NO,一段时间后,达到新平衡时 NO的体积分数与原平衡时相比______(填“增大”“相等”“减小”或“不能确定”)。
③若该反应△H<0,在恒容的密闭容器中,反应达平衡后,改变某一条件,下列示意图正确的是____________(填字母)。
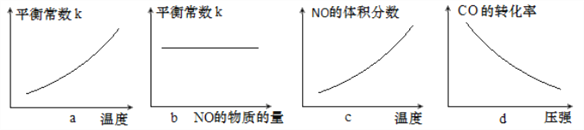
【答案】 4H2(g)+2CO(g)+1/2O2(g) ![]() HOCH2CH2OH(l)+2H2O(g) △H3=(1/2a+b+c)kJ·mol-1 < a bc 0.01mol··L-1·min-1 100 增大 b
HOCH2CH2OH(l)+2H2O(g) △H3=(1/2a+b+c)kJ·mol-1 < a bc 0.01mol··L-1·min-1 100 增大 b
【解析】(1)已知反应 I: 4NO(g)+4CH3OH(g)+O2(g) ![]() 4CH3ONO(g)+2H2O(g) △H1 = a kJ·mol-1
4CH3ONO(g)+2H2O(g) △H1 = a kJ·mol-1
反应 II: 2CO(g)+2CH3ONO(g) ![]() CH3OOCCOOCH3(l) + 2NO(g) △H2= b kJ·mol-1
CH3OOCCOOCH3(l) + 2NO(g) △H2= b kJ·mol-1
反应 III: CH3OOCCOOCH3(1)+4H2(g) ![]() HOCH2CH2OH(1)+2CH3OH(g) △H3= c kJ·mol-1
HOCH2CH2OH(1)+2CH3OH(g) △H3= c kJ·mol-1
根据盖斯定律,由I![]() + II+ III得反应4H2(g)+2CO(g)+
+ II+ III得反应4H2(g)+2CO(g)+ ![]() O2(g)
O2(g) ![]() HOCH2CH2OH(l)+2H2O(g) △H=(
HOCH2CH2OH(l)+2H2O(g) △H=(![]() a+b+c)kJ·mol-1;该反应为熵减的反应△S<0,已知该反应在较低温条件下能自发进行,要使△G=△H-T△S<0,必须△H<0;(2)①a. CO 的质量不再变化,说明反应已达平衡状态,故选; b. 该反应在恒容条件下进行且参与物质不完全为气体,气体的密度为变量,当混合气体的密度不再变化,说明反应已达平衡状态,故选;c.单位时间内生成 CO 和 NO 的物质的量相等,说明正逆反应速率相等,反应达平衡状态,故选;d. CO 和 CH3ONO 的投料相等且在反应中计量数相等,故两者的浓度比始终不变,不能作为平衡状态的判断依据,故不选。答案选a bc;
a+b+c)kJ·mol-1;该反应为熵减的反应△S<0,已知该反应在较低温条件下能自发进行,要使△G=△H-T△S<0,必须△H<0;(2)①a. CO 的质量不再变化,说明反应已达平衡状态,故选; b. 该反应在恒容条件下进行且参与物质不完全为气体,气体的密度为变量,当混合气体的密度不再变化,说明反应已达平衡状态,故选;c.单位时间内生成 CO 和 NO 的物质的量相等,说明正逆反应速率相等,反应达平衡状态,故选;d. CO 和 CH3ONO 的投料相等且在反应中计量数相等,故两者的浓度比始终不变,不能作为平衡状态的判断依据,故不选。答案选a bc;
②设平衡转化率为x,则 2CO(g)+2CH3ONO(g) ![]() CH3OOCCOOCH3(l) + 2NO(g)
CH3OOCCOOCH3(l) + 2NO(g)
开始时的浓度(mol/L) 0.2 .02 0 0
改变的浓度(mol/L) 0.2x 0.2x 0.1x 0.2x
平衡时的浓度(mol/L)0.2-0.2x 0.2-0.2x 0.1x 0.2x
10min 达到平衡时CO的体积分数与NO的体积分数相等,则0.2-0.2x=0.2x,解得x=0.5;10min 内该反应的速率 ν(NO)= ![]() 0.01mol··L-1·min-1;该温度下化学平衡常数 K=
0.01mol··L-1·min-1;该温度下化学平衡常数 K=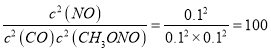 ;若此时向容器中再通入0.4 mol NO,恒容条件下相当于增大压强,平衡向气体体积缩小的正方向移动,NO的体积分数增大;故新平衡时 NO的体积分数与原平衡时相比增大;③a.该反应为气体计量数减小的放热反应,升高温度,平衡逆向移动,生成物浓度减小,反应物浓度增大,平衡常数减小,选项a错误;b平衡常数只与温度有关,与浓度无关,故NO的浓度变化,K值保持不变,选项b正确;c.该反应为放热反应,升高温度平衡逆向移动,NO的体积分数减小,选项c错误;d.该反应为气体体积缩小的反应,增大压强,平衡正向移动,CO的转化率增大,选项d错误;答案选b。
;若此时向容器中再通入0.4 mol NO,恒容条件下相当于增大压强,平衡向气体体积缩小的正方向移动,NO的体积分数增大;故新平衡时 NO的体积分数与原平衡时相比增大;③a.该反应为气体计量数减小的放热反应,升高温度,平衡逆向移动,生成物浓度减小,反应物浓度增大,平衡常数减小,选项a错误;b平衡常数只与温度有关,与浓度无关,故NO的浓度变化,K值保持不变,选项b正确;c.该反应为放热反应,升高温度平衡逆向移动,NO的体积分数减小,选项c错误;d.该反应为气体体积缩小的反应,增大压强,平衡正向移动,CO的转化率增大,选项d错误;答案选b。


科目:高中化学 来源: 题型:
【题目】短周期主族元素 W、X、Y、Z的原子序数依次增大,WX2 为红棕色气体,Y的单质既能与强酸又能与强碱反应,W、Z 最外层电子数之和是X最外层电子数的2 倍。下列说法中错误的是
A. Y 与X、Y与Z均形成离子化合物
B. 对应简单离子的半径:W>X>Y
C. Z 对应的最高价含氧酸是一元强酸
D. ZX2 是一种消毒能力强于氯气且更加安全的自来水消毒剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程中ΔH小于零的是( )
A. Ba(OH)2与NH4Cl固体混合反应 B. 氯化铵分解得氨气
C. 碳酸钙分解得二氧化碳 D. 验室制备氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,二元弱酸 H2Y 溶液中滴加 KOH 溶液,所得混合溶液的 pH 与离子浓度变化的关系如图所示,下列有关说法错误的是
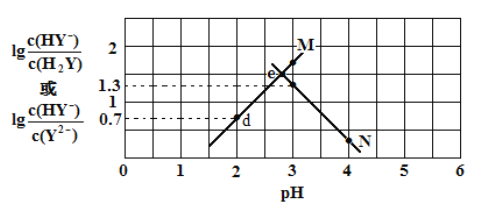
A. 曲线 M 表示 pH与![]() 的变化关系
的变化关系
B. Ka2(H2Y)=10-2.7
C. d 点溶液中: c(H+)-c(OH -)=2c(Y2-)+ c(HY-)-c(K+)
D. 交点 e 的溶液中: c(H2Y) = c(Y2-) > c(HY-)> c(H+)> c(OH -)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质之间的相互关系错误的是( )
A.12C和13C互为同位素
B.(CH3)2CHCH2CH3和CH3CH2C(CH3)3互为同分异构体
C.CH3CH3和CH3(CH2)3CH3互为同系物
D.O2和O3互为同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列物质中选择合适的物质的序号填空:①苯②乙醇③乙酸④乙酸乙酯。
(1)在加热有铜作催化剂的条件下,被氧化后的产物能发生银镜反应的是____;该催化氧化反应的化学方程式为______________________。
(2)在浓硫酸和加热条件下,能发生酯化反应的是_______________________;
(3)既能发生加成反应又能发生取代反应的是____;
(4)在无机酸或碱作用下,能发生水解反应的是____;写出其在碱性条件下水解的化学方程式_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED(Light Emitting Diode),发光二极管,是一种能够将电能转化为可见光的固态的半导体器件,它可以直接把电能转化为光能。下图是课外活动小组设计的用化学电源使LED灯发光的装置。下列说法错误的是
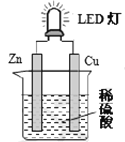
A.装置中存在“化学能→电能→光能”的转换
B.铜片上发生的反应为:2H++2e―=H2↑
C.如果将硫酸换成柠檬汁,导线中不会有电子流动
D.如果将锌片换成铁片,电路中的电流方向不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X由两种元素组成,为探究其组成和性质,设计并完成如下实验:
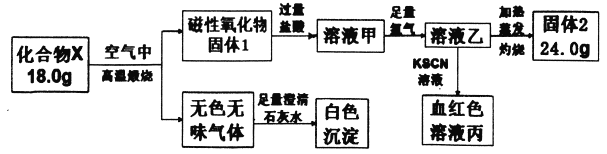
请回答:
(1)X的化学式是________。
(2)溶液甲与足量氯气反应的离子方程式为____________。
(3)加热条件下氨气被固体2氧化成一种气体单质,写出该反应的化学方程式_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com