
【题目】伪麻黄碱(D)是新康泰克的成分之一,能够缓解感冒时带来的鼻塞、流鼻涕和打喷嚏等症状,其中一种合成路线如下:
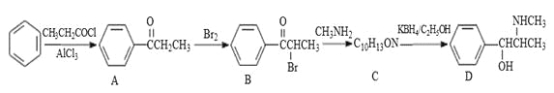
回答下列问题:
(1)伪麻黄碱(D)的分子式为 ;B中含有的官能团有 (写名称)。
(2)写出 B—C反应的化学方程式: 。C—D的反应类型为 。
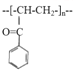
(3)B的消去产物可以用于合成高分子化合物E,请写出 E的结构简式: 。
(4)满足下列要求的A的同分异构体有 种;
①能发生银镜反应
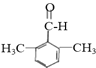
②苯环上的一氯代物有两种结构,其中核磁共振氢谱为4组峰,且峰面积之比为6:2:1:1的为 (写结构简式)。
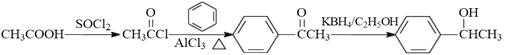
(5)已知:![]() 。参照上述合成路线,设计一条由苯和乙酸为起始原料制备
。参照上述合成路线,设计一条由苯和乙酸为起始原料制备![]() 的合成路线: 。
的合成路线: 。
【答案】(1)C10H15NO;羰基 、溴原子
(2)![]() +HBr;还原反应
+HBr;还原反应
(3)
(4)4;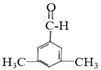
(5)
【解析】试题分析:(1)根据D的结构简式可知其分子式为C10H15NO,根据B的结构简式可知其所含的官能团为羰基和溴原子。
故答案为:C10H15NO;羰基、溴原子;
(2)比较B的结构简式与C的分子式可知,B与CH3NH2发生取代反应生成C,反应方程式为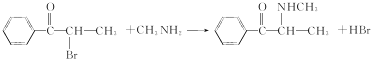 ,比较C的分子式与D的结构简式可知,C发生还原反应生成D。
,比较C的分子式与D的结构简式可知,C发生还原反应生成D。
故答案为: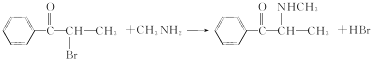 ;还原反应;
;还原反应;
(3)B中溴原子与邻位碳上的氢原子发生消去反应生成碳碳双键,碳碳双键可以发生加聚反应得到E为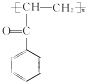 。
。
故答案为: ;
;
(4)根据条件①能发生银镜反应,说明有醛基,②苯环上的一氯代物有两种结构,即苯环上有两种位置的氢原子,则符合条件的A的同分异构体为苯环的对位上连有两个基团:-CH2CH3、-CHO或:-CH2CHO、-CH3,也可以是连有三个基团结构为: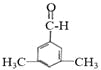 、
、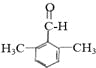 ,所以共有4种,其中核磁共振氢谱为4组峰,分子中有四种位置的氢原子,且峰面积之比为6:2:1:1,即个数比为6:2:1:1的A的同分异构体为;
,所以共有4种,其中核磁共振氢谱为4组峰,分子中有四种位置的氢原子,且峰面积之比为6:2:1:1,即个数比为6:2:1:1的A的同分异构体为; 、
、 。
。
故答案为:4; 、
、 ;
;
(5)由苯和乙酸为起始原料制备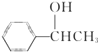 ,可以将CH3COOH与氯气发生信息中的取代反应生成CH3COCl,与苯在氯化铝作催化剂的条件下发生取代反应生成甲苯酮,甲苯酮发生还原反应即可得产品,其合成路线为:
,可以将CH3COOH与氯气发生信息中的取代反应生成CH3COCl,与苯在氯化铝作催化剂的条件下发生取代反应生成甲苯酮,甲苯酮发生还原反应即可得产品,其合成路线为: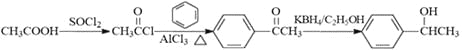 。
。
故答案为: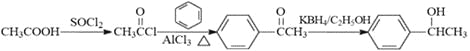 。
。


科目:高中化学 来源: 题型:
【题目】某链烃A有支链且只有一个官能团,其相对分子质量在65~75之间,1mol A完全燃烧消耗7mol氧气.
①A的结构简式是: , 名称是: .
②链烃B是A的同分异构体,分子中的所有碳原子共平面,其催化氢化产物为正戊烷,写出B的一种结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列粒子的描述不正确的是( )
A. PH3的电子式为![]() ,其热稳定性不如NH3
,其热稳定性不如NH3
B. HS-的电子式为![]() ,是含有极性键的18电子的粒子
,是含有极性键的18电子的粒子
C. CH2Cl2的电子式为![]() ,是结构呈正四面体的分子
,是结构呈正四面体的分子
D. KF的电子式为![]() ,它是易溶于水的离子化合物
,它是易溶于水的离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第四周期有18种元素,其相关化合物在化工、医药、材料等领域均有着广泛的应用。请回答下列问题:
(1)基态钙原子核外电子云形状为____________,电子占据的最高能层符号是____________。
(2)五氧化二钒(V2O5)是硫酸工业中重要的催化剂,基态钒原子的价电子排布式为____________。
(3)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,其中“亚铁”是关键成分,K3[Fe(CN)6]溶液是检验Fe2+的试剂,1molCN-中含π键的数目为____________,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是____________。
(4)镓、锗、砷、硒的第一电离能由大到小的顺序为____________(用元素符号表示);其中锗的化合物四氯化锗可用作光导纤维渗杂剂,其熔点为-49.5℃,沸点为83.1℃,则其晶体类型为____________,中心原子的杂化类型为____________;砷酸酸性弱于硒酸,从分子结构的角度解释原因____________;砷化硼是一种新型材料,或成为最好的热导体,其结构与金刚石相似,已知砷化硼晶胞参数为bpm,则该晶体的密度为____________ g ·cm-3。(NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为;
(2)反应是反应.(选填“吸热”、放热).
(3)能判断该反应是否达到化学平衡状态的依据是 .
a.容器中压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)c(CH2)=c(CO)c(H2O),试判断此时的温度为℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由钠、铜、铝、铁四种金属单质中的两种组成的合金共15g,跟足量的盐酸反应产生5.6L氢气(标准状况下),那么此合金中一定含有的金属是
A. 钠 B. 铜 C. 铝 D. 铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定铁铜合金的组成,将7.6g铁、铜合金加入100mL某浓度的稀硝酸中,待合金完全溶解后,共收集到NO气体2.24L(标准状况下),并测得溶液中H+的浓度为0.5molL﹣1 . 若反应前后溶液的体积变化忽略不计,则下列判断正确的是( )
A.上述反应中金属共失去电子0.1 mol
B.合金中,铜的质量为2.8 g
C.原硝酸的浓度:c(HNO3)=4.5 molL﹣1
D.要使溶液中的金属离子完全沉淀,需加5 molL﹣1的NaOH溶液60 mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com