
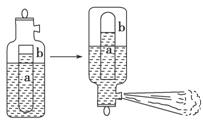
一种常用的泡沫灭火器构造如图。内筒a是玻璃瓶,外筒b是钢瓶,平时泡沫灭火器内筒外筒盛有液态试剂,当遇火警时,将灭火器取下倒置,内外筒液体试剂立即混合产生大量CO2泡沫灭火,从液态试剂在灭火器中长久放置和快速灭火两个角度分析,盛放药品正确的是( )
 A.a中盛饱和Na2CO3溶液,b中盛Al2(SO4)3溶液
A.a中盛饱和Na2CO3溶液,b中盛Al2(SO4)3溶液
B.a中盛饱和NaHCO3溶液,b中盛Al2(SO4)3溶液
C.a中盛Al2(SO4)3溶液,b中盛饱和Na2CO3溶液
D.a中盛Al2(SO4)3溶液,b中盛饱和NaHCO3溶液
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
乙炔是有机合成工业的一种重要原料。工业上曾用CaC2与水反应生成乙炔。
⑴CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为 ,1mol O22+中含有的π键数目为 。
⑵将乙炔通入[Cu(NH3)2]Cl溶液中生成红棕色沉淀Cu2C2。Cu+简写的核外电子排布式为 。
⑶乙炔与HCN反应可得到丙烯腈(CH2=CH—C≡N), 丙烯腈分子中碳原子轨道的杂化类型是 ;分子中处于同一直线上原子数目最多有 个。
⑷CaC2晶体的晶胞结构与NaCl晶体相似(如图所示),但CaC2晶体中哑铃形的C22-的存在,使晶胞沿一个方向拉长, CaC2晶体中一个Ca2+周围距离最近的C22-数目为 。

查看答案和解析>>
科目:高中化学 来源: 题型:
写出下列反应的热化学方程式:
(1)N2(g)与H2(g)反应生成1 mol NH3(g),放出46.1 kJ热量________。
(2)1 mol C(石墨)与适量H2O(g)反应生成CO(g)和H2(g),吸收131.3 kJ热量________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的( )
①NaOH(固体) ②H2O ③HCl ④CH3COONa(固体)
A.②④ B.①④ C.②③ D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
将6 g CH3COOH溶于水制得1 L溶液,此溶液的物质的量浓度为________________,经测定溶液中[CH3COO-]为1.4×10-3 mol·L-1,此温度下醋酸的电离常数:Ka=______________,温度升高Ka将________(填“变大”、“变小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各离子①R- ②R+ ③R2+ ④R3+ ⑤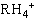 ⑥RH-(R表示不同的元素)都有10个电子,其中不会破坏水的电离平衡的有:( )
⑥RH-(R表示不同的元素)都有10个电子,其中不会破坏水的电离平衡的有:( )
A.仅有①③ B.仅有② C.②③⑥ D.②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
用0.10mol·L-1的盐酸滴定0.10mol·L-1的氨水,滴定过程中不可能出现的结果是( )
A.c(NH )>c(Cl-),c(OH-)>c(H+) B.c(NH
)>c(Cl-),c(OH-)>c(H+) B.c(NH )=c(Cl-),c(OH-)=c(H+)
)=c(Cl-),c(OH-)=c(H+)
C.c (Cl-)>c(NH ),c(OH-)>c(H+) D.c(Cl-)>c(NH
),c(OH-)>c(H+) D.c(Cl-)>c(NH ),c(H+)>c(OH-)
),c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度下等物质的量浓度的下列溶液中,c(NH4+)最大的是( )
A.NH4Cl B.NH4HCO3 C.NH4HSO4 D. (NH4)2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、L四种元素分别位于周期表中三个紧相邻的周期且原子序数依次增大,它们相关信息如下:
X元素原子的价电子构型为nsnnp2n
Y和Z位于同一周期,最外层都有两个未成对电子
L元素原子的基态未成对电子数是同周期最多的元素。
请回答如下问题:
(1)L元素在周期表中的位置是 。
该原子核外电子排布式是 。
其最高正价氧化物对应的水化物的化学式是 和 。
(2)元素X与Y形成的化合物晶体类型是 晶体
1mol该化合物含有的化学键数为 (用阿伏加德罗常数NA表示)
(3)元素M是周期表中电负性最强的元素,X与M形成的化合物XM2的分子几何构型是 ,该化合物中X原子的杂化轨道类型是 。
(4)X与碳、氢三种元素形成的相对分子质量最小的分子里有 个δ键, 个л键
(5)金属元素N与Z形成的离子化合物的晶胞结构如图,晶胞中Z离子数目为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com