
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
检验SO2中是否混有CO2气体,可采用的方法是( )
A.通过澄清的石灰水 B.通过NaOH溶液,再通过澄清石灰水
C.先通过酸性KMnO4溶液,再通过澄清石灰水
D.先通过NaHCO3溶液,再通过澄清石灰水
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化合物:①HCl ②NaOH ③CH3COOH ④NH3·H2O ⑤CH3COONa ⑥NH4Cl ⑦C2H5OH ⑧SO2
(1)属于弱电解质的是 ,溶液呈碱性的有 (填序号)。
(2)常温下0.01 mol/L NaOH溶液的pH= ;pH=11的CH3COONa溶液中由水电离产生的c(OH-) = 。
mol/L NaOH溶液的pH= ;pH=11的CH3COONa溶液中由水电离产生的c(OH-) = 。
(3)用离子方程式表示CH3COONa溶液呈碱性的原因 ,其溶液中离子浓度按由大到小的顺序为 。
 (4)常温下,向100 mL 0.01 mol·L-1HA溶液逐滴加入0.02 mol·L-1MOH 溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
(4)常温下,向100 mL 0.01 mol·L-1HA溶液逐滴加入0.02 mol·L-1MOH 溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
①由图中信息可知HA为_______酸
(填“强”或“弱”)。
②在滴加过程中,水的电离程度的变化是先 后 (填“增大”、“减小”或“不变”)
③K点对应的溶液中, c(M+)+c(MOH)= mol·L-1。
(5)在25 ℃下,向浓度均为0.01 mol·L-1的FeCl3和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),当测得溶液pH=11时,则此温度下残留在溶液中的c(Cu2+):c(Fe3+)
= 。
(已知25℃时Ksp[Fe(OH)3]=4.0×10-38, Ksp[Cu(OH)2]=2.2×10-20)
(6)25℃时,将bmol NH4NO3溶于水,向该溶液滴加aL氨水后溶液呈中性,则所滴加氨水的浓度为_______mol·L-1。(NH3·H2O的电离平衡常数取Kb = 2×10-5 mol·L-1)
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:

下列叙述正确的是( )
A.试剂X可以是氢氧化钠溶液,也可以是盐酸
B.反应①过滤后所得沉淀为氢氧化铁
C.反应②通入的过量Y是CO2气体
D.图中所示的转化反应①②都是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
2009年4月22日是第40个世界地球日,今年世界地球日的主题是“绿色世纪”。下列行为不符合这一主题的是
A.分类回收、利用垃圾,减少资源浪费
B.推广使用一次性木筷,减少疾病传染
C.开发风能等洁净能源,减少使用化石燃料
D.研究煤和石油脱硫新技术,减少酸雨发生
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对有关实验的说法正确的是
A.向盛有碘水的分液漏斗中加入无水乙醇,振荡、静置,放出有机层后再蒸馏,提取碘水中的碘
B.取淀粉、稀硫酸共热后的溶液与新制Cu(OH)2反应,无红色沉淀生成,说明淀粉未水解
C.为绘制中和滴定曲线,在滴定过程中,每隔相同时间用pH计测定一次锥形瓶中溶液的pH
D.为除去粗盐中的Ca2+、Mg2+、SO42-,先后加入的试剂是H2O、Ba(OH)2、Na2CO3、HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
下表列出了某冷轧厂排放的废水中各成份的含量及国家环保标准值的有关数据:
| 冷轧含锌废水水质 | 经处理后的水国家环保标准值 | |
| Zn2+浓度/(mg·L-1) | ≤800 | ≤3.9 |
| pH | 1~5 | 6~9 |
| SO42-浓度/(mg·L-1) | ≤23 000 | ≤150 |
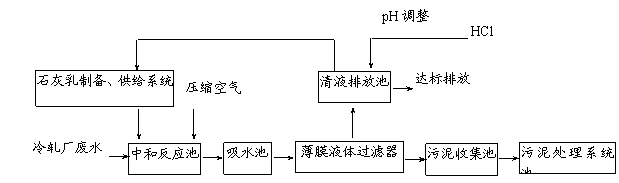 某科研机构为该厂量身定做,设计了如下废水处理系统,不但节约大量工业用水,而且大大降低了生产成本。
某科研机构为该厂量身定做,设计了如下废水处理系统,不但节约大量工业用水,而且大大降低了生产成本。
请回答下列问题:
⑴ 向中和反应池中通入压缩空气的作用是 ▲ 。
⑵ 若废水中细菌含量较高,往往用漂白粉代替石灰乳沉淀Zn2+,漂白粉沉淀Zn2+的离子方程式是
▲ 。
⑶ 污泥处理系统除去污泥后,可得到的工业副产品有 ▲ (填化学式)。
⑷ 薄膜液体过滤器是将膨体聚四氟乙烯专利技术与全自动控制系统完美地结合在一起的固液分离设备。为提高薄膜液体过滤器的过滤能力,废水处理系统工作一段时间后,需要对薄膜进行化学处理,薄膜定期处理的方法是 ▲ 。
⑸ 经上述工艺处理后的废水pH=8,此时废水中Zn2+的浓度为 ▲ mg/L(常温下,Ksp[Zn(OH)2]=1.2×10-17), ▲ (填“符合”或“不符合”)国家环保标准。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有吸水性
B.硫粉在过量的氧气中燃烧可以生成SO3
C.将少量SO2通入BaCl2溶液能生成白色沉淀
D.将浓盐酸、浓硝酸和浓硫酸分别露置在空气中,溶质的物质的量浓度都降低
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式不正确的是
A.向NH4HCO3溶液中加入过量烧碱溶液:NH4+ +OH-= NH3↑+H2O
B.将CO2通入到纯碱饱和溶液中:2Na++CO32-+CO2+H2O=2NaHCO3↓
C.向Ba(OH)2溶液中加入足量的KHSO4溶液:Ba2+ +2OH-+2H++ SO42- = BaSO4↓+2H2O
D.将饱和FeCl3溶液滴入沸水中制胶体:Fe3+ + 3 H2O Fe(OH)3(胶体) +3H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com