
| A. | 2gH2含有的氢原子数目为NA | |
| B. | 1L1mol•L-1KOH溶液中含有的钾离子数目为NA | |
| C. | 1molZn完全变为Zn2+失去的电子数目为NA | |
| D. | 常温常压下,22.4LO2含有的分子数目为NA |
分析 A.1个氢气分子含有2个氢原子;
B.依据n=CV 计算氢氧化钾的物质的量,氢氧化钾为强电解质完全电离,依次计算钾离子数目;
C.1个Zn变为Zn2+时失去2个电子;
D.常温常压下Vm≠22.4L/mol.
解答 解:A.1个氢气分子含有2个氢原子,2g H2的物质的量=$\frac{2g}{2g/mol}$=1mol,含氢原子个数为2NA,故A错误;
B.溶液中氢氧化钾的物质的量=1L×1mol•L-1 =1mol,氢氧化钾为强电解质完全电离,所以含钾离子的物质的量为1mol,个数为NA,故B正确;
C.1个Zn变为Zn2+时失去2个电子,1mol Zn变为Zn2+时失去的电子数目为2NA,故C错误;
D.常温常压下Vm≠22.4L/mol,22.4L O2的物质的量不是1mol,所以分子数不是NA,故D错误;
故选:B.
点评 本题考查阿伏加德罗常数的有关计算和判断,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,注意气体摩尔体积的使用条件.


 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:解答题
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| -c(NO)/mol•L -1 | 1.00×10 -3 | 4.50×10-4 | 2.50×10 -4 | 1.50×10 -4 | 1.00×10 -4 | 1.00×10 -4 |
| -c(CO)/mol•L-1 | 3.60×10 -3 | 3.05×10 -3 | 2.85×10 -3 | 2.75×10 -3 | 2.70×10 -3 | 2.70×10-3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
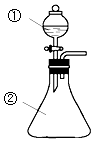 将①中液体逐滴滴入到②中(如图),实验结果与预测的现象一致的是( )
将①中液体逐滴滴入到②中(如图),实验结果与预测的现象一致的是( )| 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 氨水 | 氯化铝溶液 | 产生白色沉淀 |
| B | 浓硫酸 | 铜片 | 产生大量气体溶液变蓝 |
| C | 浓硝酸 | 用砂纸打磨过的铝条 | 产生大量红棕色气体 |
| D | 稀盐酸 | Na2CO3与NaOH的混合液 | 立即产生大量气体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2是还原产物 | |
| B. | □处对应的物质为H2O | |
| C. | 氧化剂与还原剂物质的量之比为1:8 | |
| D. | 若1mol KMnO4参加反应,转移的电子的物质的量是4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 顺-2-丁烯与反-2-丁烯与氢气加成的产物不相同 | |
| B. | 新戊烷的二氯代物有2种 | |
| C. | 分子式为C2H4和C4H8的物质一定互为同系物 | |
| D. | 键线式为 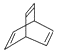 的有机物的分子式为C8H10 的有机物的分子式为C8H10 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com