
| A. | 乙炔和苯 | B. | 甲烷和乙烷 | C. | 丙烯和丙烷 | D. | 乙烷和丁烯(C4H8) |
分析 不论以何种比例混合,只要混合物的质量一定,完全燃烧后生成CO2的量也一定说明两种化合物中碳元素含量相同,据此分析解答.
解答 解:不论以何种比例混合,只要混合物的质量一定,完全燃烧后生成CO2的量也一定说明两种化合物中碳元素含量相同.
A.乙炔和苯的最简式都是CH,含碳量相同,符合条件,故A正确;
B.甲烷、乙烷的分子式分别是CH4、C2H6,含碳量不同,不符合条件,故B错误;
C.丙烯和丙烷分子式分别是C3H6、C3H8,含碳量不同,不符合条件,故C错误;
D.乙烷和丁烯的分子式分别C2H6、C4H8,含碳量不相同,不符合条件,故D错误;
故选A.
点评 本题考查混合物的有关计算,侧重考查学生分析判断能力,注意该题解答技巧,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1 L 0.5 mol•L-1 CH3COOH溶液中所含CH3COO-个数为0.5NA | |
| B. | 在Fe参与的反应中,1 mol Fe失去的电子数为3NA | |
| C. | 14 g 14N所含最外层电子数为5NA | |
| D. | 1 mol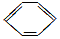 分子中含碳碳双键数为3NA 分子中含碳碳双键数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、Na+、NO3-、Cl- | B. | K+、Na+、Cl-、HCO3- | ||
| C. | Ba2+、Na+、Cl-、NO3- | D. | K+、NH4+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第3列元素种类最多,第14列元素形成的化合物种类最多 | |
| B. | 第8、9、10三列元素中没有非金属元素 | |
| C. | 只有第2列元素的原子最外层有2个电子 | |
| D. | 从上到下第1列碱金属元素的单质熔点逐渐降低,第17列元素的单质熔点逐渐升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
. ,Y2电子式
,Y2电子式 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 验证NH3给合H+的能力强于Ag+:向含有NaCl的银氨溶液中滴入过量稀硝酸,观察现象 | |
| B. | 检验某酸雨中是否含有SO42-:向酸雨试样中加入盐酸酸化的Ba(NO3)2溶液,观察现象 | |
| C. | 配制FeCl2溶液:将FeCl2溶于较浓盐酸中,然后加适量水稀释,再向配制好的溶液中加入几枚光亮的铁钉 | |
| D. | 提纯含有少量苯的苯酚:向含有少量苯的苯酚混合物中加入NaOH溶液充分振荡,静置分液;在水相中再通入足量CO2,再静置分液,取有机相-苯酚 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
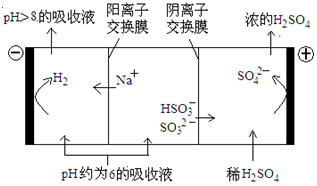
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com